20.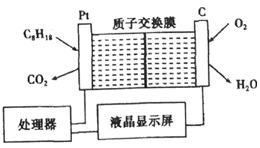 为了强化安全管理,某油库引进了一台空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液作电解质溶液).下列说法中不正确的是( )
为了强化安全管理,某油库引进了一台空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液作电解质溶液).下列说法中不正确的是( )
 为了强化安全管理,某油库引进了一台空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液作电解质溶液).下列说法中不正确的是( )
为了强化安全管理,某油库引进了一台空气中汽油含量的测量仪,其工作原理如图所示(用强酸性溶液作电解质溶液).下列说法中不正确的是( )| A. | 石墨电极作正极,发生还原反应 | |
| B. | 铂电极的电极反应式为:C8H18+16H2O-50e-═8CO2+50H+ | |
| C. | 每消耗标准状况下5.6 L O2溶液中通过lmol 电子 | |
| D. | H+由质子交换膜左侧向右侧迁移 |
19.纵观古今,化学与生活皆有着密切联系.下列有关说法错误的是( )
| A. | 草莓棚中使用的“吊袋式二氧化碳气肥”的主要成分可以是碳酸钙 | |
| B. | 制作烟花的过程中常加入金属发光剂和发色剂使烟花放出五彩缤纷的颜色 | |
| C. | “梨花淡自柳深青,柳絮飞时花满城”中柳絮的主要成分和棉花的相同 | |
| D. | 《本草纲目》记载的“凡酸坏之酒,皆可蒸烧”的实验方法可用来分离乙酸和乙醇 |
18.固体硝酸盐加热易分解且产物较复杂.某学习小组以AgNO3为研究对象,拟通过实验探究其热分解的产物,提出如下3种猜想:
甲:Ag2O、NO2、O2乙:Ag、NO2、O2 丙:Ag2O、NO2、N2
(1)实验前,小组成员经讨论认定猜想丙不成立,理由是不符合氧化还原反应原理.
查阅资料得知:
2NO2+2NaOH═NaNO3+NaNO2+H2O;Ag2O与粉末态的Ag均为黑色;Ag2O可溶于氨水.针对甲、乙猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):

(2)实验过程
①仪器连接后,放入固体试剂之前,首先进行的操作是检验装置的气密性.
②将AgNO3固体置于A中,加热前通入N2以驱尽装置内的空气,其目的是避免对产物O2检验产生干扰;关闭K,用酒精灯加热时,正确操作是先移动酒精灯预热硬质玻璃管,然后固定在管中固体部位下加热.
③观察到A 中有红棕色气体出现,C、D 中有气泡.
④待样品完全分解,A 装置冷却至室温.
⑤取少量剩余固体于试管中,加入适量水,未见明显现象.
(3)实验结果分析讨论
①证明一定有O2生成的依据是C中的溶液不褪色,且D中的溶液褪色,与此相关的化学原理为Na2SO3+H2O?NaHSO3+NaOH、2Na2SO3+O2═2Na2SO4(用化学方程式表示).
②针对试管中残留黑色固体的成分,该学习小组进行了如下探究:
【提出假设】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag和Ag2O.
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
【实验评价】根据上述实验,不能确定固体产物成分的实验是b(填实验编号).
【实验结论】根据上述实验结果,该小组得出AgNO3固体热分解的化学方程式为2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑.
(4)从实验安全的角度判断该实验装置有无缺陷?若有,应如何改进?有,应在AB装置间增加防倒吸的装置.
甲:Ag2O、NO2、O2乙:Ag、NO2、O2 丙:Ag2O、NO2、N2
(1)实验前,小组成员经讨论认定猜想丙不成立,理由是不符合氧化还原反应原理.
查阅资料得知:
2NO2+2NaOH═NaNO3+NaNO2+H2O;Ag2O与粉末态的Ag均为黑色;Ag2O可溶于氨水.针对甲、乙猜想,设计如图所示的实验装置(图中加热、夹持仪器等均省略):

(2)实验过程
①仪器连接后,放入固体试剂之前,首先进行的操作是检验装置的气密性.
②将AgNO3固体置于A中,加热前通入N2以驱尽装置内的空气,其目的是避免对产物O2检验产生干扰;关闭K,用酒精灯加热时,正确操作是先移动酒精灯预热硬质玻璃管,然后固定在管中固体部位下加热.
③观察到A 中有红棕色气体出现,C、D 中有气泡.
④待样品完全分解,A 装置冷却至室温.
⑤取少量剩余固体于试管中,加入适量水,未见明显现象.
(3)实验结果分析讨论
①证明一定有O2生成的依据是C中的溶液不褪色,且D中的溶液褪色,与此相关的化学原理为Na2SO3+H2O?NaHSO3+NaOH、2Na2SO3+O2═2Na2SO4(用化学方程式表示).
②针对试管中残留黑色固体的成分,该学习小组进行了如下探究:
【提出假设】试管中残留的黑色固体可能是:ⅰ.Ag;ⅱ.Ag2O;ⅲ.Ag和Ag2O.
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验.
| 实验编号 | 操作 | 现象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验结论】根据上述实验结果,该小组得出AgNO3固体热分解的化学方程式为2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑.
(4)从实验安全的角度判断该实验装置有无缺陷?若有,应如何改进?有,应在AB装置间增加防倒吸的装置.
17.已知25℃时,CH3COOH、HCN和H2CO3的电离常数如表:
下列有关叙述错误的是( )
| CH3COOH | HCN | H2CO3 |
| K=1.75×10-5 | K=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
| A. | 向NaCN溶液中通入少量CO2的离子方程式:CN-+H2O+CO2═HCN+HCO3- | |
| B. | 25℃时,反应CH3COOH+CN-?HCN+CH3COO-的化学平衡常数为3.57×104 | |
| C. | 中和等体积、等物质的量浓度的CH3COOH和HCN溶液,消耗NaOH的量前者小于后者 | |
| D. | 等物质的量浓度的CH3COONa和NaCN混合溶液中:c(CH3COO-)>c(CN-)>c(OH-)>c(H+) |
16.向铝土矿(含Al2O3、FeO、Fe2O3、SiO2)中加入适量硫酸溶液,分别取浸取液并向其中加入指定物质,反应后的溶液中主要存在的一组离子正确的是( )
| A. | 通入过量H2S:H+、Fe2+、Al3+、SO42- | |
| B. | 通入过量氨气:NH4+、AlO2-、OH-、SO42- | |
| C. | 加入过量NaOH溶液:Na+、AlO2-、OH-、SO42-、SiO32- | |
| D. | 加入过量NaClO溶液:Fe3+、Na+、ClO-、SO42- |
15.下列实验中,对应的现象以及结论均正确的是( )
| 选项 | 实验 | 现象 | 结论 |
| 向淀粉水解后的溶液中加入碘水 | 溶液变蓝色 | 淀粉没有水解 | |
| 将苯滴入溴水中,振荡,静置 | 溴水层褪色 | 溴和苯发生加成反应 | |
| 向1.0mol•L-1的NaHCO3溶液中滴加2滴甲基橙 | 溶液呈黄色 | NaHCO3溶液呈碱性 | |
| 相同的铝片分别与同温同体积,且c(H+)=1mol•L-1的盐酸、硫酸反应 | 铝与盐酸反应产生气泡较快 | 可能是Cl-对该反应起到促进作用 |
| A. | A | B. | B | C. | C | D. | D |
14. LiOH常用于制备锂离子电池正极材料.工业上常利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法正确的是( )
LiOH常用于制备锂离子电池正极材料.工业上常利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法正确的是( )
 LiOH常用于制备锂离子电池正极材料.工业上常利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法正确的是( )
LiOH常用于制备锂离子电池正极材料.工业上常利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法正确的是( )| A. | a是电源的负极 | |
| B. | B极区电解液为LiOH溶液 | |
| C. | A电极的电极反应式为4OH--4e-═2H2O+O2↑ | |
| D. | 外电路中每通过0.1 mol电子,生成1.12 L氢气 |
13.常温常压时烯烃与氢气混合不反应,高温时反应很慢,但在适当的催化剂存在时可与氢气反应生成烷,
一般认为加氢反应是在催化剂表面进行.反应过程的示意图如下:

下列说法中正确的是( )
一般认为加氢反应是在催化剂表面进行.反应过程的示意图如下:

下列说法中正确的是( )
| A. | 乙烯和H2生成乙烷的反应△H>0 | |
| B. | 加入催化剂,降低了E活,并减小了反应的△H | |
| C. | 图1表明,催化加氢过程中催化剂参与反应过程并形成不稳定的中间体 | |
| D. | 图2表明,催化加氢过程中催化剂将较难发生的反应分成了多个容易发生的反应,可提高反应物的转化率 |
12.下列实验操作正确的是( )

| A. | 如图1,向容量瓶中转移溶液 | |
| B. | 图2,用标准浓度的NaOH溶液滴定未知浓度的盐酸 | |
| C. | 图3,实验室用浓硫酸和乙醇共热制乙烯 | |
| D. | 图4,验证H2在Cl2中燃烧的实验现象 |
11. 含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )
含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )
0 163535 163543 163549 163553 163559 163561 163565 163571 163573 163579 163585 163589 163591 163595 163601 163603 163609 163613 163615 163619 163621 163625 163627 163629 163630 163631 163633 163634 163635 163637 163639 163643 163645 163649 163651 163655 163661 163663 163669 163673 163675 163679 163685 163691 163693 163699 163703 163705 163711 163715 163721 163729 203614
 含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )
含氮有机物对乙酰氨基酚(如图)是生活中常见感冒药的主要成分,下列有关对乙酰氨基酚的说法正确的是( )| A. | 对乙酰氨基酚的分子式为:C8H10NO2 | |
| B. | 对乙酰氨基酚可与浓溴水发生加成反应 | |
| C. | 与对乙酰氨基酚互为同分异构体,分子中含有硝基和苯环,且苯环上有三个取代基的分子共有6种 | |
| D. | 对乙酰氨基酚可以与Na2CO3发生反应,产生CO2气体 |