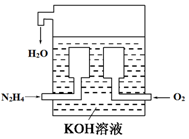
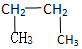8.KMnO4具有强氧化性,在实验室和工业上常用作氧化剂.某化学兴趣小组采用标准的酸性KMnO4溶液测定可能发生变质的还原性物质Na2SO3固体中Na2SO3的含量.
(1)简述检验Na2SO3已经变质的操作和现象:取少量样品于试管中,加水溶解,先加入过量盐酸,再加入氯化钡溶液,如果有白色沉淀生成,表明Na2SO3已经变质.
(2)另取10.0g试样配成250mL溶液,配制溶液时,可能用到的玻璃仪器有量筒、烧杯、玻璃棒、250 mL容量瓶、胶头滴管.取出25.00mL所配制的Na2SO3溶液于锥形瓶中,用标准酸性KMnO4溶液滴定,采用的指示剂是无(如果不需要,可写“无”).判断滴定实验达到终点的方法是当最后一滴酸性KMnO4溶液滴入锥形瓶后,瓶内溶液变成浅粉红色且半分钟内不褪色.反应的离子方程式为SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平).重复操作四次,消耗0.10mol•L-1 KMnO4溶液的体积如下:
求样品中Na2SO3的质量分数63%.
(3)操作时,若未用0.10mol•L-1的酸性KMnO4溶液润洗滴定管,会导致测定结果偏高(填“偏高”、“偏低”或“没有影响”).
(1)简述检验Na2SO3已经变质的操作和现象:取少量样品于试管中,加水溶解,先加入过量盐酸,再加入氯化钡溶液,如果有白色沉淀生成,表明Na2SO3已经变质.
(2)另取10.0g试样配成250mL溶液,配制溶液时,可能用到的玻璃仪器有量筒、烧杯、玻璃棒、250 mL容量瓶、胶头滴管.取出25.00mL所配制的Na2SO3溶液于锥形瓶中,用标准酸性KMnO4溶液滴定,采用的指示剂是无(如果不需要,可写“无”).判断滴定实验达到终点的方法是当最后一滴酸性KMnO4溶液滴入锥形瓶后,瓶内溶液变成浅粉红色且半分钟内不褪色.反应的离子方程式为SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平).重复操作四次,消耗0.10mol•L-1 KMnO4溶液的体积如下:
| 编号溶液 | 1 | 2 | 3 | 4 |
| KMnO4(mL) | 20.01 | 19.00 | 19.99 | 20.00 |
| Na2SO3(mL) | 25.00 | 25.00 | 25.00 | 25.00 |
(3)操作时,若未用0.10mol•L-1的酸性KMnO4溶液润洗滴定管,会导致测定结果偏高(填“偏高”、“偏低”或“没有影响”).
6.某有机物的结构简式为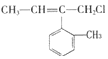 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )
 ,则该物质不能发生的反应有( )
,则该物质不能发生的反应有( )| A. | 加成反应 | B. | 氧化反应 | C. | 取代反应 | D. | 消去反应 |
4.现用邻苯二甲酸氢钾标准溶液来测定某NaOH溶液的浓度,进行如下操作:
步骤I:用天平精确称取5.207 g邻苯二甲酸氢钾(相对分子质量为204.2)固体配成 250 mL标准溶液.
步骤Ⅱ:移取25.00 mL标准溶液于250 mL锥形瓶中,加入1~2滴酚酞试液,用NaOH待测溶液滴定至终点.再按上述方法重复操作2次.
(1)操作I中,所得邻苯二甲酸氢钾标准溶液的物质的量浓度是0.1020 mol/L.
(2)滴定结果记录如下:
①滴定过程中发生反应的化学方程式是(有机物写结构简式) .
.
②待测NaOH溶液的物质的量浓度为0.1275 mol/L.
(3)根据步骤Ⅱ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH待测溶液进行滴定,则测得NaOH溶液的浓度偏低(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH待测溶液的体积无影响(填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶内溶液颜色的变化.
④滴定终点时溶液的颜色如何变化?由无色变为浅红色,半分钟内不褪色.
步骤I:用天平精确称取5.207 g邻苯二甲酸氢钾(相对分子质量为204.2)固体配成 250 mL标准溶液.
步骤Ⅱ:移取25.00 mL标准溶液于250 mL锥形瓶中,加入1~2滴酚酞试液,用NaOH待测溶液滴定至终点.再按上述方法重复操作2次.
(1)操作I中,所得邻苯二甲酸氢钾标准溶液的物质的量浓度是0.1020 mol/L.
(2)滴定结果记录如下:
| 滴定次数 | 标准溶液的体积/mL | 待测溶液的体积 | |
| 滴定前刻度/mL | 滴定后刻度/mL | ||
| 1 | 25.00 | 1.02 | 21.04 |
| 2 | 25.00 | 2.00 | 21.98 |
| 3 | 25.00 | 0.20 | 20.20 |
 .
.②待测NaOH溶液的物质的量浓度为0.1275 mol/L.
(3)根据步骤Ⅱ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH待测溶液进行滴定,则测得NaOH溶液的浓度偏低(填“偏高”、“偏低”或“无影响”).
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH待测溶液的体积无影响(填“偏大”、“偏小”或“无影响”).
③滴定时边滴边摇动锥形瓶,眼睛应观察锥形瓶内溶液颜色的变化.
④滴定终点时溶液的颜色如何变化?由无色变为浅红色,半分钟内不褪色.
3. 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净,再用待测溶液润洗后,注入待测溶液,然后调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③用蒸馏水将锥形瓶洗净后,从碱式滴定管中放入20.00mL待测溶液,滴入甲基橙作指示剂,然后用标准盐酸进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL;
④重复以上过程,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中溶液的颜色从黄色变为橙色时,停止滴定.
(2)图1中,第②步“调节滴定管的尖嘴部分充满溶液”方法正确的是②,如果滴定前有气泡,滴定后气泡消失,由此对测定结果形成的影响是偏高(填“偏高”、“偏低”或“无影响”)
(3)图2中是某次滴定时的滴定管中的液面,其读数为23.60mL.
(4)根据下列数据:
请计算待测烧碱溶液的浓度为0.1200mol/L.
 某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:①将碱式滴定管用蒸馏水洗净,再用待测溶液润洗后,注入待测溶液,然后调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
②将酸式滴定管用蒸馏水洗净,再用标准酸液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;
③用蒸馏水将锥形瓶洗净后,从碱式滴定管中放入20.00mL待测溶液,滴入甲基橙作指示剂,然后用标准盐酸进行滴定.滴定至指示剂刚好变色,且半分钟内颜色不再改变为止,测得所耗盐酸的体积为V1mL;
④重复以上过程,测得所耗盐酸的体积为V2mL.
试回答下列问题:
(1)锥形瓶中溶液的颜色从黄色变为橙色时,停止滴定.
(2)图1中,第②步“调节滴定管的尖嘴部分充满溶液”方法正确的是②,如果滴定前有气泡,滴定后气泡消失,由此对测定结果形成的影响是偏高(填“偏高”、“偏低”或“无影响”)
(3)图2中是某次滴定时的滴定管中的液面,其读数为23.60mL.
(4)根据下列数据:
| 滴定次数 | 待测液体积 | 标准盐酸体积(mL) | |
| 滴定前读数(mL) | 滴定后读数(mL) | ||
| 第一次 | 20.00 | 0.20 | 24.10 |
| 第二次 | 20.00 | 3.00 | 27.10 |
2.下列变化属于物理变化的是( )
| A. | 煤的气化 | B. | 煤的干馏 | C. | 石油的分馏 | D. | 乙烯聚合 |
1.如图表示某有机反应的过程,该反应的类型是( )


| A. | 取代反应 | B. | 加成反应 | C. | 氧化反应 | D. | 加聚反应 |
20.一定条件下,溶液的酸碱性对TiO2光催化染料R降解反应的影响如图所示.下列判断正确的是( )
0 163466 163474 163480 163484 163490 163492 163496 163502 163504 163510 163516 163520 163522 163526 163532 163534 163540 163544 163546 163550 163552 163556 163558 163560 163561 163562 163564 163565 163566 163568 163570 163574 163576 163580 163582 163586 163592 163594 163600 163604 163606 163610 163616 163622 163624 163630 163634 163636 163642 163646 163652 163660 203614

| A. | 在20~25min之间,pH=10时R的平均降解速率为0.04 mol•L-1•min-1 | |
| B. | 溶液酸性越强,R的降解速率越小 | |
| C. | R的起始浓度越小,降解速率越大 | |
| D. | 50min时,pH=2和pH=7时R的降解百分率相等 |