5.下表是25℃时三种弱酸的电离平衡常数:
回答下列问题:
(1)用离子方程式表示NaNO2溶液呈碱性的原因NO2-+H2O?HNO2+OH-.
(2)NaHCO3的电离方程式是NaHCO3=Na++HCO3-.
(3)A-、CO32-、HCO3-在水中结合H+的能力由大到小的顺序为CO32->A->HCO3->NO2-.
(4)25℃时,等物质的量浓度的HA和NaA的混合溶液呈碱性,则该混合溶液中各离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+),解释HA和NaA的混合溶液呈碱性的原因A-离子水解程度大于HA电离程度.
(5)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-.
(6)某同学用Na2CO3和NaHCO3溶液进行如图所示实验.
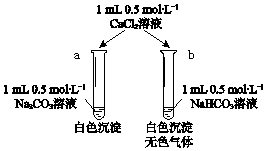
①充分反应后a试管中大量存在的离子是Na+、Cl-.
②用离子方程式表示b试管中发生的反应2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O.
| 化学式 | HA(A代表某种酸根) | HNO2 | H2CO3 |
| Ka | Ka=4.9×10-10 | Ka=4.6×10-4 | Ka1=4.1×10-7 Ka2=5.6×10-11 |
(1)用离子方程式表示NaNO2溶液呈碱性的原因NO2-+H2O?HNO2+OH-.
(2)NaHCO3的电离方程式是NaHCO3=Na++HCO3-.
(3)A-、CO32-、HCO3-在水中结合H+的能力由大到小的顺序为CO32->A->HCO3->NO2-.
(4)25℃时,等物质的量浓度的HA和NaA的混合溶液呈碱性,则该混合溶液中各离子浓度大小关系为c(Na+)>c(A-)>c(OH-)>c(H+),解释HA和NaA的混合溶液呈碱性的原因A-离子水解程度大于HA电离程度.
(5)写出NaA溶液中通少量CO2的离子方程式A-+CO2+H2O=HA+HCO3-.
(6)某同学用Na2CO3和NaHCO3溶液进行如图所示实验.

①充分反应后a试管中大量存在的离子是Na+、Cl-.
②用离子方程式表示b试管中发生的反应2HCO3-+Ca2+=CaCO3↓+CO2↑+H2O.
4.下列事实不能用平衡移动原理解释的是( )
| A. | 由H2、I2(g)、HI组成的平衡体系,缩小体积后颜色加深 | |
| B. | 实验室用排饱和食盐水的方法收集氯气 | |
| C. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 | |
| D. | 加压有利于N2和H2在一定的条件下转化为NH3 |
2.食盐中所加的碘以碘酸钾(KIO3)形式存在.根据反应:IO3-+5I-+6H+═3I2+3H2O,可用淀粉KI试纸和食醋进行实验,证明加碘食盐中存在IO3-.下列说法不正确的是( )
| A. | 实验时可观察到试纸变蓝 | |
| B. | 实验可证明该条件下I-可被IO3-氧化 | |
| C. | 上述反应中氧化剂和还原剂的物质的量之比为1:5 | |
| D. | 可根据元素周期律推断出酸性:HIO3<HClO3 |
20.在酯化反应CH3COOH+HOC2H5→CH3COOCH2CH3+H2O中,若乙醇中的氧采用18O,则反应体系中,不可能存在的物质是( )
| A. | CH3CO18OH | B. | H218O | C. | C2H518OH | D. | CH3CO18OC2H5 |
19.下列原子结构示意图表示的元素与 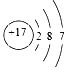 的元素同主族的是( )
的元素同主族的是( )
 的元素同主族的是( )
的元素同主族的是( )| A. |  | B. |  | C. |  | D. |  |
18.下列各组物质中属于同系物的是( )
| A. | 金刚石和C60 | B. | 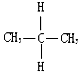 与 与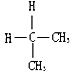 | ||
| C. | 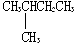 与 与 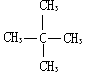 | D. | CH3CH3与CH3CH2CH2CH3 |
16.下列反应中,既属于氧化还原反应同时又是吸热反应的是( )
0 163363 163371 163377 163381 163387 163389 163393 163399 163401 163407 163413 163417 163419 163423 163429 163431 163437 163441 163443 163447 163449 163453 163455 163457 163458 163459 163461 163462 163463 163465 163467 163471 163473 163477 163479 163483 163489 163491 163497 163501 163503 163507 163513 163519 163521 163527 163531 163533 163539 163543 163549 163557 203614
| A. | Ba(OH)2•8H2O与NH4Cl反应 | B. | 甲烷与O2的燃烧反应 | ||
| C. | 铝与稀盐酸 | D. | 灼热的炭与CO2反应 |
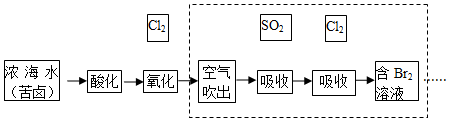
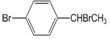 .写出该两步反应所需的试剂及条件:液溴、溴化铁作催化剂,溴、光照
.写出该两步反应所需的试剂及条件:液溴、溴化铁作催化剂,溴、光照 .
. .
.