题目内容
4.下列事实不能用平衡移动原理解释的是( )| A. | 由H2、I2(g)、HI组成的平衡体系,缩小体积后颜色加深 | |
| B. | 实验室用排饱和食盐水的方法收集氯气 | |
| C. | 工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率 | |
| D. | 加压有利于N2和H2在一定的条件下转化为NH3 |
分析 勒夏特列原理为:如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动.使用勒夏特列原理时,该反应必须是可逆反应,否则勒夏特列原理不适用.
解答 解:A.由H2、I2(g)、HI气体组成的平衡,反应前后气体体积不变,减压后平衡不动,体积增大颜色变浅,不能用勒夏特列原理解释,故A选;
B.实验室用排饱和食盐水法收集氯气,利用饱和食盐水中氯离子浓度使平衡逆向进行,Cl2+H2O?H++Cl-+HClO,可以用勒夏特列原理解释,故B不选;
C.工业上生产硫酸的过程中,二氧化硫和氧气反应生成三氧化硫为可逆反应,使用过量的空气促进平衡正向进行,以提高二氧化硫的利用率,可以用勒夏特列原理解释,故C不选;
D.合成氨反应是气体体积减小的反应,合成氨工厂学采用增大压强以提高原料的利用率,可以用勒夏特列原理解释,故D不选;
故选A.
点评 本题考查了化学平衡移动原理的分析判断,为高频考点,侧重于学生的分析能力的考查,影响因素的分析,平衡移动原理的理解是解题关键,题目难度中等.

练习册系列答案
相关题目
15.合成氨反应中,下列措施不能加快化学反应速率的是( )
| A. | 升高温度 | B. | 降低温度 | ||
| C. | 增大反应物浓度 | D. | 使用合适的催化剂 |
16.下列叙述正确的是( )
| A. | 同一周期元素的原子,半径越小越容易失去电子 | |
| B. | 元素周期表中的所有元素都是从自然界中发现的,过渡元素都是金属元素 | |
| C. | 非金属元素形成的共价化合物中,原子的最外层都达到了8电子的稳定结构 | |
| D. | 第ⅠA族与第ⅦA族元素间可形成共价化合物或离子化合物 |
19.下列原子结构示意图表示的元素与 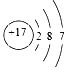 的元素同主族的是( )
的元素同主族的是( )
 的元素同主族的是( )
的元素同主族的是( )| A. |  | B. |  | C. |  | D. |  |
9.下列变化的有机反应的类型,不正确的是( )
| A. | CH3CH3→CH3CH2Cl 取代反应 | B. | CH2═CH2→CH3CH2OH 取代反应 | ||
| C. | CH2═CH2→CH2BrCH2Br 加成反应 | D. |  取代反应 取代反应 |
16.化学与生产、生活密切相关.下列叙述错误的是( )
| A. | 料酒可以除去食物中的腥味 | |
| B. | 裂化汽油可用于萃取碘水中的碘单质 | |
| C. | 葡萄糖可用于补钙药物的合成 | |
| D. | 次氯酸钠溶液可用于环境的消毒杀菌 |
15.下列各组物质中所含化学键类型完全相同的是( )
| A. | NaF、NH4Cl | B. | NaOH、NaClO | C. | CaO、Na2O2 | D. | MgCl2、Mg(OH)2 |
16.为了除去MnSO4酸性溶液中的Fe3+,可加入过量的某种试剂充分搅拌,过滤.该试剂是( )
| A. | MnCO3 | B. | MnO2 | C. | Na2CO3 | D. | 氨水 |

 +
+ $\stackrel{△}{→}$
$\stackrel{△}{→}$

 .
. 、
、 ;
;