15.(1)基态Cl原子中,电子占据的最高能层符号为M.
(2)金属锂氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
M是Mg (填元素符号).
(3)金属Cu的原子堆积模型为;Cu2+基态的电子排布式为1s22s22p63s23p63d9;向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4•H2O晶体,硫酸根离子中硫原子的杂化方式为sp3;不考虑空间构型,其内界结构可用示意图表示为 .
.
(4)某单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示,若已知该原子半径为d,NA表示阿伏伽德罗常数.摩尔质量为M,则该原子的配位数为12,该晶体的密度可表示为$\frac{{M}_{r}}{4\sqrt{2}{d}^{3}{N}_{A}}$.

(2)金属锂氢化物是具有良好发展前景的储氢材料.
①LiH中,离子半径Li+<H-(填“>”、“=”或“<”).
②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
| I1/kJ•mol-1 | I2/kJ•mol-1 | I3/kJ•mol-1 | I4/kJ•mol-1 | I5/kJ•mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
(3)金属Cu的原子堆积模型为;Cu2+基态的电子排布式为1s22s22p63s23p63d9;向硫酸铜溶液中加入过量氨水,然后加入适量乙醇,溶液中会析出深蓝色的[Cu(NH3)4]SO4•H2O晶体,硫酸根离子中硫原子的杂化方式为sp3;不考虑空间构型,其内界结构可用示意图表示为
 .
.(4)某单质的晶体中原子的堆积方式如图甲所示,其晶胞特征如图乙所示,原子之间相互位置关系的平面图如图丙所示,若已知该原子半径为d,NA表示阿伏伽德罗常数.摩尔质量为M,则该原子的配位数为12,该晶体的密度可表示为$\frac{{M}_{r}}{4\sqrt{2}{d}^{3}{N}_{A}}$.

12.以菱镁矿(主要成分为MgCO3,含少量FeCO3)为原料制备高纯氧化镁的实验流程如图:

已知:
(1)MgCO3与稀硫酸反应的离子方程式为MgCO3+2H+=Mg2++H2O+CO2↑.
(2)加入H2O2氧化时,反应体系中的反应物和生成物有:FeSO4、H2O2、H2SO4、Fe2(SO4)3、H2O,该反应中的还原剂是FeSO4(填化学式,下同)、还原产物是H2O.
(3)滤渣2的成分是Fe(OH)3(填化学式).
(4)煅烧过程存在以下反应:
①2MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$2MgO+2SO2↑+CO2↑
②MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$MgO+SO2↑+CO↑
③MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑
反应①中若生成40gMgO,转移电子物质的量为2mol.

已知:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Mg2+ | 8.1 | 9.4 |
(2)加入H2O2氧化时,反应体系中的反应物和生成物有:FeSO4、H2O2、H2SO4、Fe2(SO4)3、H2O,该反应中的还原剂是FeSO4(填化学式,下同)、还原产物是H2O.
(3)滤渣2的成分是Fe(OH)3(填化学式).
(4)煅烧过程存在以下反应:
①2MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$2MgO+2SO2↑+CO2↑
②MgSO4+C$\frac{\underline{\;800℃\;}}{\;}$MgO+SO2↑+CO↑
③MgSO4+3C$\frac{\underline{\;800℃\;}}{\;}$MgO+S↑+3CO↑
反应①中若生成40gMgO,转移电子物质的量为2mol.
8.氮的固定是几百年来科学家一直研究的课题.
(1)表列举了不同温度下大气固氮和工业固氮的部分K值.
①分析数据可知:大气固氮反应属于吸热(填“吸热”或“放热”)反应.
②分析数据可知:人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适.
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较р1、р2的大小关系р1<р1.(填“<”、“>”或者“=”)

0 163287 163295 163301 163305 163311 163313 163317 163323 163325 163331 163337 163341 163343 163347 163353 163355 163361 163365 163367 163371 163373 163377 163379 163381 163382 163383 163385 163386 163387 163389 163391 163395 163397 163401 163403 163407 163413 163415 163421 163425 163427 163431 163437 163443 163445 163451 163455 163457 163463 163467 163473 163481 203614
(1)表列举了不同温度下大气固氮和工业固氮的部分K值.
| 反应 | 大气固氮 N2 (g)+O2 (g)?2NO(g) | 工业固氮 N2 (g)+3H2 (g)?2NH3(g) | |||
| 温度/℃ | 27 | 2000 | 25 | 400 | 450 |
| K | 3.84×10-31 | 0.1 | 5×108 | 0.507 | 0.152 |
②分析数据可知:人类不适合大规模模拟大气固氮的原因K值小,正向进行的程度小(或转化率低),不适合大规模生产.
③从平衡视角考虑,工业固氮应该选择常温条件,但实际工业生产却选择500℃左右的高温,解释其原因从反应速率角度考虑,高温更好,但从催化剂活性等综合因素考虑选择500℃左右合适.
(2)工业固氮反应中,在其他条件相同时,分别测定N2的平衡转化率在不同压强(р1、р2)下随温度变化的曲线,如图所示的图示中,正确的是A(填“A”或“B”);比较р1、р2的大小关系р1<р1.(填“<”、“>”或者“=”)


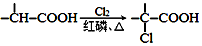

 +NaOH $→_{△}^{水}$
+NaOH $→_{△}^{水}$ +NaCl.
+NaCl. .
. 为原料制取
为原料制取  的合成路线图.合成路线图示例如下:
的合成路线图.合成路线图示例如下:

 .
. .
. .
. .
. .
.
 +2nH2O⑩
+2nH2O⑩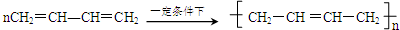

 在容积为 1.0L 的密闭容器中进行反应:A(g)=B(g)+C(g),A 的初始浓度为 0.5mol?L-1.在温度T1、T2 下,A 的浓度与时间关系如图所示,回答下列问题:
在容积为 1.0L 的密闭容器中进行反应:A(g)=B(g)+C(g),A 的初始浓度为 0.5mol?L-1.在温度T1、T2 下,A 的浓度与时间关系如图所示,回答下列问题: .
. .
. .
. 、
、 .
.