6.SO2是高中化学重点学习的三大气体之一,是常见的大气污染物之一,同时也是重要的工业原料,探究其制备方法和性质具有非常重要的意义,请回答下列问题.
Ⅰ.某研究小组将纯净的SO2气体通入0.5mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀.为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设一:
①请在下表空白处填写相关实验现象
②设计实验一的目的是做对比实验.
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图甲.实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2NO3-+2H2O=3SO42-+2NO↑+4H+.
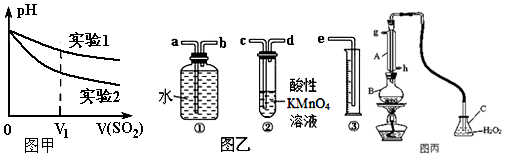
Ⅱ.我国规定空气中SO2含量不得超过0.02mg/L.某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量.
(1)若原料气从左向右流,上述装置连接的顺序是:原料气→c→d→b→a→e(用字母和箭头表示).当装置②中出现溶液紫(或紫红)色褪去现象时,立即停止通气.
(2)你认为以下试剂中,可以用来代替试管中的酸性高锰酸钾溶液的是B.
A.NaOH溶液 B.溴水C.氨水 D.BaCl2溶液
Ⅲ.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L.某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对含量定性测定.
(1)B中加入250.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为0.192g/L.
(2)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施盐酸易挥发,用不挥发的强酸例如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,排除盐酸挥发的影响.
Ⅰ.某研究小组将纯净的SO2气体通入0.5mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀.为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设一:
①请在下表空白处填写相关实验现象
| 实 验 步 骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的10mL 0.5mol/L BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体. | 无现象 | 假设一成立 |
| 实验2:在盛有不含O2的10mL 0.5mol/L Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体. | 白色沉淀生成 |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图甲.实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2NO3-+2H2O=3SO42-+2NO↑+4H+.

Ⅱ.我国规定空气中SO2含量不得超过0.02mg/L.某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量.
(1)若原料气从左向右流,上述装置连接的顺序是:原料气→c→d→b→a→e(用字母和箭头表示).当装置②中出现溶液紫(或紫红)色褪去现象时,立即停止通气.
(2)你认为以下试剂中,可以用来代替试管中的酸性高锰酸钾溶液的是B.
A.NaOH溶液 B.溴水C.氨水 D.BaCl2溶液
Ⅲ.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L.某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对含量定性测定.
(1)B中加入250.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为0.192g/L.
(2)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施盐酸易挥发,用不挥发的强酸例如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,排除盐酸挥发的影响.
4. 氢氧化铝可用于阻燃和药物等领域.
氢氧化铝可用于阻燃和药物等领域.
(1)已知:Ksp[Al(OH)3]=1.3×10-33.实验室利用Al2(SO4)3溶液与氨水反应制备Al(OH)3,若使反应后的溶液中c(Al3+)<1.3×10-6 mol•L-1,应控制溶液pH5.
(2)Al(OH)3可添加到可燃性高聚物中用作阻燃剂,请写出两条其阻燃的原因:Al(OH)3受热分解吸热,抑制聚合物升温;使可燃性高聚物浓度下降;或受热分解放出水汽稀释可燃性气体和氧气的浓度;或分解产生的Al2O3可隔绝氧气;或使塑料等高聚物炭化而不易产生挥发性物质,从而阻止火焰蔓延.
(3)胃舒平药片中含有Al(OH)3和三硅酸镁(Mg2Si3O8•5H2O)等.通过下列实验测定药片中Al(OH)3含量.
已知:测定过程中,EDTA与Al3+、Mg2+、Zn2+均按物质的量1:1反应,发生反应的pH如表所示:
步骤一:准确称取0.7425g Zn(NO3)2•6H2O,用蒸馏水溶解,定容成250mL Zn(NO3)2标准溶液;另配制EDTA溶液250mL,取25.00mL EDTA溶液,调pH为5~6并加入指示剂,用Zn(NO3)2标准溶液滴定至终点,消耗Zn(NO3)2标准溶液50.00mL.
步骤二:取10片(0.45g/片)胃舒平研细,称取2.2500g研细后的粉末,加入足量盐酸和蒸馏水,煮沸、过滤、洗涤沉淀2次,洗涤液与滤液合并,定容成250mL溶液A.
步骤三:移取5.00mL溶液A,调pH=4,准确加入步骤一中配制的EDTA溶液25.00mL,煮沸,充分反应后,调pH为5~6并加入指示剂,以步骤一中配制的Zn(NO3)2标准溶液滴定过量的EDTA至终点,消耗Zn(NO3)2标准溶液20.00mL.
①计算每片胃舒平中Al(OH)3的质量.
②步骤一滴定终点时俯视读数,会使测得胃舒平药片中Al(OH)3的质量偏小(填“偏大”、“偏小”或“不变”).
 氢氧化铝可用于阻燃和药物等领域.
氢氧化铝可用于阻燃和药物等领域.(1)已知:Ksp[Al(OH)3]=1.3×10-33.实验室利用Al2(SO4)3溶液与氨水反应制备Al(OH)3,若使反应后的溶液中c(Al3+)<1.3×10-6 mol•L-1,应控制溶液pH5.
(2)Al(OH)3可添加到可燃性高聚物中用作阻燃剂,请写出两条其阻燃的原因:Al(OH)3受热分解吸热,抑制聚合物升温;使可燃性高聚物浓度下降;或受热分解放出水汽稀释可燃性气体和氧气的浓度;或分解产生的Al2O3可隔绝氧气;或使塑料等高聚物炭化而不易产生挥发性物质,从而阻止火焰蔓延.
(3)胃舒平药片中含有Al(OH)3和三硅酸镁(Mg2Si3O8•5H2O)等.通过下列实验测定药片中Al(OH)3含量.
已知:测定过程中,EDTA与Al3+、Mg2+、Zn2+均按物质的量1:1反应,发生反应的pH如表所示:
| 金属离子 | Al3+ | Zn2+ | Mg2+ |
| 与EDTA反应的pH | 4 | 5~6 | 9.5~10 |
步骤二:取10片(0.45g/片)胃舒平研细,称取2.2500g研细后的粉末,加入足量盐酸和蒸馏水,煮沸、过滤、洗涤沉淀2次,洗涤液与滤液合并,定容成250mL溶液A.
步骤三:移取5.00mL溶液A,调pH=4,准确加入步骤一中配制的EDTA溶液25.00mL,煮沸,充分反应后,调pH为5~6并加入指示剂,以步骤一中配制的Zn(NO3)2标准溶液滴定过量的EDTA至终点,消耗Zn(NO3)2标准溶液20.00mL.
①计算每片胃舒平中Al(OH)3的质量.
②步骤一滴定终点时俯视读数,会使测得胃舒平药片中Al(OH)3的质量偏小(填“偏大”、“偏小”或“不变”).
3.硫酸亚铁铵[(NH4)2Fe(SO4)2]是一种重要的化工原料,用途十分广泛.它可以作净水剂,在无机化学工业中,它是制取其它铁化合物的原料.
【査阅资料】隔绝空气加热至500℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等.
【实验探究】某化学小组选用图1所示部分装置进行实验(部分夹持装置略)
(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分.
①所选用装置的正确连接顺序为ACBD(填装置的字母序号).
②A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含 FeO 或 Fe3O4:取少量A中残留固体加入适量稀硫酸使其完全溶解,向溶液中滴加少量酸性高锰酸钾溶液,若高锰酸钾溶液不褪色,则残留固体是Fe2O3而不含FeO和Fe3O4.
(2)探究分解产物中的硫氧化物,连接装置A-E-F-B进行实验.
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是分解产物中有SO2,没有SO3.
②实验证明(NH4)2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式2(NH4)2Fe(SO4)2$\frac{\underline{\;500°C\;}}{\;}$Fe2O3+4SO2↑+2NH3↑+N2↑+5H2O↑.
(3)已知BaSO3、BaSO4均难溶于水,化学小组利用上述实验分离出的SO2气体,进行与可溶性钡盐溶液反应的探究实验(图2).
①步骤Ⅱ的现象说明实验中产生的白色沉淀是BaSO4(填化学式).
②关于G中有白色沉淀产生的原因,你认为可能是由于装置中的氧气参加了反应.
③写出H中发生反应的离子方程式3SO2+3Ba2++2NO3-+2H2O=3BaSO4↓+2NO↑+4H+.
【査阅资料】隔绝空气加热至500℃时硫酸亚铁铵能完全分解,分解产物中含有铁氧化物、硫氧化物、氨气和水蒸气等.
【实验探究】某化学小组选用图1所示部分装置进行实验(部分夹持装置略)

(1)验证分解产物中含有氨气和水蒸气,并探究残留固体成分.
①所选用装置的正确连接顺序为ACBD(填装置的字母序号).
②A中固体完全分解后变为红棕色粉末,设计实验证明A中残留固体仅为Fe2O3,而不含 FeO 或 Fe3O4:取少量A中残留固体加入适量稀硫酸使其完全溶解,向溶液中滴加少量酸性高锰酸钾溶液,若高锰酸钾溶液不褪色,则残留固体是Fe2O3而不含FeO和Fe3O4.
(2)探究分解产物中的硫氧化物,连接装置A-E-F-B进行实验.
①实验过程中观察到:E中没有明显现象,F中溶液褪色,据此得出的结论是分解产物中有SO2,没有SO3.
②实验证明(NH4)2Fe(SO4)2受热分解除上述产物外,还有N2生成,写出A中反应的化学方程式2(NH4)2Fe(SO4)2$\frac{\underline{\;500°C\;}}{\;}$Fe2O3+4SO2↑+2NH3↑+N2↑+5H2O↑.
(3)已知BaSO3、BaSO4均难溶于水,化学小组利用上述实验分离出的SO2气体,进行与可溶性钡盐溶液反应的探究实验(图2).
| 序号 | 步骤 | 现象 |
| I | 向图2装置内充SO2气体 | G中:有气泡冒出,产生白色沉淀;H中:有气泡冒出,产生白色沉淀;液面上方先略显红棕色,后逐渐消失 |
| Ⅱ | 从G、H中过滤出白色沉淀,分别加入稀盐酸中 | G、H中的白色沉淀均不溶解 |
②关于G中有白色沉淀产生的原因,你认为可能是由于装置中的氧气参加了反应.
③写出H中发生反应的离子方程式3SO2+3Ba2++2NO3-+2H2O=3BaSO4↓+2NO↑+4H+.
2. 实验室制备1,2-二溴乙烷的原理:
实验室制备1,2-二溴乙烷的原理:
CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
有关数据列表如下:
(1)在反应中若加热后发现未加沸石,应采取的正确方法是冷却后补加;判断该制备反应已经结束的最简单方法是溴的颜色已完全褪色.
(2)装置C中应加入c,吸收反应中产生的某些有影响的杂质气体(填写正确选项前的字母)
a.水 b.浓硫酸 c.NaOH溶液 d.KMnO4溶液
(3)装置B中竖直的长导管起安全管的作用,其原理是当B中的压强过大时,安全管中液面上升,从而调节B中气压相对稳定.
(4)若产物中有少量Br2,最好用d洗涤除去(填写正确选项前的字母)
a.水 b.乙醇 c.KI溶液 d.NaHSO3溶液
发生反应的化学方程为NaHSO3+Br2+H2O=NaHSO4+2HBr.
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,主要目的是乙烯与溴水反应放热,冷却可避免溴的大量挥发,但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的熔点为9℃,过度冷却会使凝固而使气路堵塞.
0 163247 163255 163261 163265 163271 163273 163277 163283 163285 163291 163297 163301 163303 163307 163313 163315 163321 163325 163327 163331 163333 163337 163339 163341 163342 163343 163345 163346 163347 163349 163351 163355 163357 163361 163363 163367 163373 163375 163381 163385 163387 163391 163397 163403 163405 163411 163415 163417 163423 163427 163433 163441 203614
 实验室制备1,2-二溴乙烷的原理:
实验室制备1,2-二溴乙烷的原理:CH3CH2OH $→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O
CH2=CH2+Br2→BrCH2CH2Br
可能存在的主要副反应有:乙醇在浓硫酸的存在下在l40℃脱水生成乙醚.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示,有关数据列表如下:
有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm -3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(2)装置C中应加入c,吸收反应中产生的某些有影响的杂质气体(填写正确选项前的字母)
a.水 b.浓硫酸 c.NaOH溶液 d.KMnO4溶液
(3)装置B中竖直的长导管起安全管的作用,其原理是当B中的压强过大时,安全管中液面上升,从而调节B中气压相对稳定.
(4)若产物中有少量Br2,最好用d洗涤除去(填写正确选项前的字母)
a.水 b.乙醇 c.KI溶液 d.NaHSO3溶液
发生反应的化学方程为NaHSO3+Br2+H2O=NaHSO4+2HBr.
(5)若产物中有少量副产物乙醚,可用蒸馏的方法除去.
(6)反应过程中应用冷水冷却装置D,主要目的是乙烯与溴水反应放热,冷却可避免溴的大量挥发,但又不能过度冷却(如用冰水),其原因是1,2-二溴乙烷的熔点为9℃,过度冷却会使凝固而使气路堵塞.
 氮(N)、磷(P)、砷(As)等都是ⅤA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题:
氮(N)、磷(P)、砷(As)等都是ⅤA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题: .
. ,ZX与水反应放出的气体的化学式为H2.
,ZX与水反应放出的气体的化学式为H2.