题目内容
1. 氮(N)、磷(P)、砷(As)等都是ⅤA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题:
氮(N)、磷(P)、砷(As)等都是ⅤA族的元素,该族元素的化合物在研究和生产中有许多重要用途.回答下列问题:(1)化合物N2H4的电子式为
 .
.(2)As原子的核外电子排布式为1s22s22p63s23p63d104s24p3.
(3)P和S是同一周期的两种元素,P的第一电离能比S大,原因是P的p亚层是半充满状态,比较稳定,所以第一电离能比硫的大.
(4)NH4+中H-N-H的健角比NH3中H-N-H的键角大,原因是NH4+中的氮原子上均为成键电子,而NH3分子中的氮原子上有一对孤对电子,孤对电子和成键电子之间的排斥力强于成键电子和成键电子之间的排斥力.
(5)Na3AsO4中含有的化学键类型包括离子键、共价键;AsO43-空间构型为正四面体,As4O6的分子结构如图1所示,则在该化合物中As的杂化方式是sp3.
(6)白磷(P4)的晶体属于分子晶体,其晶胞结构如图2(小圆圈表示白磷分子).己知晶胞的边长为acm,阿伏加德罗常数为NAmol-1,则该晶胞中含有的P原子的个数为16,该晶体的密度为$\frac{496}{{a}^{3}{N}_{A}}$ g•cm-3(用含NA、a的式子表示).
分析 (1)化合物N2H4为共价化合物,含有N-N、N-H键;
(2)As原子核外电子数为33,根据能量最低原理书写核外电子排布式;
(3)P的3p亚层是半充满状态,比较稳定,第一电离能高于同周期相邻元素的;
(4)NH4+中的氮原子上均为成键电子,而NH3分子中的氮原子上有一对孤对电子,孤对电子和成键电子之间的排斥力强于成键电子和成键电子之间的排斥力;
(5)Na3AsO4属于离子化合物,酸根离子中含有共价键;AsO43-中As原子孤电子对数=$\frac{5+3-2×4}{2}$=0、价层电子对数为4+0=4,据此判断空间构型;As4O6的分子中As原子形成3个As-O键,含有1对孤对电子,杂化轨道数目为4;
(6)根据均摊法可知,晶胞中P4分子数目为4,则晶胞中含有16个P原子,计算晶胞质量,再根据ρ=$\frac{m}{V}$计算晶胞密度.
解答 解:(1)化合物N2H4为共价化合物,含有N-N、N-H键,电子式为 ,故答案为:
,故答案为: ;
;
(2)As原子核外电子数为33,根据能量最低原理,核外电子排布式为:1s22s22p63s23p63d104s24p3,
故答案为:1s22s22p63s23p63d104s24p3;
(3)P的3p亚层是半充满状态,比较稳定,第一电离能高于同周期相邻元素的,第一电离能大于硫的,
故答案为:P的p亚层是半充满状态,比较稳定,所以第一电离能比硫的大;
(4)NH4+中的氮原子上均为成键电子,而NH3分子中的氮原子上有一对孤对电子,孤对电子和成键电子之间的排斥力强于成键电子和成键电子之间的排斥力,故NH4+中H-N-H的键角比NH3中H-N-H的键角大,
故答案为:NH4+中的氮原子上均为成键电子,而NH3分子中的氮原子上有一对孤对电子,孤对电子和成键电子之间的排斥力强于成键电子和成键电子之间的排斥力;
(5)Na3AsO4属于离子化合物,含有离子键,酸根离子中含有共价键;AsO43-中As原子孤电子对数=$\frac{5+3-2×4}{2}$=0、价层电子对数为4+0=4,空间构型为正四面体;As4O6的分子中As原子形成3个As-O键,含有1对孤对电子,杂化轨道数目为4,杂化类型为sp3杂化,
故答案为:离子键、共价键;正四面体;sp3;
(6)根据均摊法可知,晶胞中P4分子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,则晶胞中P原子数目为4×4=16,晶胞质量为16×$\frac{31}{{N}_{A}}$g,晶胞体积为(a cm)3,则晶胞密度为$\frac{4×\frac{31}{{N}_{A}}g}{(acm)^{3}}$=$\frac{496}{{a}^{3}{N}_{A}}$g.cm-3,
故答案为:16;$\frac{496}{{a}^{3}{N}_{A}}$.
点评 本题是对物质结构与性质的考查,为高频考点,侧重考查学生的分析能力、计算能力,涉及核外电子排布、电离能、价层电子对互斥联立、杂化方式与空间构型判断、化学键、晶胞计算等,是对物质结构主干知识的考查,需要学生具备扎实的基础与灵活运用能力,难度中等,掌握均摊法进行有关晶胞计算.

 溶液的酸碱性可用酸度(AG)表示[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$],室温下,向浓度均为0.1mol/L体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,AG随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )
溶液的酸碱性可用酸度(AG)表示[AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$],室温下,向浓度均为0.1mol/L体积均为100mL的两种一元酸HX、HY的溶液中,分别加入NaOH固体,AG随加入NaOH的物质的量的变化如图所示.下列叙述正确的是( )| A. | HX、HY均为弱酸 | |
| B. | a点由水电离出的c(H+)=1.0×l0-13mol•L-l | |
| C. | c点溶液中:c(Y-)<c(Na+)<c(HY) | |
| D. | b点时,溶液的pH=7,酸碱恰好完全中和 |
| A. | 5 | B. | 6 | C. | 7 | D. | 8 |
Ⅰ.某研究小组将纯净的SO2气体通入0.5mol•L-1的Ba(NO3)2溶液中,得到了BaSO4沉淀.为探究上述溶液中何种微粒能氧化通入的SO2,该小组提出了如下假设:
假设一:溶液中的NO3-
假设二:溶液中溶解的O2
(1)验证假设一:
①请在下表空白处填写相关实验现象
| 实 验 步 骤 | 实验现象 | 结论 |
| 实验1:在盛有不含O2的10mL 0.5mol/L BaCl2溶液的烧杯中,缓慢通入纯净的SO2气体. | 无现象 | 假设一成立 |
| 实验2:在盛有不含O2的10mL 0.5mol/L Ba(NO3)2溶液的烧杯中,缓慢通入纯净的SO2气体. | 白色沉淀生成 |
(2)为深入研究该反应,该小组还测得上述两个实验中溶液的pH随通入SO2体积的变化曲线如图甲.实验2中溶液pH小于实验1的原因是(用离子方程式表示)3SO2+2NO3-+2H2O=3SO42-+2NO↑+4H+.
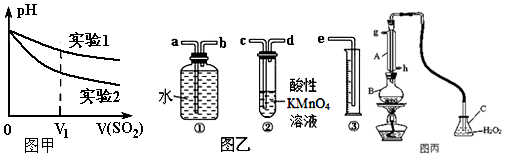
Ⅱ.我国规定空气中SO2含量不得超过0.02mg/L.某化学兴趣小组选用图乙实验装置,测定工业原料气(含SO2、N2、O2)中SO2的含量.
(1)若原料气从左向右流,上述装置连接的顺序是:原料气→c→d→b→a→e(用字母和箭头表示).当装置②中出现溶液紫(或紫红)色褪去现象时,立即停止通气.
(2)你认为以下试剂中,可以用来代替试管中的酸性高锰酸钾溶液的是B.
A.NaOH溶液 B.溴水C.氨水 D.BaCl2溶液
Ⅲ.中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g/L.某兴趣小组用图丙装置(夹持装置略)收集某葡萄酒中SO2,并对含量定性测定.
(1)B中加入250.00ml葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,除去C中过量的H2O2,然后用0.0600mol/LNaOH标准溶液进行滴定,滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为0.192g/L.
(2)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施盐酸易挥发,用不挥发的强酸例如硫酸代替盐酸,或用蒸馏水代替葡萄酒进行对比实验,排除盐酸挥发的影响.
 电解质溶液的电导率越大,导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度 均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温 Ksp[(CH3)2NH•H2O3=1.6×l04),利用传感器测得滴定过程中溶液的电导率如图所示》下列说法正确的是( )
电解质溶液的电导率越大,导电能力越强.常温下用0.100mol•L-1盐酸分别滴定10.00mL浓度 均为0.100mol•L-1的NaOH溶液和二甲胺[(CH3)2NH]溶液(二甲胺在水中电离与氨相似,常温 Ksp[(CH3)2NH•H2O3=1.6×l04),利用传感器测得滴定过程中溶液的电导率如图所示》下列说法正确的是( )| A. | b、c、d三点的溶液中水的电离程度:b<d<c | |
| B. | a 点溶液中:c(Na+)=2c(OH-)-2c(H+) | |
| C. | d 点溶液中:c[(CH3)2NH2+]+c(H+)-(OH-)=0.100mol•L-1 | |
| D. | e 点溶液中:c(H+)>c[(CH3)2NH2+]+2c[(CH3)2NH•H2O] |
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |

 ;F含有的官能团名称是羧基、羟基.
;F含有的官能团名称是羧基、羟基. .
. 或
或 .
.
 属及贵金属.从阳极泥中提取Se 的流程如下:
属及贵金属.从阳极泥中提取Se 的流程如下: