16.下列有关溶液中离子存在和转化的表达合理的是( )
| A. | Fe(OH)3溶于氢碘酸:Fe(OH)3+3H+=Fe3++3H2O | |
| B. | 由水电离出的c(OH-)=1×10-12mol/L的溶液中可能大量存在K+、I-、Mg2+、NO3- | |
| C. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液使SO42-完全沉淀:NH4++Al3++2SO42-+2Ba2++4OH-=NH3•H2O+Al(OH)3↓+2BaSO4↓ | |
| D. | 标准状况下,将1.12LCO2气体通入1L0.1mol/L的KAlO2溶液中:CO2+2H2O+AlO2-=Al(OH)3↓+HCO3- |
15.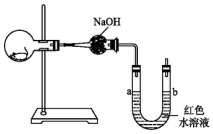 如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )
如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )
 如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )
如图所示,烧瓶内有一只活的小白鼠,U形管内装有红色水溶液,使a、b两端的液面处于同一水平面.经数小时后,U形管a、b两处的液面会出现下列哪种情况(实验装置足以维持实验期间小白鼠的生命活动,瓶口密封,忽略水蒸气和温度变化对实验结果的影响)( )| A. | a端下降,b端上升 | B. | a端上升,b端下降 | C. | a、b两端都下降 | D. | a、b两端都上升 |
12.常见无机物A、B、C、D存在如图转化关系(部分产物已略去),下列说法错误的是( )

| A. | 若B、D是空气的主要成分,则A可能用做制冷剂 | |
| B. | 若A、B、C的水溶液均显碱性,焰色反应均为黄色,则C可能用做胃酸中和剂 | |
| C. | 若D为生产生活中用量最大、用途最广泛的金属单质,则B可能为Fe( NO3)2 | |
| D. | 若B具有两性,则D可能为NaOH溶液或盐酸 |
11.下列条件下,两瓶气体所含的原子数一定相等的是( )
①同质量不同密度的CO和N2②同温同体积的H2和Cl2
③同温同压同体积的N2和O2④同压同体积的N2O和CO2.
①同质量不同密度的CO和N2②同温同体积的H2和Cl2
③同温同压同体积的N2和O2④同压同体积的N2O和CO2.
| A. | ①③ | B. | ①② | C. | ②④ | D. | ③④ |
10.合成高分子材料因有优良的性能而大受欢迎,因此高分子材料合成是化学工业中的最重要产业.与一般金属材料相比,其优点是( )
| A. | 硬度高,热稳定性强 | B. | 耐热性好,耐磨性强 | ||
| C. | 导电性强,延展性好 | D. | 强度大,电绝缘性好 |
9.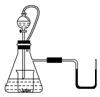 如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
 如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )
如图所示,若锥形瓶内是水,分液漏斗内的液体也是水,向烧杯内滴加水时,发现U形管内液体慢慢右移,恢复到原温度后液面左边与右边基本相平,则下列说法正确的是( )| A. | U型管内液体慢慢向右移动说明将分液漏斗中的水滴入到烧杯中一定发生了化学反应 | |
| B. | U型管内液体慢慢向右移动是由于锥形瓶中气体的总物质的量增大造成压强增大而引起 | |
| C. | 该装置中连接分液漏斗和锥形瓶的橡胶管对于上述实验现象而言其实是可有可无的 | |
| D. | 小烧杯中的物质可以是NaOH也可以是Na2O |
8.工业上曾经通过反应“3Fe+4NaOH $\stackrel{1100℃}{?}$Fe3O4+2H2↑+4Na↑”生产金属钠,己知铁的熔点1535℃、沸点3000℃.下列有关说法正确的是( )
| A. | 每生成1mol H2,转移的电子数约为4NA | |
| B. | 增大铁的量可以使反应速率加快 | |
| C. | 该反应条件下铁的金属性比钠强 | |
| D. | 将生成的气体在空气中冷却可获得钠 |
7.实验室测得4molSO2参加下述反应:已知2SO2(g)+O2(g)?2SO3(g);△H=-197kJ•mol-1,当放出314.3kJ热量时,SO2的转化率最接近于( )
0 163063 163071 163077 163081 163087 163089 163093 163099 163101 163107 163113 163117 163119 163123 163129 163131 163137 163141 163143 163147 163149 163153 163155 163157 163158 163159 163161 163162 163163 163165 163167 163171 163173 163177 163179 163183 163189 163191 163197 163201 163203 163207 163213 163219 163221 163227 163231 163233 163239 163243 163249 163257 203614
| A. | 40% | B. | 50% | C. | 80% | D. | 90% |
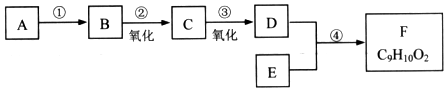
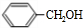 ;
;
 .
. .
.