14.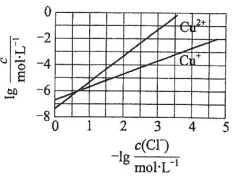 在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )
在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )
 在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )
在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )| A. | Ksp(CuCl)的数量级为10-7 | |
| B. | 除Cl-反应为Cu+Cu2++2Cl-=2CuCl | |
| C. | 加入Cu越多,Cu+浓度越高,除Cl-效果越好 | |
| D. | 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全 |
13. 全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )
 全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )
全固态锂硫电池能量密度高、成本低,其工作原理如图所示,其中电极a常用掺有石墨烯的S8材料,电池反应为:16Li+xS8=8Li2Sx(2≤x≤8).下列说法错误的是( )| A. | 电池工作时,正极可发生反应:2Li2S6+2Li++2e-=3Li2S4 | |
| B. | 电池工作时,外电路中流过0.02 mol电子,负极材料减重0.14 g | |
| C. | 石墨烯的作用主要是提高电极a的导电性 | |
| D. | 电池充电时间越长,电池中的Li2S2量越多 |
12.NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 0.1 mol 的11B中,含有0.6NA个中子 | |
| B. | pH=1的H3PO4溶液中,含有0.1NA个H+ | |
| C. | 2.24L(标准状况)苯在O2中完全燃烧,得到0.6NA个CO2分子 | |
| D. | 密闭容器中1 mol PCl3与1 mol Cl2反应制备 PCl5(g),增加2NA个P-Cl键 |
11.化学与生活密切相关.下列说法错误的是( )
| A. | PM2.5是指粒径不大于2.5μm的可吸入悬浮颗粒物 | |
| B. | 绿色化学要求从源头上消除或减少生产活动对环境的污染 | |
| C. | 燃煤中加入CaO可以减少酸雨的形成及温室气体的排放 | |
| D. | 天然气和液化石油气是我国目前推广使用的清洁燃料 |
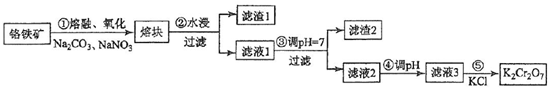
10.TiCl4是由钛精矿(主要成分为TiO2)制备钛(Ti)的重要中间产物,制备纯TiCl4的流程示意图如下:

资料:TiCl4及所含杂质氯化物的性质
(1)氯化过程:TiO2与Cl2难以直接反应,加碳生成CO和CO2可使反应得以进行.
已知:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)△H1=+175.4kJ•mol-1
2C(s)+O2(g)=2CO(g)△H2=-220.9kJ•mol-1
①沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g)△H=-45.5kJ•mol-1.
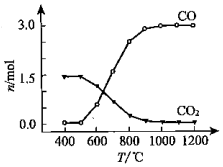
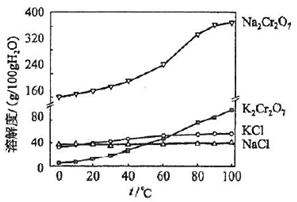
②氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的△H>0(填“>”“<”或“=”),判断依据:温度越高,CO的物质的量越多而CO2的物质的量少,说明CO2生成CO的反应是吸热反应.
③氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是饱和食盐水、氯化亚铁溶液.
④氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有TiO2、C.
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4.示意图如下:
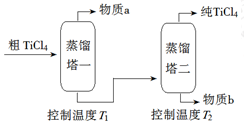
物质a是SiCl4,T2应控制在136℃左右.

资料:TiCl4及所含杂质氯化物的性质
| 化合物 | SiCl4 | TiCl4 | AlCl3 | FeCl3 | MgCl2 |
| 沸点/℃ | 58 | 136 | 181(升华) | 316 | 1412 |
| 熔点/℃ | -69 | 25 | 193 | 304 | 714 |
| 在TiCl4中的溶解性 | 互溶 | - | 微溶 | 难溶 | |
已知:TiO2(s)+2Cl2(g)=TiCl4(g)+O2(g)△H1=+175.4kJ•mol-1
2C(s)+O2(g)=2CO(g)△H2=-220.9kJ•mol-1
①沸腾炉中加碳氯化生成TiCl4(g)和CO(g)的热化学方程式:TiO2(s)+2Cl2(g)+2C(s)=TiCl4(g)+2CO(g)△H=-45.5kJ•mol-1.
②氯化过程中CO和CO2可以相互转化,根据如图判断:CO2生成CO反应的△H>0(填“>”“<”或“=”),判断依据:温度越高,CO的物质的量越多而CO2的物质的量少,说明CO2生成CO的反应是吸热反应.

③氯化反应的尾气须处理后排放,尾气中的HCl和Cl2经吸收可得粗盐酸、FeCl3溶液,则尾气的吸收液依次是饱和食盐水、氯化亚铁溶液.
④氯化产物冷却至室温,经过滤得到粗TiCl4混合液,则滤渣中含有TiO2、C.
(2)精制过程:粗TiCl4经两步蒸馏得纯TiCl4.示意图如下:

物质a是SiCl4,T2应控制在136℃左右.
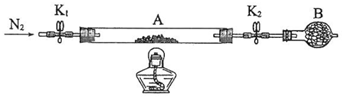
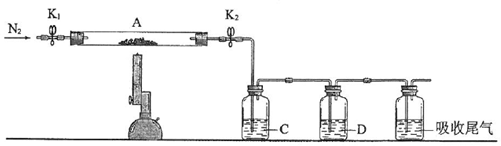
8.下述实验中均有红棕色气体产生,对比分析所的结论不正确的是( )
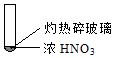 | 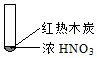 | 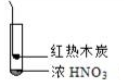 |
| ① | ② | ③ |
| A. | 由①中的红棕色气体,推断产生的气体一定是混合气体 | |
| B. | 红棕色气体不能表明②中木炭与浓硝酸产生了反应 | |
| C. | 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物 | |
| D. | ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应 |
7.聚维酮碘的水溶液是一种常见的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如下 (图中虚线表示氢键)
(图中虚线表示氢键)
下列说法不正确的是( )
0 162991 162999 163005 163009 163015 163017 163021 163027 163029 163035 163041 163045 163047 163051 163057 163059 163065 163069 163071 163075 163077 163081 163083 163085 163086 163087 163089 163090 163091 163093 163095 163099 163101 163105 163107 163111 163117 163119 163125 163129 163131 163135 163141 163147 163149 163155 163159 163161 163167 163171 163177 163185 203614
 (图中虚线表示氢键)
(图中虚线表示氢键)下列说法不正确的是( )
| A. | 聚维酮的单体是 | |
| B. | 聚维酮分子由(m+n)个单体聚合而成 | |
| C. | 聚维酮碘是一种水溶性物质 | |
| D. | 聚维酮在一定条件下能发生水解反应 |


 .B中所含的官能团是硝基.
.B中所含的官能团是硝基. 和
和 .
.