12.下列各有机物的名称肯定错误的是( )
| A. | 3-甲基-2-戊烯 | B. | 2-甲基-3-丁醇 | ||
| C. | 3,3,4-三甲基庚烷 | D. | 2,4,6-三硝基甲苯 |
11.红色物质甲在空气中加热生成黑色物质乙,甲也能溶于浓硝酸放出红色气体丙,并得到溶质为丁的蓝色溶液.下列推断中正确的是( )
| A. | 甲为铁锈 | B. | 乙为FeO | C. | 丙为NO2 | D. | 丁为CuCl2 |
10.有机化学在日常生活应用广泛,下列有关说法不正确的是( )
| A. | 相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大 | |
| B. | 煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 | |
| C. | 甲苯和Cl2光照下的反应与乙醇和乙酸反应属于同一类型的反应 | |
| D. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
9.苯是一种重要的有机化工原料,广泛用于合成橡胶、塑料和医药等方面.下列关于苯的叙述正确的是( )
| A. | 分子式为C6H6 | B. | 属于不饱和烃 | C. | 能在空气中燃烧 | D. | 无色无毒的液体 |
7.现有8种元素的性质、数据如下表所列,它们属于第二或第三周期.
回答下列问题:
(1)③的元素符号是Li;⑧的元素名称是硼;①在元素周期表中的位置是(周期、族)第二周期第VIA族;其氢化物的电子式是: .
.
(2)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3.
(3)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
| 编号 元素 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
(1)③的元素符号是Li;⑧的元素名称是硼;①在元素周期表中的位置是(周期、族)第二周期第VIA族;其氢化物的电子式是:
 .
.(2)比较④和⑦的氢化物的稳定性(用化学式表示)NH3>PH3.
(3)写出⑦的最高价氧化物对应水化物跟它的氢化物反应的化学方程式:NH3+HNO3=NH4NO3.
6.下列变化属于放热反应的是( )
①碳与二氧化碳化合 ②生石灰与水反应生成熟石灰 ③Zn与稀硫酸反应
④浓硫酸溶于水 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥甲烷与氧气的燃烧.
①碳与二氧化碳化合 ②生石灰与水反应生成熟石灰 ③Zn与稀硫酸反应
④浓硫酸溶于水 ⑤Ba(OH)2•8H2O与NH4Cl反应 ⑥甲烷与氧气的燃烧.
| A. | ①②④⑥ | B. | ①④⑤ | C. | ②③⑥ | D. | ②④⑥ |
4.碳与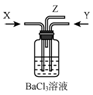 浓硫酸共热产生的气体X和铜和浓硝酸反应产生的气体Y间时通入盛有足量氯化钡溶液的气瓶中(如图装置),下列有关说法不正确的是( )
浓硫酸共热产生的气体X和铜和浓硝酸反应产生的气体Y间时通入盛有足量氯化钡溶液的气瓶中(如图装置),下列有关说法不正确的是( )
 浓硫酸共热产生的气体X和铜和浓硝酸反应产生的气体Y间时通入盛有足量氯化钡溶液的气瓶中(如图装置),下列有关说法不正确的是( )
浓硫酸共热产生的气体X和铜和浓硝酸反应产生的气体Y间时通入盛有足量氯化钡溶液的气瓶中(如图装置),下列有关说法不正确的是( )| A. | 洗气瓶中产生的沉淀是碳酸钡 | B. | 洗气瓶中产生的沉淀是亚硫酸钡 | ||
| C. | 洗气瓶中有氧化还原反应发生 | D. | 在Z导管口有红棕色气体出现 |
3.下列有关叙述中正确的是( )
0 162791 162799 162805 162809 162815 162817 162821 162827 162829 162835 162841 162845 162847 162851 162857 162859 162865 162869 162871 162875 162877 162881 162883 162885 162886 162887 162889 162890 162891 162893 162895 162899 162901 162905 162907 162911 162917 162919 162925 162929 162931 162935 162941 162947 162949 162955 162959 162961 162967 162971 162977 162985 203614
| A. | 在提纯鸡蛋中的蛋白质时,可向鸡蛋清溶液中加入浓硝酸,然后将所得沉淀滤出,即得较纯的蛋白质 | |
| B. | 可用过滤的方法除去四氯化碳中的I2 | |
| C. | 苯和溴苯的混合物可用分液漏斗分液分离 | |
| D. | 乙酸乙酯中混有乙酸,可用饱和Na2CO3溶液洗涤,然后分液分离出乙酸乙酯 |
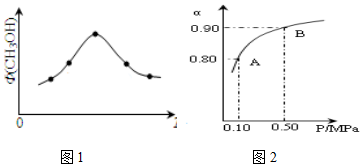 科学家为实现“低碳”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为:
科学家为实现“低碳”构想,把空气中的CO2转化为可再生能源甲醇(CH3OH).该反应的热化学方程式为:
 .
.