题目内容
10.有机化学在日常生活应用广泛,下列有关说法不正确的是( )| A. | 相同条件下,正丁烷、新戊烷、异戊烷的沸点依次增大 | |
| B. | 煤可与水蒸气反应制成水煤气,水煤气的主要成分为CO和H2 | |
| C. | 甲苯和Cl2光照下的反应与乙醇和乙酸反应属于同一类型的反应 | |
| D. | 苯与甲苯互为同系物,均能使KMnO4酸性溶液褪色 |
分析 A.由于烷烃的沸点随碳原子数的增多而升高,碳数相同时,支链越多,沸点越低;
B.水煤气主要成分为CO和H2,可由碳和水在高温下反应生成;
C.甲苯与氯气发生取代反应,乙酸、乙醇发生酯化反应,也为取代反应;
D.苯性质稳定,与高锰酸钾不反应.
解答 解:A.由于烷烃的沸点随碳原子数的增多而升高,碳数相同时,支链越多,沸点越低,正丁烷有4个碳原子,新戊烷、异戊烷都有5个碳原子,新戊烷支链多余异戊烷,所以沸点正丁烷<新戊烷<异戊烷,故A正确;
B.水煤气主要成分为CO和H2,可由碳和水在高温下反应生成,故B正确;
C.甲苯与氯气发生取代反应,乙酸、乙醇发生酯化反应生成乙酸乙酯,也为取代反应,二者反应类型相同,故C正确;
D.苯性质稳定,与高锰酸钾不反应,甲苯可被高锰酸钾氧化生成苯甲酸,故D错误.
故选D.
点评 本题考查有机物的结构与性质,为高频考点,侧重考查学生的分析能力,把握常见有机物的结构、官能团、性质及反应类型为解答的关键,题目难度不大.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
1.R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法正确的是(m、n 均为正整数)( )
| A. | 离子半径:Rn+>Zm- | |
| B. | 若Y的最高价氧化物对应的水化物HnY0m为强酸,则X的氢化物沸点一定比Y的氢化物的沸点低 | |
| C. | 若X的气态氢化物能使湿润的石蕊试纸变蓝,则标准状况下,18g Y的氢化物的体积为2.24 L | |
| D. | 若R(OH)n为弱电解质,则W(OH)n+1可与KOH溶液反应 |
18.下列说法正确的( )
| A. | 含有共价键的化合物一定是共价化合物 | |
| B. | 分子中只有共价键的化合物一定是共价化合物 | |
| C. | 离子化合物中只能含离子键 | |
| D. | 只有非金属原子间才能形成共价键 |
15.下列离子方程式正确的是( )
| A. | Cl2与NaOH溶液反应:Cl2+2OH-═Cl-+ClO-+H2O | |
| B. | F2与NaOH溶液反应:F2+4OH-═2F-+O2+2H2O | |
| C. | AgNO3溶液中加入少量氨水:Ag++2NH3•H2O═Ag(NH3)2++2H2O | |
| D. | Fe3O4与稀HNO3反应:Fe3O4+8H+═Fe2++2Fe3++4H2O |
2.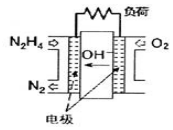 肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
 肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )
肼(N2H4)-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液.下列说法中,不正确的是( )| A. | 该电池放电时,通入肼的一极为负极 | |
| B. | 电池每释放1mol N2转移的电子数为4NA | |
| C. | 通入空气的一极的电极反应式是:O2+4e-+4H+=2H2O | |
| D. | 电池工作一段时间后,电解质溶液的pH将减小 |
19.某元素的原子最外层有2个电子,则这种元素是( )
| A. | 金属元素 | B. | 惰性气体元素 | C. | 第二主族元素 | D. | 以上叙述都可能 |
20.对下列选项中的操作和现象,其解释与结论完全正确的是( )
| 选项 | 操作 | 现象 | 解释与结论 |
| A | 室温下,向浓度均为0.1mol•L-1的KCl和KI混合溶液中滴加AgNO3溶液 | 出现黄色沉淀 | Ksp(AgCl)<Ksp(AgI) |
| B | 无水乙醇与浓硫酸共热至170℃,将产生的气体通入溴水 | 溴水褪色 | 乙烯和溴水发生加成反应 |
| C | 向物质的量浓度、体积均相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞 | 变红,前者红色更深 | 水解程度:CO32->HCO3- |
| D | 将Fe(NO3)2样品溶于稀H2SO4,滴加KSCN溶液 | 溶液变红 | 原Fe(NO3)2样品溶于酸前已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
 .
.