1.R、W、X、Y、Z为原子序数依次递增的同一短周期元素,下列说法正确的是(m、n 均为正整数)( )
| A. | 离子半径:Rn+>Zm- | |
| B. | 若Y的最高价氧化物对应的水化物HnY0m为强酸,则X的氢化物沸点一定比Y的氢化物的沸点低 | |
| C. | 若X的气态氢化物能使湿润的石蕊试纸变蓝,则标准状况下,18g Y的氢化物的体积为2.24 L | |
| D. | 若R(OH)n为弱电解质,则W(OH)n+1可与KOH溶液反应 |
3.表是部分短周期元素的原子半径及主要化合价,根据表中信息,判断以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径/nm | 0.160 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +2 | +3 | +2 | +6、-2 | -2 |
| A. | 氢化物的稳定性为H2T<H2R | |
| B. | M与T形成的化合物既能与强酸反应又能与强碱反应 | |
| C. | L2+与R2-的核外电子数相等 | |
| D. | 单质分别与浓度相等的稀盐酸反应的速率为Q>L |
2.下列所列各物质的用途中,不正确的是( )
| A. | 硅酸:粘合剂、耐火材料 | B. | 硅胶:干燥剂、吸附剂、催化剂载体 | ||
| C. | 碳化硅:砂纸、砂轮 | D. | 分子筛:吸附剂、催化剂 |
1.下面是某同学完成的探究实验报告的一部分:
实验名称:卤素单质的氧化性强弱比较
实验药品:KBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸.
实验设计如下
下列有关该实验的说法不正确的是( )
实验名称:卤素单质的氧化性强弱比较
实验药品:KBr溶液、KI溶液、氯水、溴水、碘水、四氯化碳、淀粉碘化钾试纸.
实验设计如下
| 实验步骤 | 实验结论 |
| ①氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | 氧化性从强到弱的顺序:氯、溴、碘 |
| ②NaBr溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 | |
| ③KI溶液+氯水+1 mL CCl4,振荡,静置,观察四氯化碳层颜色 |
| A. | 完成该实验需用到的实验仪器有试管和胶头滴管 | |
| B. | CCl4在实验中所起的作用是萃取剂 | |
| C. | ③中反应的离子方程式为Cl2+2I-═2Cl-+I2 | |
| D. | 上述三步实验能很好的探究卤素单质的氧化性强弱 |
20.下列各项中表达正确的是( )
| A. | H、D、T表示同一种核素 | B. | F-离子结构示意图  | ||
| C. | 次氯酸电子式  | D. | 用电子式表示HCl形成过程  |
19.下列离子方程式错误的是( )
| A. | 硅酸钠溶液中通入CO2气体:SiO32-+H2O+CO2═H2SiO3↓+CO32- | |
| B. | 氯气与氢氧化钾溶液反应:Cl2+OH-═Cl-+ClO-+2H2O | |
| C. | 硫酸铝与氨水反应:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ | |
| D. | 小苏打溶液与稀盐酸反应:HCO3-+H+═H2O+CO2↑ |
18.化学与生产、生活密切相关.下列有关叙述正确的是( )
0 162788 162796 162802 162806 162812 162814 162818 162824 162826 162832 162838 162842 162844 162848 162854 162856 162862 162866 162868 162872 162874 162878 162880 162882 162883 162884 162886 162887 162888 162890 162892 162896 162898 162902 162904 162908 162914 162916 162922 162926 162928 162932 162938 162944 162946 162952 162956 162958 162964 162968 162974 162982 203614
| A. | 大气雾霾污染现象的产生与汽车尾气排放有关 | |
| B. | 玻璃和氮化硅陶瓷都属于新型无机非金属材料 | |
| C. | 活性炭与二氧化硫都可用于漂白,其漂白原理相同 | |
| D. | 空气中的臭氧对人体健康有益无害 |
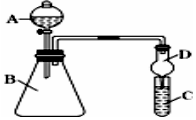 某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.
某同学为探究元素周期表中元素性质的递变规律,设计了如下系列实验.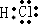 ,X2Y的结构式
,X2Y的结构式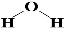 .
.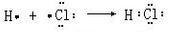 .
.