13.有四种短周期的主族元素X、Y、Z、W.X的一种原子常用于鉴定文物的年代,Y是地壳中含量最多的金属元素,W的原子核外某两层电子数目之比为4:3,X和Z同族.下列说法中正确的是( )
| A. | 简单离子半径:Y>W | |
| B. | 上述四种元素的单质中只有2种能导电 | |
| C. | X与Z两者的最高价氧化物的组成和结构相似 | |
| D. | 在加热条件下,Y的单质可溶于W的最高价含氧酸的浓溶液中 |
12.有机物X的结构简式为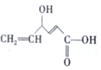 ,下列关于X的说法正确的是( )
,下列关于X的说法正确的是( )
 ,下列关于X的说法正确的是( )
,下列关于X的说法正确的是( )| A. | X中有4种官能团 | |
| B. | X的分子式为C6H5O3 | |
| C. | X可发生氧化、取代、加成反应 | |
| D. | 1molX与足量钠反应可生成11.2L气体(标准状况) |
10.以炼锌烟尘(主要成份为ZnO,含少量CuO和FeO)为原料,可以制取氧化锌和金属锌.
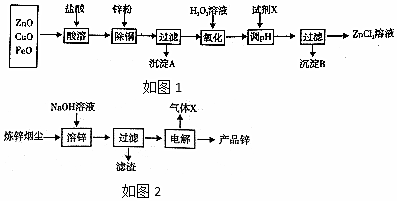
Ⅰ.制取氧化锌主要工艺如图1:
表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算).
(1)为了加快反应,“酸溶”需要适当加热,但温度不宜太高,原因是减少盐酸挥发.
(2)加入H2O2溶液发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)流程图中,为了降低溶液的酸度,调节pH范围为3.2≤PH<5.2;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为3Zn2(OH)2CO3+4Fe3++3H2O=4Fe(OH)3↓+6Zn2++3CO2↑.
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为4.0×10-5.从ZnCl2溶液中提取无水ZnCl2的方法是在氯化氢气体,蒸干氯化锌溶液并加热至失去结晶水.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O═Na2[Zn(OH)4](aq),然后电解浸取液.
(5)如图2,炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
(6)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
Ⅰ.制取氧化锌主要工艺如图1:

表列出了相关金属离子生成氢氧化物沉淀的pH(开始沉淀的pH按金属离子浓度为l.0mol/L计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Zn2+ | 5.2 | 6.4 |
| Fe2+ | 5.8 | 8.8 |
(2)加入H2O2溶液发生反应的离子方程式2Fe2++H2O2+2H+=2Fe3++2H2O.
(3)流程图中,为了降低溶液的酸度,调节pH范围为3.2≤PH<5.2;若试剂X为Zn2(OH)2CO3,加入X除杂质的离子方程式为3Zn2(OH)2CO3+4Fe3++3H2O=4Fe(OH)3↓+6Zn2++3CO2↑.
(4)已知,室温下,Ksp[Fe(OH)3]=4.0×10-38,当pH=3时,溶液中c(Fe3+)为4.0×10-5.从ZnCl2溶液中提取无水ZnCl2的方法是在氯化氢气体,蒸干氯化锌溶液并加热至失去结晶水.
Ⅱ.制取金属锌采用碱溶解ZnO(s)+2NaOH (aq)+H2O═Na2[Zn(OH)4](aq),然后电解浸取液.
(5)如图2,炼锌烟尘采用碱溶,而不采用酸溶后电解,主要原因是氧化铜、氧化亚铁不溶于碱溶液中.
(6)以石墨作电极电解时,阳极产生的气体为O2;阴极的电极反应为[Zn(OH)4]2-+2e-=Zn+4OH-.
9.下列有关100mL 0.1mol•L-1 (NH4)2Fe(SO4)2溶液的叙述正确的是( )
| A. | 与K+、Na+、AlO2-、CO32-可以大量共存 | |
| B. | 可用铁氰化钾溶液检验该溶液是否变质 | |
| C. | 与100mL 0.1mol/L Ba(OH)2反应的离子方程式:Ba2++2OH-+SO42-+2NH4+═BaSO4↓+2NH3•H2O | |
| D. | 与足量酸性KMnO4溶液混合充分反应,共转移电子0.01mol |
8.漂粉精的有效成分是( )
| A. | Ca(ClO)2 | B. | CaCl2 | C. | CaCO3 | D. | Ca(OH)2 |
7.下列说法正确的是( )
| A. | 反应2H2(g)+O2(g)═2H2O(l) 在室温下可自发进行,则该反应的△H<0 | |
| B. | 常温常压下,7.8gNa2O2与水完全反应,产生1.12L气体 | |
| C. | 煤的干馏是物理变化,石油的裂化是化学变化 | |
| D. | 气体分子总数不再改变时,反应H2(g)+I2(g)?2HI(g))达到平衡 |
6.下列指定反应的离子方程式正确的是( )
| A. | 向碳酸钠溶液中加入过量醋酸:CO32-+2H+═H2O+CO2↑ | |
| B. | 向偏铝酸钠溶掖中通入过量二氧化碳;CO2+2H2O+AlO2-═Al(OH)3↓+HCO3- | |
| C. | 向莫尔盐[(NH4)2Fe(SO4)2•6H2O]溶液中加入过量氧氧化钠溶液:NH4++Fe2++3OH-═NH3•H2O+Fe(OH)2↓ | |
| D. | 向双氧水中加入酸性高锰酸钾溶液:5H2O2+2MnO4-═2Mn2++5O2↑+6OH-+2H2O |
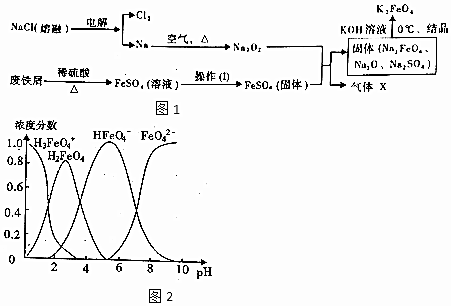
4.阅读下列信息:
Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
A、B、C均为上表中的元素;
Ⅱ.A与B可形成化合物AB、AB2,二者可用于制备强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3,二者可用于制备强酸乙.
请回答:
(1)该表中两种元素的氢化物所含电子数不同,这两种氢化物之间能发生反应,写出符合要求的化学方程式NH3+HCl=NH4Cl等(有多组符合,写出任意一个即可).
(2)元素②氢化物的沸点高于元素⑤氢化物的沸点,原因是水分子之间存在氢.
(3)甲、乙分别与氨反应生成丙、丁、戊三种盐.0.1mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式)H2SO4、NH4HSO4、HNO3、(NH4)2SO4、NH4NO3.
(4)很稀的甲溶液与Zn反应,当反应的甲与Zn的物质的量之比为5:2时,还原产物可能为(填写化学式)NH4NO3、N2O.
0 162729 162737 162743 162747 162753 162755 162759 162765 162767 162773 162779 162783 162785 162789 162795 162797 162803 162807 162809 162813 162815 162819 162821 162823 162824 162825 162827 162828 162829 162831 162833 162837 162839 162843 162845 162849 162855 162857 162863 162867 162869 162873 162879 162885 162887 162893 162897 162899 162905 162909 162915 162923 203614
Ⅰ.表中①~⑥为短周期元素主要化合价及最简单氢化物沸点的数据:
| 元素性质 | 元素编号 | |||||
| ① | ② | ③ | ④ | ⑤ | ⑥ | |
| 氢化物沸点(℃) | -33.4 | 100 | 19.54 | -87.7 | -60.7 | -84.9 |
| 主要化合价 | +5 -3 | -2 | -1 | +5 -3 | +6 -2 | +7 -1 |
Ⅱ.A与B可形成化合物AB、AB2,二者可用于制备强酸甲;
Ⅲ.C与B可形成化合物CB2、CB3,二者可用于制备强酸乙.
请回答:
(1)该表中两种元素的氢化物所含电子数不同,这两种氢化物之间能发生反应,写出符合要求的化学方程式NH3+HCl=NH4Cl等(有多组符合,写出任意一个即可).
(2)元素②氢化物的沸点高于元素⑤氢化物的沸点,原因是水分子之间存在氢.
(3)甲、乙分别与氨反应生成丙、丁、戊三种盐.0.1mol/L的甲、乙、丙、丁、戊五种溶液,pH由小到大排列的顺序是(填写化学式)H2SO4、NH4HSO4、HNO3、(NH4)2SO4、NH4NO3.
(4)很稀的甲溶液与Zn反应,当反应的甲与Zn的物质的量之比为5:2时,还原产物可能为(填写化学式)NH4NO3、N2O.
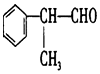 ,该物质是一种香料.
,该物质是一种香料.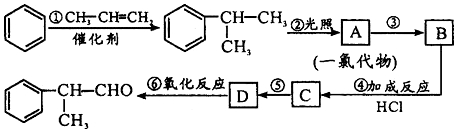
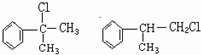 ;
; ;⑥2
;⑥2 +O2$→_{△}^{催化剂}$2
+O2$→_{△}^{催化剂}$2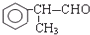 +2H2O.
+2H2O.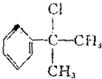 的水解产物
的水解产物 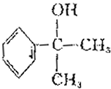 中的-OH不在链端,不能氧化成-CHO.
中的-OH不在链端,不能氧化成-CHO.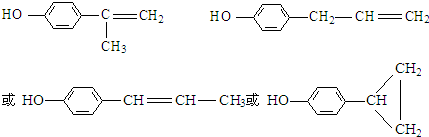 .
.