2.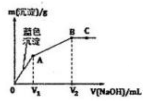 向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
 向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )
向含MgCl2和CuCl2的溶液中逐滴加入0.1 mol•L-1的NaOH溶液,沉淀的质量(m)与加入NaOH溶液体积(V)的关系如图所示,已知V2=3V1,下列说法正确的是( )| A. | 水的电离程度:A>B>C | |
| B. | 该实验不能证明Cu(OH)2的Ksp比Mg(OH)2的Ksp小 | |
| C. | 原溶液中MgCl2和CuCl2的物质的量浓度相等 | |
| D. | 若向Mg(OH)2悬浊液中加入CuCl2溶液,一定会有Cu(OH)2生成 |
1.化学与生产、生活、环境等密切相关.下列叙述正确的是( )
| A. | 加强化石燃料的开采利用,能从根本上解决能源危机 | |
| B. | 苹果放在空气中久置变黄和纸张在空气中久置变黄原理相似 | |
| C. | 从海水中提取物质,都必须经过化学反应才能实现 | |
| D. | 焙制糕点的发酵粉主要成分之一是碳酸氢纳,它也是治疗胃酸过多的一种药剂 |
20.表是元素周期表的一部分,针对表中的①-⑧八种元素,用元素符号或化学式回答相关问题:
(l)在这些元素中,化学性质最不活泼原子的原子结构示意图为 .
.
(2)用电子式表示①与③形成化合物的过程 .
.
(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O.
(4)①②③④四种元素的简单离子半径由大到小的顺序是F->Na+>Mg2+>Al3+.(用离子符号和“>”表示).
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是Br2>Cl2>F2.(用化学式和“>”表示).
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | |||||||
| 三 | ② | ③ | ④ | ⑤ | ⑥ | |||
| 四 | ⑦ | ⑧ |
 .
.(2)用电子式表示①与③形成化合物的过程
 .
.(3)这些元素的最高价氧化物对应的水化物中,酸性最强的是HClO4,②、④的最高价氧化物对应水化物的溶液反应的离子方程式为:Al(OH)3+OH-=AlO2-+2H2O.
(4)①②③④四种元素的简单离子半径由大到小的顺序是F->Na+>Mg2+>Al3+.(用离子符号和“>”表示).
(5)①⑤⑧三种元素的单质沸点由高到低的顺序是Br2>Cl2>F2.(用化学式和“>”表示).
19. 亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:
亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:
①2NO+Na2O2═2NaNO2
②2NO2+Na2O2═2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-被还原成Mn2+.
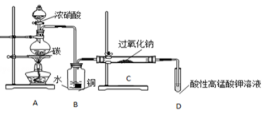
Ⅰ.产品制备与检验:用如图装置制备NaNO2
(1)写出装置A烧瓶中发生反应的化学方程式C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B装置的作用是将NO2转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO);盛浓硝酸的仪器名称为分液漏斗.
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净的NaNO2,应在B、C装置间增加一个干燥管.在干燥管中盛放的试剂名称为碱石灰.
(4)请设计实验,检验装置C中NaNO2的存在(写出操作、现象和结论)取少量装置C中产物置于试管中,加入适量蒸馏水溶解,滴加少量酸性KMnO4溶液,若溶液紫色褪去,说明C中产物含有NaNO2.
Ⅱ.含量的测定
称取装置C中反应后的固体4.00g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如表所示:
(5)第一组实验数据出现异常,造成这种异常的原因可能是A、C.
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
D.滴定结束后俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%或0.8625.
 亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:
亚硝酸钠(NaNO2)是一种常见的食品添加剂,使用时必须严格控制其用量.某兴趣小组进行下面实验探究,查阅资料知道:①2NO+Na2O2═2NaNO2
②2NO2+Na2O2═2NaNO3
③酸性KMnO4溶液可将NO2-氧化为NO3-,MnO4-被还原成Mn2+.
Ⅰ.产品制备与检验:用如图装置制备NaNO2
(1)写出装置A烧瓶中发生反应的化学方程式C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O.
(2)B装置的作用是将NO2转化为NO,同时Cu与稀硝酸反应生成NO(或制取NO);盛浓硝酸的仪器名称为分液漏斗.
(3)有同学认为装置C中产物不仅有亚硝酸钠,还有碳酸钠和氢氧化钠,为制备纯净的NaNO2,应在B、C装置间增加一个干燥管.在干燥管中盛放的试剂名称为碱石灰.
(4)请设计实验,检验装置C中NaNO2的存在(写出操作、现象和结论)取少量装置C中产物置于试管中,加入适量蒸馏水溶解,滴加少量酸性KMnO4溶液,若溶液紫色褪去,说明C中产物含有NaNO2.
Ⅱ.含量的测定
称取装置C中反应后的固体4.00g溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用0.1000mol/L酸性KMnO4溶液进行滴定,实验所得数据如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| KMnO4溶液体积/mL | 20.60 | 20.02 | 20.00 | 19.98 |
A.酸式滴定管用蒸馏水洗净后未用标准液润洗
B.锥形瓶洗净后未干燥
C.滴定结束后仰视读数
D.滴定结束后俯视读数
(6)根据表中数据,计算所得固体中亚硝酸钠的质量分数86.25%或0.8625.
17.一定质量的甲烷燃烧后的产物为CO、CO2和水蒸气,此混合气体质量为99.2g,当其缓慢经过无水CaCl2时,CaCl2增重50.4g.原混合气体中CO2的质量为( )
| A. | 13.2 g | B. | 22.4g | C. | 24.4g | D. | 26.4g |
16.现有反应 3Fe(s)+4H2O(g)$\stackrel{△}{?}$ Fe3O4(s)+4H2(g),在一体积可调的密闭容器中进行,采取下列措施对其反应速率几乎无影响的是( )
| A. | 增加H2的量 | |
| B. | 将容器体积缩小一半 | |
| C. | 保持容器内体积不变,充入Ar使体系压强增大 | |
| D. | 充入Ar,保持容器内压强不变 |
15.下列说法中,错误的是( )
| A. | 相同质量的乙烯和甲烷完全燃烧后产生的水的质量相同 | |
| B. | 用溴的四氯化碳溶液或酸性KMnO4溶液都可以鉴别乙烯和乙烷 | |
| C. | 无论乙烯与Br2的加成,还是乙烯使酸性KMnO4溶液褪色,都与分子内含有碳碳双键有关 | |
| D. | 乙烯的化学性质比乙烷的化学性质活泼 |
14.古代的很多成语、谚语都蕴含着很多科学知识,下列对成语、谚语的解释正确的是( )
| A. | “冰,水为之,而寒于水”说明相同质量和温度的水和冰,冰的能量高 | |
| B. | “玉不琢不成器”,“百炼方能成钢”发生的均为化学变化 | |
| C. | “爆竹声中除旧岁,春风送暖入屠苏”爆竹爆炸发生的是分解反应 | |
| D. | “火树银花”中的焰火实质上是金属元素的焰色反应 |
13.900℃时,向2.0L恒容密闭容器中充入0.40mol乙苯,发生反应:
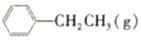 ?
?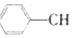 =CH2(g)+H2(g)
=CH2(g)+H2(g)
经一段时间后达到平衡,反应过程中测定的部分数据如表所示:
下列说法正确的是( )
0 162502 162510 162516 162520 162526 162528 162532 162538 162540 162546 162552 162556 162558 162562 162568 162570 162576 162580 162582 162586 162588 162592 162594 162596 162597 162598 162600 162601 162602 162604 162606 162610 162612 162616 162618 162622 162628 162630 162636 162640 162642 162646 162652 162658 162660 162666 162670 162672 162678 162682 162688 162696 203614
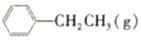 ?
? =CH2(g)+H2(g)
=CH2(g)+H2(g)经一段时间后达到平衡,反应过程中测定的部分数据如表所示:
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(乙苯)/mol | 0.40 | 0.30 | 0.24 | n2 | n3 |
| n(苯乙烯)/mol | 0.00 | 0.10 | n1 | 0.20 | 0.20 |
| A. | 保持其他条件不变,向容器中充入不参与反应的水蒸气作为稀释剂,则乙苯的转化率大于50.0% | |
| B. | 反应在前20分钟的平均速率为v(H2)=0.008molmol/( L•min) | |
| C. | 若混合气体的平均摩尔质量不再变化,则说明反应已达到平衡状态 | |
| D. | 相同温度下,起始时向容器中充入0.10mol乙苯、0.10mol苯乙烯和0.30molH2,达到平衡前v正>v逆 |
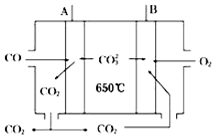 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.