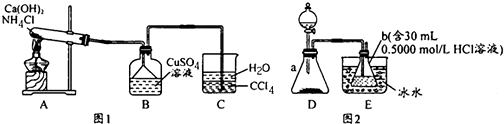
6.在100℃时,将0.200mol的四氧化二氮气体充入2L真空的密闭容器中,每隔一定的时间对该容器内的物质进行分析,得到如下表格:
试填空:
(1)该反应的化学方程式为N2O4?2 NO2,
达到平衡时,四氧化二氮的转化率为60%,表中c2>c3、a=b(填“>”、“<”或“=”).
(2)20s时四氧化二氮的浓度c1=0.07mol/L,40s时二氧化氮的浓度c2=0.1mol/L,在0s~20s时间段内,二氧化氮的平均反应速率为v(NO2)=0.003mol/(L•s),四氧化二氮的平均反应速率为v(N2O4)=0.0015mol/(L•s)
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是0.2mol/L.
 | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
(1)该反应的化学方程式为N2O4?2 NO2,
达到平衡时,四氧化二氮的转化率为60%,表中c2>c3、a=b(填“>”、“<”或“=”).
(2)20s时四氧化二氮的浓度c1=0.07mol/L,40s时二氧化氮的浓度c2=0.1mol/L,在0s~20s时间段内,二氧化氮的平均反应速率为v(NO2)=0.003mol/(L•s),四氧化二氮的平均反应速率为v(N2O4)=0.0015mol/(L•s)
(3)若在相同情况下最初向该容器充入的是二氧化氮气体,要达到上述同样的平衡状态,二氧化氮的起始浓度是0.2mol/L.
5.煤的气化过程中发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),若在恒温压容器中充入1mol CO和3mol 水蒸气发生上述反应,达到平衡时测得反应物
与生成物的物质的量之比为5:3,且吸收热量180kJ,请回答下列问题:
(1)该反应的热化学方程式可写为CO(g)+H2O=CO2(g)+H2(g)△=+240kJ/mol.
(2)两种反应物的转化率之和为1.
(3)该条件下此反应的平衡常数为1.
(4)若要在相同的温度下和相同的容器中,按下列物料配比充入,建立平衡后CO的体积百分含量与题干平衡相同,下列选项中可行的是ABC.
(5)若要在相同的温度下和相同的容器中,充入下列物料建立平衡,平衡后CO2的体积分数与题干平衡的CO2的体积分数相同,但CO的体积分数与题干平衡中CO的体积分数不同的是BC.
与生成物的物质的量之比为5:3,且吸收热量180kJ,请回答下列问题:
(1)该反应的热化学方程式可写为CO(g)+H2O=CO2(g)+H2(g)△=+240kJ/mol.
(2)两种反应物的转化率之和为1.
(3)该条件下此反应的平衡常数为1.
(4)若要在相同的温度下和相同的容器中,按下列物料配比充入,建立平衡后CO的体积百分含量与题干平衡相同,下列选项中可行的是ABC.
| 物质 选项 | n(CO) | n(H2O) | n(CO2) | n(H2) |
| A | 0mol | 4mol | 2mol | 2mol |
| B | 0.5mol | 2.5mol | 0.5mol | 0.5mol |
| C | 1mol | 4mol | 0.5mol | 0.5mol |
| D | 0mol | 0mol | 1mol | 3mol |
| 物质 选项 | n(CO) | n(H2O) | n(CO2) | n(H2) |
| A | 0mol | 0mol | 1mol | 3mol |
| B | 2.5mol | 0.5mol | 0.5mol | 0.5mol |
| C | 3mol | 1mol | 0mol | 0mol |
| D | 0mol | 0mol | 3mol | 1mol |
4. 工业合成氨反应为:N2(g)+3H2(g) $?_{高温高压}^{催化剂}$ 2NH3(g),对其研究如下:
工业合成氨反应为:N2(g)+3H2(g) $?_{高温高压}^{催化剂}$ 2NH3(g),对其研究如下:
(1)已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,N≡N键的键能是945.6kJ•mol-1,则上述反应的△H=-92.46kJ•mol-1.
(2)上述反应的平衡常数K的表达式为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.若反应方程式改写为:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g),在该温度下的平衡常数:K1=$\sqrt{K}$(用K表示).
(3)在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
①该温度下,若向同容积的另一容器中投入的N2、H2、NH3浓度分别为3mol/L,3mol/L、3mol/L,此时v正大于v逆(填“大于”、“小于”或“等于”)
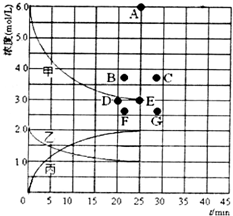
②由上述表中的实验数据计算得到“浓度~时间”的关系可用如图的曲线表示,表示 c(N2)~t的曲线是乙.在此温度下,若起始充入4molN2和12molH2,反应刚达到平衡时,表示c(H2)的曲线上相应的点为B.
0 162252 162260 162266 162270 162276 162278 162282 162288 162290 162296 162302 162306 162308 162312 162318 162320 162326 162330 162332 162336 162338 162342 162344 162346 162347 162348 162350 162351 162352 162354 162356 162360 162362 162366 162368 162372 162378 162380 162386 162390 162392 162396 162402 162408 162410 162416 162420 162422 162428 162432 162438 162446 203614
 工业合成氨反应为:N2(g)+3H2(g) $?_{高温高压}^{催化剂}$ 2NH3(g),对其研究如下:
工业合成氨反应为:N2(g)+3H2(g) $?_{高温高压}^{催化剂}$ 2NH3(g),对其研究如下:(1)已知H-H键能为436kJ•mol-1,N-H键能为391kJ•mol-1,N≡N键的键能是945.6kJ•mol-1,则上述反应的△H=-92.46kJ•mol-1.
(2)上述反应的平衡常数K的表达式为:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$.若反应方程式改写为:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g),在该温度下的平衡常数:K1=$\sqrt{K}$(用K表示).
(3)在773K时,分别将2molN2和6molH2充入一个固定容积为1L的密闭容器中,随着反应的进行,气体混合物中n(H2)、n(NH3)与反应时间t的关系如下表:
| t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
| n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
| n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
②由上述表中的实验数据计算得到“浓度~时间”的关系可用如图的曲线表示,表示 c(N2)~t的曲线是乙.在此温度下,若起始充入4molN2和12molH2,反应刚达到平衡时,表示c(H2)的曲线上相应的点为B.
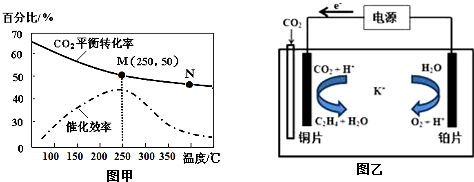

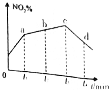 研究氧化物与悬浮在大气中的海盐粒子的相互作用时,设计如下反应:
研究氧化物与悬浮在大气中的海盐粒子的相互作用时,设计如下反应: