题目内容
8.蕴藏在海底的“可燃冰”是高压下形成的外观像冰的甲烷水合物固体.根据你所学的知识回答下列问题:(1)碳元素在周期表中的位置是第二周期ⅣA族,甲烷是其简单气态氢化物,与水比较不稳定的是甲烷(或CH4);已知1g甲烷完全燃烧生成液态水时放热55.6kJ•mol-1,写出该反应的热化学方程式CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6kJ•mol-1.
(2)碳有多种同素异形体,C60所属的晶体类型为分子晶体;金刚石熔化时破坏的作用力是共价键;
金刚石、石墨的能量关系如图所示,则等质量的金刚石和石墨完全燃烧金刚石(填“金刚石”或“石墨”)放出热量更多,写出石墨转化为金刚石的热化学方程式C(s,石墨)=C(s,金刚石)△H=+1.9kJ•mol-1.

(3)工业上常利用甲烷制氢气,反应方程式为:CH4(g)+H2O(g)?CO(g)+3H2(g)△H=+160kJ•mol-1;现向容积为2L的密闭容器中分别通入2mol的甲烷和水蒸气,4s时测得氢气的反应速率为0.3mol•L-1.s-1,则4s时剩余的甲烷的浓度为0.6mol/L,反应吸收(填“放出”或“吸收”)热量;上述反应可以通过电解池来实现,电解液为硫酸钠溶液,电解过程能量的转化形式为电能转化为化学能.
分析 (1)根据碳原子的电子层数、最外层电子数确定碳元素在周期表中的位置;非金属性越强,气态氢化物越稳定;计算1mol甲烷完全燃烧生成液态水时放热量,热化学方程式中化学计量数代表物质的量;
(2)C60由分子构成,金刚石为原子构成的原子晶体,只含共价键;由图可知,等物质的量时,金刚石的能量比石墨的高;
(3)容积为2L的密闭容器中分别通入2mol的甲烷和水蒸气,4s时测得氢气的反应速率为0.3mol•L-1.s-1,可知生成氢气为0.3mol•L-1.s-1×4s=1.2mol/L,由反应可知转化的甲烷为1.2mol/L×$\frac{1}{3}$=0.4mol/L,焓变为正;电解时电能转化为化学能,以此来解答.
解答 解:(1)C是两个电子层,最外层4个电子,所以在元素周期表中的位置为第二周期ⅣA族;
非金属性越强,气态氢化物越稳定,非金属性O>C,所以气态氢化物的稳定性CH4<H2O;
1g甲烷完全燃烧生成液态水时放热55.6kJ•mol-1,由物质的量与热量成正比、焓变为负,可知热化学方程式为CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6 kJ•mol-1,
故答案为:第二周期ⅣA族;甲烷(或CH4);CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-889.6 kJ•mol-1;
(2)C60由分子构成,C60所属的晶体类型为分子晶体;金刚石熔化时破坏的作用力是共价键;由金刚石、石墨的能量关系图可知,等物质的量时,金刚石的能量比石墨的高,则等质量的金刚石和石墨完全燃烧,产物相同,金刚石放出热量更多,石墨转化为金刚石的热化学方程式为C(s,石墨)=C(s,金刚石)△H=(-110.5kJ/mol-283kJ/mol)-(-395.4kJ/mol)=+1.9 kJ•mol-1,
故答案为:分子晶体;共价键;金刚石; C(s,石墨)=C(s,金刚石)△H=+1.9 kJ•mol-1;
(3)容积为2L的密闭容器中分别通入2mol的甲烷和水蒸气,4s时测得氢气的反应速率为0.3mol•L-1.s-1,可知生成氢气为0.3mol•L-1.s-1×4s=1.2mol/L,由反应可知转化的甲烷为1.2mol/L×$\frac{1}{3}$=0.4mol/L,4s时剩余的甲烷的浓度为1mol/L-0.4mol/L=0.6mol/L;焓变为正,该反应发生时吸收能量;电解时电能转化为化学能,
故答案为:0.6mol•L-1,吸收; 电能转化为化学能.
点评 本题考查化学平衡计算及反应热计算,为高频考点,把握图中能量变化、反应中能量变化、化学平衡计算为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.

 中考解读考点精练系列答案
中考解读考点精练系列答案 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案| A. | 用丁达尔效应可区分胶体和溶液 | |
| B. | 煤可经分馏获得洁净的燃料 | |
| C. | 非金属材料中不可以含有金属元素 | |
| D. | 电解氯化镁饱和溶液,可制得金属镁 |
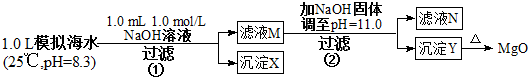
| 海水中的离子浓度(mol/L) | Na+ | Mg2+ | Ca2+ | Cl- | HCO3 |
| 0.439 | 0.050 | 0.011 | 0.560 | 0.001 |
实验过程中,假设溶液体积不变.
已知:Ksp(CaCO3)=4.96×10-9;Ksp(MgCO3)=6.82×10-6;
Ksp[Ca(OH)2]=4.68×10-6;Ksp[Mg(OH)2]=5.61×10-12.
下列说法正确的是( )
| A. | 沉淀物X为CaCO3,MgCO3 | |
| B. | 滤液M中存在Mg2+,不存在Ca2+ | |
| C. | 滤液N中存在Mg2+、Ca2+ | |
| D. | 步骤②中若改为加入8 g NaOH固体,沉淀物Y为Ca(OH)2和Mg(OH)2的混合物 |
| A. | 甲烷的燃烧热△H=-890.3kJ/mol,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O(g)△H=-890.3 kJ/mol | |
| B. | 一定条件下,将0.5 mol N2和1.5 molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)?2NH3(g)△H=-38.6 kJ/mol | |
| C. | 在101kPa时,2gH2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol | |
| D. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ba(OH)2反应的反应热△H=2×(-57.3)kJ/mol |
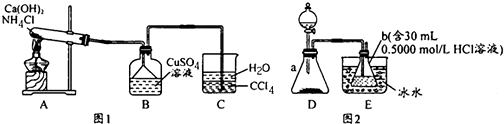
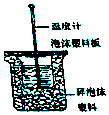 Ⅰ.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题.
Ⅰ.50mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题.(1)从实验装置上看,图中尚缺少的一种玻璃用品是环形玻璃搅拌棒.
(2)烧杯间填满碎纸条的作用是减少实验过程中的热量损失.
(3)实验中改用60mL0.50mol/L盐酸与50mL0.55mol/LNaOH溶液进行反应,与上述实验相比较,所放出的热量不相等(填“相等”或“不相等”),但中和热应相等(填“相等”或“不相等”).
(4)记录的实验数据如表:
| 实验用品 | 溶液温度 | |||
| t1 | t2 | |||
| ① | 50ml0.55mol/LNaOH | 50ml0.5mol/LHCl | 20℃ | 23.3℃ |
| ② | 50ml0.55mol/LNaOH | 50ml0.5mol/LHCl | 20℃ | 23.5℃ |
| 50ml0.55mol/LNaOH | 50ml0.5mol/LHCl | 20℃ | 21.5℃ | |
过氧化氢是重要的氧化剂,也可作还原剂,它的水溶液称为双氧水,常用于消毒、杀菌、漂白等.某化学研究性学习小组取一定量的市售过氧化氢溶液测定其中H2O2的含量,并探究它的有关性质.
Ⅱ.测定市售过氧化氢溶液中H2O2的质量分数
(1)量取10.00mL密度为ρ g/mL的市售过氧化氢溶液,应选用酸式滴定管(填“酸式滴定管”或“碱式滴定管”);
(2)将上述溶液配制成250.00mL,配制过程需用到的玻璃仪器是烧杯、玻璃棒、250 mL容量瓶、胶头滴管(填名称);
(3)取25.00mL(2)中的溶液于锥形瓶中,用稀H2SO4酸化,并加适量蒸馏水稀释,用高锰酸钾标准液滴定.
①完成反应的离子方程式:
2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑
②重复滴定三次,平均消耗C mol/L KMnO4标准液V mL,则原过氧化氢溶液中H2O2的质量分数为$\frac{17CV}{200ρ}$.
 PbSO4+2H2O的说法正确的是
PbSO4+2H2O的说法正确的是