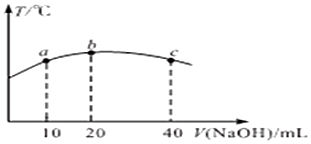
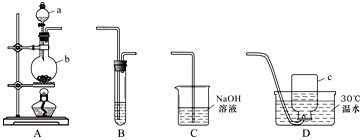
17.下列关于电解质溶液的叙述正确的是( )
| A. | 常温下电离常数为Ka的酸HA溶液中c(H+)$\sqrt{{K}_{a}}$mol•L-1 | |
| B. | 向0.1 mol•L-1的氨水中加入少量硫酸铵固体,则溶液中$\frac{c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$增大 | |
| C. | 0.2 mol•L-1CH3COOH溶液与0.1 mol•L-1NaOH溶液等体积混合:2c(H+)-2 c(OH-)═c(CH3COO-)-c(CH3COOH) | |
| D. | 将饱和Na2SO4溶液加入到饱和石灰水中,有白色沉淀产生,说明Ksp[Ca(OH)2]大于Ksp(CaSO4) |
15.室温条件下列溶液中离子浓度的等量关系正确的是( )
| A. | 0.1 mol/L氨水中:c(NH4+)+c(H+)═c(OH-) | |
| B. | 0.1 mol/L的NH4Cl溶液中:c(NH4+)═c(Cl-) | |
| C. | 同为0.1 mol/L的硫酸和氨水等体积混合后:c(NH4+)+c(NH3•H2O)═2c(SO42-) | |
| D. | pH=3的盐酸和pH=11的氨水等体积混合后:c(OH-)=c(H+) |
13.在CaCl2、MgI2、K2CO3、HClO、NaOH这几种物质中,含有共价键的离子化合物有( )
| A. | 1种 | B. | 3种 | C. | 2种 | D. | 4种 |
12.下列关于元素周期律的叙述中,正确的是( )
| A. | 随着元素原子序数的递增,原子最外层电子总是从1到8重复出现 | |
| B. | 随着元素原子序数的递增,元素最高正价从+1到+7、负价从-7到-1重复出现 | |
| C. | 随着元素原子序数的递增,原子半径从小到大(稀有气体除外)重复出现 | |
| D. | 随着元素原子序数的递增,元素的金属性逐渐减弱,非金属性逐渐增强重复出现 |
11.已知A2-离子共含有x个中子,A元素的质量数为m,则n克A2-离子共含有电子的物质的量为( )
| A. | $\frac{n(m-x)}{m}$ | B. | $\frac{n(m-x+2)}{m}$ | C. | $\frac{m-x+2}{m-x}$ | D. | $\frac{n(m-x-2)}{m}$ |
9.最近,科学家研制出一种纸质电池,这种“软电池”采用薄层纸片作为载体和传导体,在一边附着锌,在另一边附着二氧化锰.电池总反应式为Zn+2MnO2+H2O═ZnO+2MnO(OH).下列说法正确的是( )
| A. | 该电池中Zn为负极,发生还原反应 | |
| B. | 该电池的正极反应式为MnO2+e-+H2O=MnOOH+OH- | |
| C. | 导电时外电路电子由Zn流向MnO2,内电路电子由MnO2流向Zn | |
| D. | 电池工作时内电路中OH-移动向MnO2一极 |
8.某电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压.该电池是以K2FeO4和Zn为电极材料,KOH溶液为电解溶质溶液,其总反应为:3Zn+2K2FeO4+8H2O$?_{充电}^{放电}$3Zn(OH)2+2Fe(OH)3+4KOH,下列说法正确的是( )
0 162158 162166 162172 162176 162182 162184 162188 162194 162196 162202 162208 162212 162214 162218 162224 162226 162232 162236 162238 162242 162244 162248 162250 162252 162253 162254 162256 162257 162258 162260 162262 162266 162268 162272 162274 162278 162284 162286 162292 162296 162298 162302 162308 162314 162316 162322 162326 162328 162334 162338 162344 162352 203614
| A. | Zn为电池的正极 | |
| B. | 充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O | |
| C. | 放电时每转移3 mol电子,正极有1 mol K2FeO4被氧化 | |
| D. | 该电池放电过程中电解质溶液浓度不变 |