7.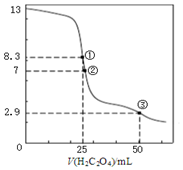 25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
 25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )| A. | 点①所示溶液中:c(H+)+2c(H2C2O4)+c(HC2O4-)=c(OH-) | |
| B. | 点②所示溶液中:c(HC2O4-)+2c(C2O42-)=0.0500mol•L-1 | |
| C. | 点③所示溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| D. | 滴定过程中可能出现:c(Na+)>c(C2O42-)=c(HC2O4-)>c(H+)>c(OH-) |
3.铁矿石(主要成份FeS)与一定浓度的HNO3反应,生成Fe(NO3)3、Fe2(SO4)3、NO2、N2O4、NO和H2O,当NO2、N2O4、NO的物质的量之比为4:1:4时,实际参加反应的FeS与HNO3的物质的量之比为( )
| A. | 16:25 | B. | 1:7 | C. | 1:6 | D. | 2:11 |
1. 科学家一直致力于“人工固氮”的方法研究.
科学家一直致力于“人工固氮”的方法研究.
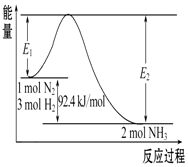
合成氨的原理为:N2(g)+3H2(g)?2NH3(g),该反应的能量变化如图所示.
(1)在反应体系中加入催化剂,反应速率增大,E2的变化是减小(填“增大”、“减小”或“不变”)
(2)该反应的反应热△H=-92.4KJ/mol,已知E2=212.4 kJ/mol,则该反应正反应的活化能是120KJ/mol
(3)该反应化学平衡常数的表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$该反应的化学平衡常数K和温度t的关系如表所示:
则K1>K2(填>、<、=)
(4)该反应的△S<0,(填大于、小于或等于),理论上在低温条件下可以自发.
0 162099 162107 162113 162117 162123 162125 162129 162135 162137 162143 162149 162153 162155 162159 162165 162167 162173 162177 162179 162183 162185 162189 162191 162193 162194 162195 162197 162198 162199 162201 162203 162207 162209 162213 162215 162219 162225 162227 162233 162237 162239 162243 162249 162255 162257 162263 162267 162269 162275 162279 162285 162293 203614
 科学家一直致力于“人工固氮”的方法研究.
科学家一直致力于“人工固氮”的方法研究.合成氨的原理为:N2(g)+3H2(g)?2NH3(g),该反应的能量变化如图所示.
(1)在反应体系中加入催化剂,反应速率增大,E2的变化是减小(填“增大”、“减小”或“不变”)
(2)该反应的反应热△H=-92.4KJ/mol,已知E2=212.4 kJ/mol,则该反应正反应的活化能是120KJ/mol
(3)该反应化学平衡常数的表达式:K=$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2}){c}^{3}({H}_{2})}$该反应的化学平衡常数K和温度t的关系如表所示:
| t℃ | 473 | 573 | 673 | … |
| K | 4.4×10-2 | K1 | K2 | … |
(4)该反应的△S<0,(填大于、小于或等于),理论上在低温条件下可以自发.
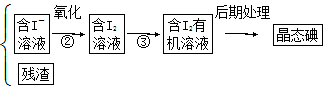
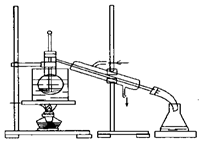
 某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对原子质量.
某化学兴趣小组用如图所示装置电解CuSO4溶液,测定铜的相对原子质量. ,请完成下列空白:
,请完成下列空白: Ⅰ红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题:
Ⅰ红磷P(s)和Cl2(g)发生反应生成PCl3(g)和PCl5(g).反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据).根据图回答下列问题: A元素最简单的氢化物的电子式为
A元素最简单的氢化物的电子式为 .
.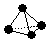 ,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.写出B4转化为B2的热化学方程式:N4(g)=2N2(g)△H=-882kJ•mol-1;
,已知断裂1mol B-B键吸收167kJ的热量,生成1mol B≡B键放出942kJ热量.写出B4转化为B2的热化学方程式:N4(g)=2N2(g)△H=-882kJ•mol-1;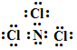 ;X遇水蒸气可形成一种常见的漂白性物质.则X与水反应的化学方程式是NCl3+3H2O=NH3↑+3HClO.
;X遇水蒸气可形成一种常见的漂白性物质.则X与水反应的化学方程式是NCl3+3H2O=NH3↑+3HClO.