题目内容
2.已知有机物A的结构简式为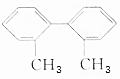 ,请完成下列空白:
,请完成下列空白:(1)有机物A的分子式是C14H14.
(2)有机物A分子中在同一平面上的碳原子至少有9个,最多有14个;
(3)有机物A的苯环上的一氯代物有4种.
分析 (1)由结构简式可知有机物分子式;
(2)由结构简式可知,分子中含2个苯环,苯环为平面结构,直接与苯环相连的原子与苯环在同一平面内,结合对称性分析;
(3)根据苯环上含有的等效氢原子数目进行判断其一氯代物种类.
解答 解:(1)有机物A的分子式是C14H14;
故答案为:C14H14;
(2)甲基与苯环平面结构通过单键相连,甲基的C原子处于苯的H原子位置,所以处于苯环这个平面;
两个苯环相连,与苯环相连的碳原子处于该苯环中的H原子位置,也处于另一个苯环这个平面,另一苯环所用的C原子都处于同一平面上,处于苯环对位上的碳原子以及碳原子所连的氢原子共线,所以至少有9个碳原子共面,至多有14个碳原子共面;
故答案为:9;14;
(3)有机物A的苯环上的一氯代物有4种: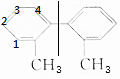 ,故答案为:4.
,故答案为:4.
点评 本题考查有机物的结构与性质,把握结构中共面问题及苯的结构为解答的关键,题目难度不大.

练习册系列答案
相关题目
7.下列解释事实的方程式不正确的是( )
| A. | 硫酸型酸雨的形成涉及反应:2H2SO3+O2$\frac{\underline{\;催化剂\;}}{\;}$2H2SO4 | |
| B. | SO2的水溶液显酸性:SO2+H2O?H2SO3?2H++SO32- | |
| C. | 常温下,0.1mol/L醋酸溶液pH≈3:CH3COOH?CH3COO-+H+ | |
| D. | Mg(OH)2固体在溶液中存在平衡:Mg(OH)2(s)?Mg2+(aq)+2OH-(aq),该固体可溶于NH4Cl溶液 |
13.下列说法正确的是(NA表示阿伏加德罗常数的值)( )
| A. | 常温常压下,44 g C3H8中含有的碳碳单键数为3NA | |
| B. | 标准状况下,22.4L 甲醇中含有的氧原子数为1NA | |
| C. | 1mol羟基中电子数为10NA | |
| D. | 在30 g甲醛和醋酸的混合物中,含有碳原子数为1NA |
7.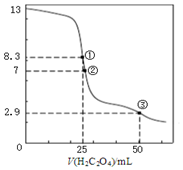 25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
 25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )
25℃时,用0.0500mol•L-1H2C2O4(二元弱酸)溶液滴定25.00mL0.1000mol•L-1NaOH溶液所得滴定曲线如图.下列说法不正确的是( )| A. | 点①所示溶液中:c(H+)+2c(H2C2O4)+c(HC2O4-)=c(OH-) | |
| B. | 点②所示溶液中:c(HC2O4-)+2c(C2O42-)=0.0500mol•L-1 | |
| C. | 点③所示溶液中:c(Na+)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | |
| D. | 滴定过程中可能出现:c(Na+)>c(C2O42-)=c(HC2O4-)>c(H+)>c(OH-) |
11.表是元素周期表的一部分,针对表中①~⑩中元素,用元素符号或化学式填空回答以下问题:
(1)在①~⑦元素中,原子半径最小的是F;原子半径最大的是K,其离子结构示意图为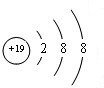
(2)①~⑩元素的最高价氧化物对就的水化物中酸性最强的是HClO4,碱性最强的是KOH;
(3)按要求写出下列两种物质的电子式:①的氢化物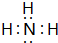 ;⑨的最高价氧化物对应的水化物
;⑨的最高价氧化物对应的水化物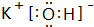 ;
;
(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用1个化学反应说明该事实(写出反应的化学方程式):Cl2+2KBr═2KCl+Br2.
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |

(2)①~⑩元素的最高价氧化物对就的水化物中酸性最强的是HClO4,碱性最强的是KOH;
(3)按要求写出下列两种物质的电子式:①的氢化物
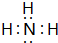 ;⑨的最高价氧化物对应的水化物
;⑨的最高价氧化物对应的水化物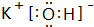 ;
;(4)在⑦与⑩的单质中,化学性质较活泼的是Cl2,可用1个化学反应说明该事实(写出反应的化学方程式):Cl2+2KBr═2KCl+Br2.
12.能说明醋酸是弱电解质的事实是( )
| A. | 醋酸溶液的导电性比盐酸弱 | |
| B. | 醋酸溶液与碳酸钙反应,缓慢放出二氧化碳 | |
| C. | 醋酸钠溶液呈一定的碱性 | |
| D. | 0.1mol/L的CH3COOH溶液中,氢离子浓度约为0.001mol/L |
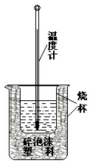 50ml 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题:
50ml 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如下图所示的装置中进行中和反应.通过测定反应过程中放出的热量可计算中和热.回答下列问题: