2.G是合成双酚A的原料,其结构简式如图,关于G说法不正确的是( )


| A. | 分子式为C6H10 | B. | 是乙烯的同系物 | ||
| C. | 可以发生加成反应 | D. | 难溶于水 |
20.下列过程对应的离子方程式正确的是( )
| A. | NaHSO3溶于水呈酸性:NaHSO3═Na++H++SO32- | |
| B. | 在Na2S2O3溶液中滴加稀硫酸:2H++S2O32-═SO2↑+S↓+H2O | |
| C. | 浓盐酸与MnO2反应制氯气:MnO2+4HCl═Mn2++2Cl2+2H2O | |
| D. | 工业冶炼Mg:2Mg2++2O2-$\frac{\underline{\;电解\;}}{\;}$2Mg+O2↑ |
18.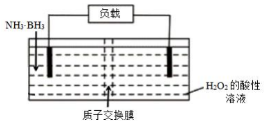 氨硼烷(NH3•BH3)电池可在常温下工作,装置如图.该电池工作时的总反应为:NH3•BH3+3H2O2═NH4BO2+4H2O. 下列说法正确的是( )
氨硼烷(NH3•BH3)电池可在常温下工作,装置如图.该电池工作时的总反应为:NH3•BH3+3H2O2═NH4BO2+4H2O. 下列说法正确的是( )
 氨硼烷(NH3•BH3)电池可在常温下工作,装置如图.该电池工作时的总反应为:NH3•BH3+3H2O2═NH4BO2+4H2O. 下列说法正确的是( )
氨硼烷(NH3•BH3)电池可在常温下工作,装置如图.该电池工作时的总反应为:NH3•BH3+3H2O2═NH4BO2+4H2O. 下列说法正确的是( )| A. | 电流从左侧电极经过负载后流向右侧电极 | |
| B. | BO2-通过质子交换膜向正极移动 | |
| C. | 负极附近溶液pH增大 | |
| D. | 正极的反应式为 3H2O2+6H++6e-═6H2O |
17.短周期主族元素 X、Y、Z、W的原子序数依次增大,X原子最外层电子比次外层多4个,Y、Z为相邻金属元素,Z的简单离子半径在同周期元素中最小,W与X同族. 下列说法不正确的是( )
| A. | 原子半径:Y>Z>W>X | |
| B. | 气态氢化物的热稳定性:X>W | |
| C. | 工业上常用电解对应氯化物的方法制备单质 Z | |
| D. | Y 的最高价氧化物对应的水化物可溶于氯化铵溶液 |
16.设 NA为阿伏加德罗常数的值. 下列说法正确的是( )
| A. | 标准状况下,11.2 L CHCl3 中含有的分子数为 0.5NA | |
| B. | 1mol H218O 中含有的中子数为 10NA | |
| C. | 46g C2H5OH 中含有的共价键数目为 7NA | |
| D. | 1L 1mol/L CH3COONa 溶液中含 CH3COO-的数目为 NA |
15.用下列装置进行的实验,能达到相应实验目的是( )
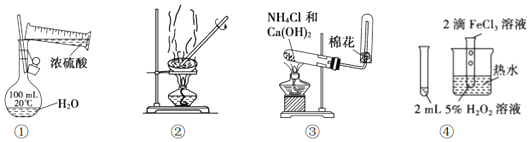

| A. | 用装置①配制一定浓度的硫酸溶液 | |
| B. | 用装置②分离溶解在CCl4中的 I2 | |
| C. | 用装置③制备和收集少量 NH3 | |
| D. | 用装置④验证FeCl3对 H2O2分解有催化作用 |
14.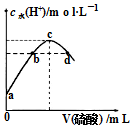 常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )
常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )
 常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )
常温下,向20mL0.1mol•L-1氨水中滴加某浓度的硫酸溶液,溶液中水电离的氢离子浓度随加入硫酸的体积变化如图.下列说法错误的是( )| A. | 若a等于1.0×10-11 mol•L-1,则此时氨水的电离度为1% | |
| B. | c点时氨水与硫酸恰好完全反应 | |
| C. | c点所示溶液中:c(H+)-c(OH-)═c(NH3•H2O) | |
| D. | 若b、d对应的水电离的氢离子浓度为1.0×10-7 mol•L-1,此时两溶液中都存在:c(NH4+)═2c(SO42-) |
13.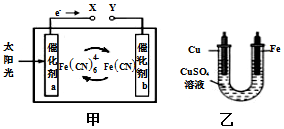 甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )
甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )
0 162091 162099 162105 162109 162115 162117 162121 162127 162129 162135 162141 162145 162147 162151 162157 162159 162165 162169 162171 162175 162177 162181 162183 162185 162186 162187 162189 162190 162191 162193 162195 162199 162201 162205 162207 162211 162217 162219 162225 162229 162231 162235 162241 162247 162249 162255 162259 162261 162267 162271 162277 162285 203614
 甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )
甲是一种太阳能电池的工作原理示意图,电解质为K3[Fe(CN)6]和K4[Fe(CN)6]的混合溶液,将甲装置和乙装置相连实现铁件上镀铜.下列说法正确的是( )| A. | 电池工作时,K+移向电极a | |
| B. | 电极b表面发生的电极反应Fe(CN)64--e-═Fe(CN)63- | |
| C. | Cu电极应与Y相连接,发生氧化反应 | |
| D. | 工作一段时间后,甲乙两装置中电解质溶液浓度均变小 |







