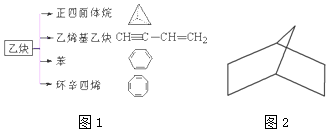
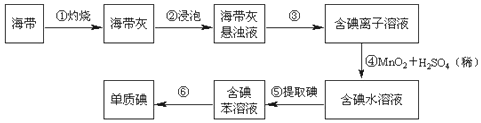
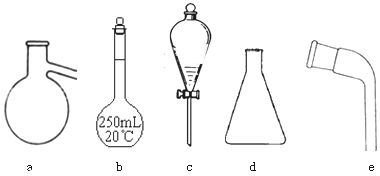
8.设NA表示阿伏加得德罗常数的数值,下列叙述中正确的是( )
| A. | 1 mol NH3所含有的原子数为NA | |
| B. | 常温常压下,22.4 L氧气所含的原子数为2NA | |
| C. | 常温常压下,48 g O3所含的氧原子数为3NA | |
| D. | 0.1 molNa+中所含的电子为1.1NA |
7.NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,NA个H2和O2的混合气体的体积约为22.4 L | |
| B. | 1mol SiO2晶体中,含有2NA个Si-O键 | |
| C. | 0.1 mol Cl2溶解于一定体积的水中,转移电子数为0.2NA | |
| D. | 标准状况下,11.2 L H2O所含分子数为0.5 NA |
6.硫酸铝、硫酸钾、明矾三种物质组成的混合物中,当SO42-的浓度为0.20mol•L-1时,加入等体积的0.20mol•L-1的KOH溶液(混合后溶液体积变化忽略不计),使生成的白色沉淀恰好溶解,那么最后混合物中K+的浓度是( )
| A. | 0.20 mol•L-1 | B. | 0.25 mol•L-1 | C. | 0.225 mol•L-1 | D. | 0.45 mol•L-1 |
5.下列各元素的性质或原子结构递变规律错误的是( )
| A. | Li、Be、B原子最外层电子数依次增多 | |
| B. | P、S、Cl元素的最高正价依次升高 | |
| C. | Li、Na、K的金属性依次减弱 | |
| D. | N、O、F原子半径依次增大 |
4.摩尔是( )
| A. | 计量微观粒子的物质的量的单位 | B. | 国际单位制的一个基本物理量 | ||
| C. | 表示物质质量的单位 | D. | 表示6.02×1023个粒子的集体 |
2.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 22.4LN2中共用电子对为3NA | |
| B. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为0.1NA | |
| C. | 常温常压下,分子总数为NA的NO2和CO2混合气体中含有氧原子数为2NA | |
| D. | 78g苯中含有C=C键数目为3NA |
1.从下列事实所得出的相应结论错误的是( )
0 161851 161859 161865 161869 161875 161877 161881 161887 161889 161895 161901 161905 161907 161911 161917 161919 161925 161929 161931 161935 161937 161941 161943 161945 161946 161947 161949 161950 161951 161953 161955 161959 161961 161965 161967 161971 161977 161979 161985 161989 161991 161995 162001 162007 162009 162015 162019 162021 162027 162031 162037 162045 203614
| 实验事实 | 结论 | |
| A | 向某溶液中滴入2滴KSCN溶液,溶液不显血红色.再向溶液中滴入几滴新制的氯水,溶液变为血红色 | 该溶液中一定含有Fe2+ |
| B | 将CO2通入到Na2SiO3溶液中产生白色浑浊 | 酸性:H2CO3>H2SiO3 |
| C | 已知反应5Cl2+I2+6H2O═2HIO3+10HCl,2BrO3-+Cl2═2ClO3-+Br2 | 氧化性强弱顺序:BrO3->Cl2>2ClO3->IO3- |
| D | 测定等物质的量浓度的Na2SO4与Na2CO3溶液的pH,后者较大 | 非金属性:S>C |
| A. | A | B. | B | C. | C | D. | D |