题目内容
2.用NA表示阿伏伽德罗常数的值,下列说法正确的是( )| A. | 22.4LN2中共用电子对为3NA | |
| B. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为0.1NA | |
| C. | 常温常压下,分子总数为NA的NO2和CO2混合气体中含有氧原子数为2NA | |
| D. | 78g苯中含有C=C键数目为3NA |
分析 A.气体状况未知;
B.溶液体积未知;
C.依据n=$\frac{N}{N{\;}_{A}}$计算物质的量,结合NO2和CO2混合气体中都含有2个氧原子计算;
D.苯分子中不含碳碳双键.
解答 解:A.气体状况未知,Vm未知,无法计算氮气的物质的量和所含共用电子对数,故A错误;
B.依据n=CV,可知溶液体积未知,无法计算氢氧根离子个数,故B错误;
C.依据n=$\frac{N}{N{\;}_{A}}$计算物质的量=1mol,结合NO2和CO2混合气体中都含有2个氧原子计算,混合气体中含有的氧原子数为2NA,故C正确;
D.苯分子中不含碳碳双键,故D错误;
故选:C.
点评 本题考查了阿伏伽德罗常数的分析应用,主要是质量换算物质的量计算微粒数,气体摩尔体积的条件应用,掌握基础是关键,注意苯中碳碳键是介于单键与双键之间一种独特的化学键,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,NA个H2和O2的混合气体的体积约为22.4 L | |
| B. | 1mol SiO2晶体中,含有2NA个Si-O键 | |
| C. | 0.1 mol Cl2溶解于一定体积的水中,转移电子数为0.2NA | |
| D. | 标准状况下,11.2 L H2O所含分子数为0.5 NA |
14.现有三组溶液:①汽油和四氯化碳混合溶液 ②植物油和水③氯化钠和单质溴的水溶液,分离以上各混合液的正确方法依次是( )
| A. | 分液、萃取、蒸馏 | B. | 萃取、蒸馏、分液 | C. | 分液、蒸馏、萃取 | D. | 蒸馏、分液、萃取 |
11.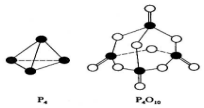 白磷与氧可发生如下反应:P4+5O2=P4O10.已知断裂下列化学键需要吸收的能量分别为:P-P akJ•mol-1、P-O bkJ•mol-1、P=O ckJ•mol-1、O=O dkJ•mol-1.根据图示的分子结构和有关数据估算生成1mol P4O10时,反应的能量变化正确的是( )
白磷与氧可发生如下反应:P4+5O2=P4O10.已知断裂下列化学键需要吸收的能量分别为:P-P akJ•mol-1、P-O bkJ•mol-1、P=O ckJ•mol-1、O=O dkJ•mol-1.根据图示的分子结构和有关数据估算生成1mol P4O10时,反应的能量变化正确的是( )
 白磷与氧可发生如下反应:P4+5O2=P4O10.已知断裂下列化学键需要吸收的能量分别为:P-P akJ•mol-1、P-O bkJ•mol-1、P=O ckJ•mol-1、O=O dkJ•mol-1.根据图示的分子结构和有关数据估算生成1mol P4O10时,反应的能量变化正确的是( )
白磷与氧可发生如下反应:P4+5O2=P4O10.已知断裂下列化学键需要吸收的能量分别为:P-P akJ•mol-1、P-O bkJ•mol-1、P=O ckJ•mol-1、O=O dkJ•mol-1.根据图示的分子结构和有关数据估算生成1mol P4O10时,反应的能量变化正确的是( )| A. | 吸收(6a+5d-4c-12b)kJ热量 | B. | 放出(4c+12b-6a-5d)kJ热量 | ||
| C. | 吸收(4c+12b-4a-5d)kJ热量 | D. | 放出(4a+5d-4c-12b)kJ热量 |
12.黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:S(s)+2KNO3(s)+3C(s)═K2S(s)+N2(g)+3CO2(g)△H=xkJ•mol-1
已知:①C(s)+O2(g)═CO2(g)△H1=akJ•mol-1
②K2S(s)═S(s)+2K(s)△H2=bkJ•mol-1
③2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=cJ•mol-1
下列说法正确的是( )
已知:①C(s)+O2(g)═CO2(g)△H1=akJ•mol-1
②K2S(s)═S(s)+2K(s)△H2=bkJ•mol-1
③2K(s)+N2(g)+3O2(g)═2KNO3(s)△H3=cJ•mol-1
下列说法正确的是( )
| A. | x>0 a<0 | |
| B. | b<o c<o | |
| C. | x=3a-b-c | |
| D. | 1mol碳(s)在空气中不完全燃烧生成CO的焓变小与akJ•mol-1 |