8.化学与生活是紧密相联的,下列说法正确的是( )
| A. | 为防止食品的氧化变质,常在食品包装袋中放入生石灰 | |
| B. | 节日里绚丽的烟花,是通过某些金属元素的化学变化实现的 | |
| C. | SO2具有漂白性,通常用于银耳等食品的漂白 | |
| D. | 干冰或碘化银可用于进行人工降雨 |
6.在密闭容器中,反应2NO2?N2O4在不同条件下的化学平衡情况如图a、图b所示.图a表示恒温条件下c(NO2)的变化情况;图b表示恒压条件下,平衡体系中N2O4的质量分数随温度的变化情况(实线上的任意一点为对应温度下的平衡状态).下列说法正确的是( )
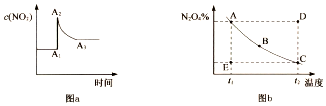

| A. | 其它条件不变时,向平衡体系中充入N2O4,平衡常数增大 | |
| B. | 图a中,A1一A2变化的原因一定是充人了NO2 | |
| C. | 图b中,E点对应状态中,v(正)>v(逆) | |
| D. | 图b中,E→A所需时间为x,D→C所需时间为y,则x<y |
5.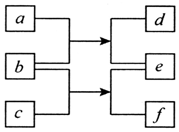 短周期元素W、X、Y、Z的原子序数依次增加,由上述元素组成的各物质转化关系如图所示.其中b为单质,其水溶液显酸性且具有漂白性;d为单质且具有同素异形体;常温下0.0l mol•L-1f溶液的pH<2.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加,由上述元素组成的各物质转化关系如图所示.其中b为单质,其水溶液显酸性且具有漂白性;d为单质且具有同素异形体;常温下0.0l mol•L-1f溶液的pH<2.下列说法正确的是( )
 短周期元素W、X、Y、Z的原子序数依次增加,由上述元素组成的各物质转化关系如图所示.其中b为单质,其水溶液显酸性且具有漂白性;d为单质且具有同素异形体;常温下0.0l mol•L-1f溶液的pH<2.下列说法正确的是( )
短周期元素W、X、Y、Z的原子序数依次增加,由上述元素组成的各物质转化关系如图所示.其中b为单质,其水溶液显酸性且具有漂白性;d为单质且具有同素异形体;常温下0.0l mol•L-1f溶液的pH<2.下列说法正确的是( )| A. | 原子半径的大小W<Y<Z | B. | 元素的非金属性Z>X>Y | ||
| C. | Y的氧化物一定为酸性氧化物 | D. | Z的含氧酸一定为强酸 |
3.某化学研究性学习小组模拟工业生产流程制备无水氯化铁并对产物做如下探究实验.
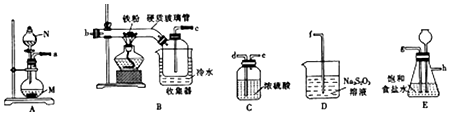
已知:①无水氯化铁在空气中易潮解,加热易升华;
②工业上,向500~600℃的铁屑中通人氯气可生产无水氯化铁;
③向炽热的铁屑中通入氯化氢可以生产无水氯化亚铁和氢气,
(1)仪器N的名称是分液漏斗,N中盛有浓盐酸,烧瓶M中的固体试剂KMnO4(或KClO3) (填化学式).
(2)装置的连接顺序为→a,→g→h→d→e→bc→d→e→f.(用小写字母表示,部分装置可以重复使用)
(3)若缺少装置E,则对本实验造成的影响是HCl和Fe反应生成的H2与Cl2混合受热发生爆炸,且有杂质氯化亚铁生成
(4)已知硫代硫酸钠(Na2S2O3)溶液在工业上可作脱氯剂,反应后Na2S2O3被氧化为Na2SO4,则装置D中
发生反应的离子方称式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
(5)实验结束并冷却后,将硬质玻璃管及收集器中的物质 一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
固体混合物$\stackrel{过量稀盐酸}{→}$淡黄色溶液$\stackrel{KSCN溶液}{→}$淡红色溶液$\stackrel{过量H_{2}O_{2}溶液}{→}$深红色溶液$\stackrel{静置一段溶液}{→}$红色褪去
①淡红色溶液中加入过量H2O2溶液后,溶液红色加深的原因是2Fe2++2H++H2O2=2F3++2H2O(用离子方程式表示).
②已知红色褪去的同时有气体生成,经检验气体为O2.该小组对红色褪去的原因进行探究.
由实验Ⅰ和Ⅱ可得出的结论为H2O2将SCN-氧化成SO42-.

已知:①无水氯化铁在空气中易潮解,加热易升华;
②工业上,向500~600℃的铁屑中通人氯气可生产无水氯化铁;
③向炽热的铁屑中通入氯化氢可以生产无水氯化亚铁和氢气,
(1)仪器N的名称是分液漏斗,N中盛有浓盐酸,烧瓶M中的固体试剂KMnO4(或KClO3) (填化学式).
(2)装置的连接顺序为→a,→g→h→d→e→bc→d→e→f.(用小写字母表示,部分装置可以重复使用)
(3)若缺少装置E,则对本实验造成的影响是HCl和Fe反应生成的H2与Cl2混合受热发生爆炸,且有杂质氯化亚铁生成
(4)已知硫代硫酸钠(Na2S2O3)溶液在工业上可作脱氯剂,反应后Na2S2O3被氧化为Na2SO4,则装置D中
发生反应的离子方称式为S2O32-+4Cl2+5H2O=2SO42-+8Cl-+10H+.
(5)实验结束并冷却后,将硬质玻璃管及收集器中的物质 一并快速转移至锥形瓶中,加入过量的稀盐酸和少许植物油(反应过程中不振荡),充分反应后,进行如下实验:
固体混合物$\stackrel{过量稀盐酸}{→}$淡黄色溶液$\stackrel{KSCN溶液}{→}$淡红色溶液$\stackrel{过量H_{2}O_{2}溶液}{→}$深红色溶液$\stackrel{静置一段溶液}{→}$红色褪去
①淡红色溶液中加入过量H2O2溶液后,溶液红色加深的原因是2Fe2++2H++H2O2=2F3++2H2O(用离子方程式表示).
②已知红色褪去的同时有气体生成,经检验气体为O2.该小组对红色褪去的原因进行探究.
| 实验 | 操作 | 现象 | |
| 实验I(取褪色后溶液3等份) | 第1份 | 滴加FeCl3溶液 | 无明显变化 |
| 第2份 | 滴加KSCN溶液 | 溶液出现红色 | |
| 第3份 | 滴加稀盐酸和BaCl2 | 产生白色沉淀 | |
| 实验Ⅱ(取褪色后溶液同浓度的FeCi3溶液) | 滴加2KSCN溶液,溶液变红,再通入O2 | 无明显变化 | |
2.氯化亚铜(CuCl,白色、易氧化,Ksp=1.2×10-6)广泛用作催化剂、脱臭剂、脱色剂等.工业上用初级铜矿粉(主要含Cu2S、CuS、Fe2O3、FeO等)制备活性CuCl的流程如图:
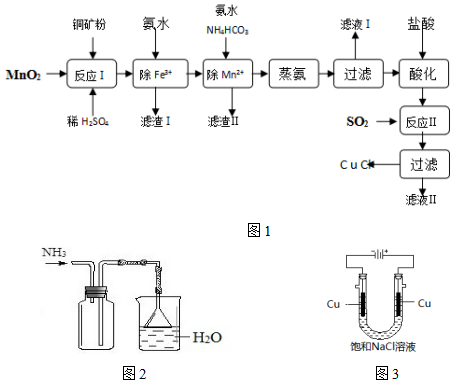
(1)滤渣Ⅰ是Fe(OH)3和单质硫的混合物,反应Ⅰ中Cu2S参与反应的化学方程式为:Cu2S+MnO2+H2SO4→CuSO4+S+MnSO4+H2O(未配平)
氧化产物为:CuSO4、S
(2)除Mn2+时得MnCO3沉淀,该反应的离子方程式Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O
(3)已知:Cu(OH)2可溶于氨水形成深蓝色溶液.Cu(OH)2+4NH3?[Cu(NH3)4]2++2OH-
蒸氨条件及蒸氨效果见表
由表中信息可知蒸氨的条件应选c(填序号).蒸出的氨可以回收利用,在实验室用图2装置来收集当集气瓶收集满氨时观察到的现象是漏斗中的液面忽上忽下.
(4)反应Ⅱ的离子方程式SO2+2Cu2++2Cl-+2H2O=2CuCl↓+SO42-+4H+.
(5)实验证明通过图3装置也可获得CuCl,现象为
阴极:产生无色气体
阳极:有白色胶状沉淀生成且逐渐增多
U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色沉淀,
①生成CuCl的电极反应式为Cu-e-+Cl-=CuCl↓.
②有同学提出说:淡黄色沉淀可能是CuOH,以下是从资料中查阅到的有关CuOH信息,哪些可以支持该同学的说法bd.(填序号)
a.容易脱水变成红色的Cu2O.
b.CuOH是黄色或淡黄色固体,不溶于水
c.价格:240元/Kg
d.CuOH的Ksp=2×10-15
e.易被氧化成Cu(OH)2.

(1)滤渣Ⅰ是Fe(OH)3和单质硫的混合物,反应Ⅰ中Cu2S参与反应的化学方程式为:Cu2S+MnO2+H2SO4→CuSO4+S+MnSO4+H2O(未配平)
氧化产物为:CuSO4、S
(2)除Mn2+时得MnCO3沉淀,该反应的离子方程式Mn2++HCO3-+NH3•H2O=MnCO3↓+NH4++H2O
(3)已知:Cu(OH)2可溶于氨水形成深蓝色溶液.Cu(OH)2+4NH3?[Cu(NH3)4]2++2OH-
蒸氨条件及蒸氨效果见表
| 序号 | 温度/℃ | 时间/min | 压强/KPa | 残液颜色 |
| a | 110 | 60 | 101.3 | 浅蓝色 |
| b | 100 | 40 | 74.6 | 几乎很浅 |
| c | 90 | 30 | 60.0 | 无色透明 |
(4)反应Ⅱ的离子方程式SO2+2Cu2++2Cl-+2H2O=2CuCl↓+SO42-+4H+.
(5)实验证明通过图3装置也可获得CuCl,现象为
阴极:产生无色气体
阳极:有白色胶状沉淀生成且逐渐增多
U形管底部:靠近阴极区白色胶状沉淀逐渐转化为淡黄色沉淀,
①生成CuCl的电极反应式为Cu-e-+Cl-=CuCl↓.
②有同学提出说:淡黄色沉淀可能是CuOH,以下是从资料中查阅到的有关CuOH信息,哪些可以支持该同学的说法bd.(填序号)
a.容易脱水变成红色的Cu2O.
b.CuOH是黄色或淡黄色固体,不溶于水
c.价格:240元/Kg
d.CuOH的Ksp=2×10-15
e.易被氧化成Cu(OH)2.
19.已知有如下反应:
①ClO3-+5Cl-+6H+═3Cl2↑+3H2O,
②2FeCl3+2KI═2FeCl2+2KCl+I2,
③2FeCl2+Cl2═2FeCl3,下列说法正确的是( )
0 161783 161791 161797 161801 161807 161809 161813 161819 161821 161827 161833 161837 161839 161843 161849 161851 161857 161861 161863 161867 161869 161873 161875 161877 161878 161879 161881 161882 161883 161885 161887 161891 161893 161897 161899 161903 161909 161911 161917 161921 161923 161927 161933 161939 161941 161947 161951 161953 161959 161963 161969 161977 203614
①ClO3-+5Cl-+6H+═3Cl2↑+3H2O,
②2FeCl3+2KI═2FeCl2+2KCl+I2,
③2FeCl2+Cl2═2FeCl3,下列说法正确的是( )
| A. | 反应①中氧化剂与还原剂的物质的量之比为5:1 | |
| B. | 反应②中FeCl3只作氧化剂,反应③中FeCl3只是氧化产物 | |
| C. | 反应②中每生成127g I2,转移的电子数为2NA | |
| D. | 根据上述三个反应可知氧化性:ClO3->Cl2>Fe3+>I2 |
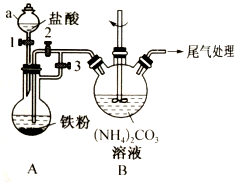 乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.以下是一种制备乳酸亚铁的实验方法.
乳酸亚铁{[CH3CH(OH)COO]2Fe}是一种很好的食品铁强化剂,易溶于水,吸收效果比无机铁好,可由乳酸与FeCO3反应制得.以下是一种制备乳酸亚铁的实验方法.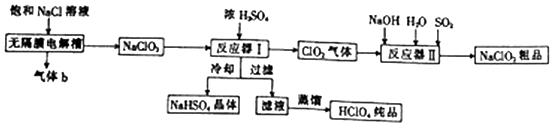
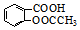 和
和 

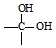 $\stackrel{自动脱水}{→}$
$\stackrel{自动脱水}{→}$
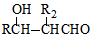 $\stackrel{△}{→}$
$\stackrel{△}{→}$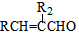 +H2O
+H2O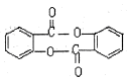 .
.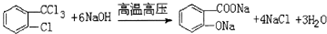 .
.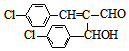 .
.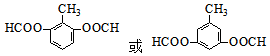 .(任写出一种)
.(任写出一种)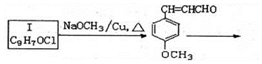
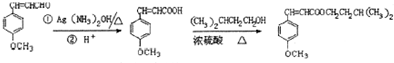 .
.