15.下列各组离子在指定溶液中能大量共存的是( )
| A. | 酸性溶液中:Na+、Cl-、OH-、CO32- | B. | 碱性溶液中:Fe3+、NH4+、HCO3-、Cl- | ||
| C. | 无色溶液中:Na+、Cu2+、MnO4-、I- | D. | 透明溶液中:Na+、Fe3+、Cl-、SO42- |
14.下列有关仪器的使用方法或实验操作正确的是( )
| A. | 盛装碱性试剂的试剂瓶应该使用橡皮塞 | |
| B. | 分离酒精和水可以采用分液法 | |
| C. | 蒸发结晶时应该将水分全部蒸干 | |
| D. | 在托盘天水左右托盘各放质量大小相同的纸,在左边纸上放氢氧化钠称量 |
13.设NA为阿伏伽德罗常数的值,下列说法正确的是( )
| A. | 标准状况下,22.4L水中含有水分子数为NA | |
| B. | 1mol Na2CO3 固体中含有的钠离子数为NA | |
| C. | 16g O2中含有的氧原子数为NA | |
| D. | 0.1mol/L的NaOH溶液中含有OH-的数为NA |
12.下列有关物质的分类不正确的是( )
| A. | 硫酸(酸) | B. | 溶液(混合物) | C. | Al2O3(两性氧化物) | D. | 纯碱(碱) |
11.化学无处不在,下列有关化学与生活、生产和技术的说法中,不正确的是( )
| A. | 医疗上常用75%的酒精进行消毒 | B. | 光导纤维的主要成份是二氧化硅 | ||
| C. | 食品行业用小苏打制作发酵粉 | D. | SO2可以随意排放,对环境没有污染 |
10.a、b、c、d为原子序数依次增大的四种短周期主族元素.a的最外层电子数是内层电子数的3倍,b的M层上有1个电子,a与c同主族.下列说法不正确的是( )
| A. | 原子半径:b>c>d | |
| B. | 气态氢化物稳定性:a>c | |
| C. | 简单阴离子还原性:d>c | |
| D. | ab可形成既含离子键又含共价键的离子化合物 |
9. X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
 X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )
X、Y、Z、M、Q、R皆为前20号元素,其原子半径与主要化合价的关系如图所示.下列说法错误的是( )| A. | Q位于第三周期IA族 | |
| B. | X、Y、Z三种元素组成的化合物可能是盐或碱 | |
| C. | 简单离子半径:M->Q+>R2+ | |
| D. | Z与M的最高价氧化物对应水化物均为强酸 |
8.已知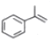 (异丙烯苯)$→_{一定条件}^{+H_{2}}$
(异丙烯苯)$→_{一定条件}^{+H_{2}}$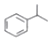 (异丙苯),下列说法错误的是( )
(异丙苯),下列说法错误的是( )
 (异丙烯苯)$→_{一定条件}^{+H_{2}}$
(异丙烯苯)$→_{一定条件}^{+H_{2}}$ (异丙苯),下列说法错误的是( )
(异丙苯),下列说法错误的是( )| A. | 反应属于加成反应 | B. | 异丙苯的一氯代物共有6种 | ||
| C. | 可用溴水鉴别异丙烯苯和异丙苯 | D. | 异丙苯是苯的同系物 |
6.硫代硫酸钠晶体(Na2S2O3•5H2O)在化学定量分析中常用作基准物质.它易溶于水,难溶于乙醇,加热、遇酸均易分解.某实验小组设计如下装置模拟工业生产制备硫代硫酸钠晶体(夹持仪器和加热装置省略).
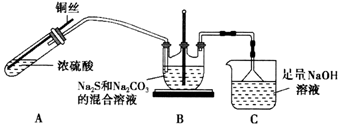
实验步骤如下:
①加热装置A,控制反应速率,使A中产生的气体均匀的通入B中,同时不断搅动,加热.
②当溶液的pH接近7时,停止通入SO2气体.
③将反应后的溶液转移至蒸发皿中,蒸发浓缩,到溶液表面出现晶膜时停止加热.再经冷却结晶、过滤、洗涤,将晶体放入烘箱中,在40℃左右干燥50~60min,得到产品.
回答下列问题:
(1)步骤①,在装置B中反应生成Na2S2O3,已知反应中只有一种变价元素,则B中反应的离子方程式为2S2-+CO32-+4SO2$\frac{\underline{\;\;△\;\;}}{\;}$3S2O32-+CO2.
(2)步骤②当溶液的pH接近7时,停止通入SO2气体的原因是Na2S2O3遇酸易分解,二氧化硫过量会使溶液的酸性增强,使产率降低.
(3)若要停止A中的化学反应,除熄灭酒精灯外,还可以采取的措施是将铜丝抽离液面.
(4)完成步骤③中的两处实验操作:蒸发浓缩、冷却结晶.
(5)为探究实验后装置C中溶液的溶质成分,该实验小组又进行了如下实验.
供选择的试剂为:Al(OH)3粉末、酚酞试液、稀硫酸、稀硝酸、Ba(NO3)2溶液
0 161753 161761 161767 161771 161777 161779 161783 161789 161791 161797 161803 161807 161809 161813 161819 161821 161827 161831 161833 161837 161839 161843 161845 161847 161848 161849 161851 161852 161853 161855 161857 161861 161863 161867 161869 161873 161879 161881 161887 161891 161893 161897 161903 161909 161911 161917 161921 161923 161929 161933 161939 161947 203614

实验步骤如下:
①加热装置A,控制反应速率,使A中产生的气体均匀的通入B中,同时不断搅动,加热.
②当溶液的pH接近7时,停止通入SO2气体.
③将反应后的溶液转移至蒸发皿中,蒸发浓缩,到溶液表面出现晶膜时停止加热.再经冷却结晶、过滤、洗涤,将晶体放入烘箱中,在40℃左右干燥50~60min,得到产品.
回答下列问题:
(1)步骤①,在装置B中反应生成Na2S2O3,已知反应中只有一种变价元素,则B中反应的离子方程式为2S2-+CO32-+4SO2$\frac{\underline{\;\;△\;\;}}{\;}$3S2O32-+CO2.
(2)步骤②当溶液的pH接近7时,停止通入SO2气体的原因是Na2S2O3遇酸易分解,二氧化硫过量会使溶液的酸性增强,使产率降低.
(3)若要停止A中的化学反应,除熄灭酒精灯外,还可以采取的措施是将铜丝抽离液面.
(4)完成步骤③中的两处实验操作:蒸发浓缩、冷却结晶.
(5)为探究实验后装置C中溶液的溶质成分,该实验小组又进行了如下实验.
供选择的试剂为:Al(OH)3粉末、酚酞试液、稀硫酸、稀硝酸、Ba(NO3)2溶液
| 序号 | 操作及现象 | 结论 |
| ① | 取少量Al(OH)3粉末于试管中,滴加适量溶液,振荡,白色粉末溶解 | 溶质中一定含有NaOH |
| ② | 取2nL溶液于试管中,滴加足量氯水,氯水褪色丙有气泡产生,再滴加几滴Ba(NO3)2溶液,有白色沉淀产生 | 溶质为NaOH和 Na2CO3、Na2SO3 |
| 取2mL溶液于试管中,若 先加入足量稀硝酸,产生气泡,再滴入几滴Ba(NO3)2溶液,无沉淀产生 | 溶质为为NaOH和Na2CO3 |
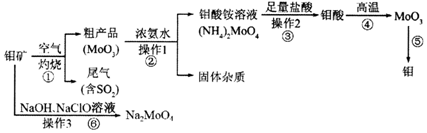
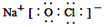 ;反应⑥生成三种钠盐,写出该反应的离子方程式:MoS2+OH-+ClO-=MoO42-+2SO42-+9Cl-+H2O
;反应⑥生成三种钠盐,写出该反应的离子方程式:MoS2+OH-+ClO-=MoO42-+2SO42-+9Cl-+H2O