1.根据下列实验操作和现象所得到的结论正确的是( )
| 选项 | 实验操作和现象 | 结论 |
| A | 向某食盐溶液中滴加淀粉溶液,溶液颜色没有变为蓝色 | 不是加碘食盐 |
| B | 某溶液中加入硝酸酸化的Ba(NO3)2溶液,无现象,再滴加AgNO3溶液,有白色沉淀生成 | 溶液中一定含有Cl- |
| C | 室温下,用pH试纸分别测0.100mol•L-1 CH3COONa溶液和0.100mol•L-1 Na2S溶液的pH,后者pH大 | 酸性:H2S<CH3COOH |
| D | 将气体X分别通入溴水和酸性高锰酸钾溶液,两溶液均褪色 | 气体X一定是C2H4 |
| A. | A | B. | B | C. | C | D. | D |
20.工业上可由乙苯生产苯乙烯,反应原理如下: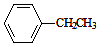 $→_{加热}^{Fe_{2}O_{3}}$
$→_{加热}^{Fe_{2}O_{3}}$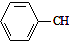 =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )
 $→_{加热}^{Fe_{2}O_{3}}$
$→_{加热}^{Fe_{2}O_{3}}$ =CH2+H2,下列说法正确的是( )
=CH2+H2,下列说法正确的是( )| A. | 酸性高锰酸钾溶液和溴水都可以用来鉴别乙苯和苯乙烯 | |
| B. | 乙苯、苯乙烯均能发生取代反应、加聚反应,氧化反应 | |
| C. | 乙苯的一氯取代产物有共有5种 | |
| D. | 乙苯和苯乙烯分子内共平面的碳原子数最多均为7 |
19.设NA为阿伏加德罗常数值,下列有关叙述正确的是( )
| A. | 1.8gH2O与CH2D2的混合物中所含质子数为NA | |
| B. | 1mol甲烷或白磷(P4)分子中所含共价键数均为4NA | |
| C. | 1mol CH3COOC2H5在稀硫酸溶液中水解可得到乙醇分子数为NA | |
| D. | 25℃时,l L pH=1的H2SO4溶液中含有的H+ 数为0.2NA |
18.化学在工农业生产和日常生活中都有重要应用.下列叙述正确的是( )
| A. | 油脂和蛋白质是人体必需的营养物质,都属于高分子化合物 | |
| B. | 食品包装袋中常有硅胶、生石灰、还原铁粉等,其作用都是防止食品氧化变质 | |
| C. | 城际“轻轨电车”启动时,电车电刷与导线的接触点会产生高温,石墨可用作接触点上的材料 | |
| D. | 中医古籍《肘后备急方》中“青蒿一握,以水二升渍,绞取汁,尽服之”启发了屠呦呦,采用低温提取,解决了关键性的技术难题.青蒿素的提取属于化学变化 |
17.三盐(3PbO•PbSO4•H2O)可用作聚氯乙烯的热稳定剂,200℃以上开始失去结晶水,不溶于水及有机溶剂.以200.0t铅泥(主要成分为PbO、Pb及PbSO4等)为原料制备三盐的工艺流程如图所示.
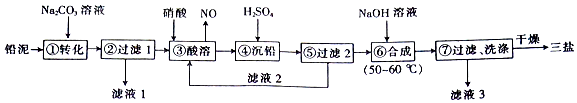
已知:PbSO4和PbCO3的溶解度和溶度积Ksp如表.
(1)步骤①转化的目的是将PbSO4转化为PbCO3,滤液1中的溶质为Na2CO3和Na2SO4(填化学式).
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是适当升温(或适当增大硝酸浓度或减小沉淀粒径等)(任写一条).其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O.
(3)滤液2中可循环利用的溶质的化学式为HNO3.若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol/L,则此时c(SO42-)=1.00×10-3mol/L.
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是取少量最后一次的洗涤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.
(5)步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH$\frac{\underline{\;50~60℃\;}}{\;}$3PbO•PbSO4•H2O+3Na2SO4+2H2O,若得到纯净干燥的三盐99.Ot,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为51.75%.

已知:PbSO4和PbCO3的溶解度和溶度积Ksp如表.
| 化合物 | PbSO4 | PbCO3 |
| 溶解度/g | 1.03×10-4 | 1.81×10-7 |
| Ksp | 1.82×10-8 | 1.46×10-13 |
(2)步骤③酸溶时,为提高酸溶速率,可采取的措施是适当升温(或适当增大硝酸浓度或减小沉淀粒径等)(任写一条).其中铅与硝酸反应生成Pb(NO3)2和NO的离子方程式为3Pb+8H++2NO3-=3Pb2++2NO↑+4H2O.
(3)滤液2中可循环利用的溶质的化学式为HNO3.若步骤④沉铅后的滤液中c(Pb2+)=1.82×10-5mol/L,则此时c(SO42-)=1.00×10-3mol/L.
(4)步骤⑦洗涤操作时,检验沉淀是否洗涤完全的方法是取少量最后一次的洗涤液于试管中,向其中滴加盐酸酸化的BaCl2溶液,若不产生白色沉淀,则表明已洗涤完全.
(5)步骤⑥合成三盐的化学方程式为4PbSO4+6NaOH$\frac{\underline{\;50~60℃\;}}{\;}$3PbO•PbSO4•H2O+3Na2SO4+2H2O,若得到纯净干燥的三盐99.Ot,假设铅泥中的铅元素有80%转化为三盐,则铅泥中铅元素的质量分数为51.75%.
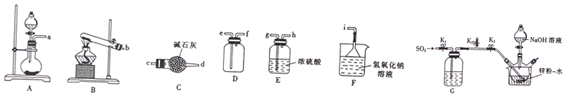
15.下列操作或装置能达到实验目的是( )
| A. | 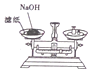 称取一定量的NaOH | |
| B. | 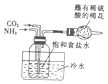 制取NaHCO3 | |
| C. | 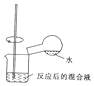 检验浓硫酸与铜反应后的产物中是否含有铜离子 | |
| D. | 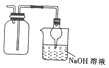 收集NO2丙防止其污染环境 |
14. 法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,合成轮烷的基本原料有CH2C12、丙烯、戊醇、苯,下列说法不正确的是( )
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,合成轮烷的基本原料有CH2C12、丙烯、戊醇、苯,下列说法不正确的是( )
 法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,合成轮烷的基本原料有CH2C12、丙烯、戊醇、苯,下列说法不正确的是( )
法国、美国、荷兰的三位科学家因研究“分子机器的设计与合成”获得2016年诺贝尔化学奖.轮烷是一种分子机器的“轮子”,合成轮烷的基本原料有CH2C12、丙烯、戊醇、苯,下列说法不正确的是( )| A. | CH2C12有两种同分异构体 | |
| B. | 丙烯能使溴水褪色 | |
| C. | 戊醇在一定条件下能与乙酸发生酯化反应 | |
| D. | 苯与足量氢气在镍催化作用下会发生加成反应生成环己烷 |
13.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | lmo1CH4中含有的电子数为9NA | |
| B. | 0.1mol•L-1的Na2S溶液中所含阴离子的数目大于0.1NA | |
| C. | 1molMg在空气中完全燃烧生成MgO和Mg3N2,转移的电子数为2NA | |
| D. | 80℃时,1LNaCl溶液中含有OH-的数目为1×10-7NA |
12.化学在生产生活中有着广泛的应用,下列对应关系错误的是( )
0 161689 161697 161703 161707 161713 161715 161719 161725 161727 161733 161739 161743 161745 161749 161755 161757 161763 161767 161769 161773 161775 161779 161781 161783 161784 161785 161787 161788 161789 161791 161793 161797 161799 161803 161805 161809 161815 161817 161823 161827 161829 161833 161839 161845 161847 161853 161857 161859 161865 161869 161875 161883 203614
| 选项 | 性质 | 实际应用 |
| A | 蛋白质受热变性 | 用高温加热的方法杀死流感病毒 |
| B | 明矾溶液显酸性 | 用明矾溶液清除铜镜表面的铜锈 |
| C | Na2CO3溶液显碱性 | 用热的纯碱溶液洗去油污 |
| D | P2O5具有吸水性 | 用P2O5干燥氨气 |
| A. | A | B. | B | C. | C | D. | D |