12.下列根据实验操作和现象得出的结论正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将少量Fe(NO3)2试样加水溶解后,滴加稀硫酸酸化,再滴加KSCN溶液 | 溶液变成血红色 | Fe(NO3)2试样已变质 |
| B | 向甲苯中滴加少量酸性高锰酸钾溶液 | 高锰酸钾溶液褪色 | 甲苯发生了氧化反应 |
| C | 常温下分别测定浓度均为0.1mol/L的Na2SiO3溶液和Na2CO3溶液的pH | pH:Na2SiO3>Na2CO3 | 非金属性:Si>C |
| D | 将少量某无色气体通入澄清石灰水中 | 出现白色沉淀 | 该气体一定是CO2 |
| A. | A | B. | B | C. | C | D. | D |
11.LiH可用作制取氢弹的原料,制备反应为2Li(熔融)+H2$\frac{\underline{\;\;△\;\;}}{\;}$2LiH.下列有关说法不正确的是( )
| A. | 还原性:H2>Li | B. | H-与Li+的电子层结构相同 | ||
| C. | 微粒半径:r(H-)>r(H)>r(H+) | D. | LiH属于离子化合物 |
10.化学与生产生活密切相关,下列说法正确的是( )
| A. | 镁铝合金粉末着火后可用干冰灭火器灭火 | |
| B. | 装潢涂料用苯作溶剂比用水作溶剂好 | |
| C. | 自来水中的亚硝胺超标会危害人体健康 | |
| D. | 提倡使用一次性筷子、纸杯等,更有利于保护环境 |
8.以下分离提纯操作能达到相应目的是( )
| 选项 | 操作 | 目的 |
| A | 蒸馏 | 分离氯化钠和硝酸钾混合溶液 |
| B | 分液 | 分离乙酸与乙酸乙酯混合物 |
| C | 洗气 | 通入小苏打溶液中除去CO2中的HCl气体 |
| D | 用乙醇作萃取剂 | 提取溴水中的溴单质 |
| A. | A | B. | B | C. | C | D. | D |
7.用NA代表阿伏加德罗常数的值.下列叙述正确的是( )
| A. | 9g超重水(3H216O)含中子数为6NA | |
| B. | 标准状况下,22.4LCCl4含有的分子数目为NA | |
| C. | 常温常压下,16g甲烷含有共价键数目为4NA | |
| D. | 1L0.1mol•L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA |
6.甲、乙、丙符合如图所示转化关系,甲是( )
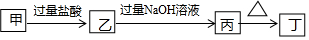
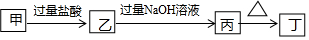
| A. | NH3 | B. | SiO2 | C. | Al2O3 | D. | Mg |
5.某有机物的结构如图,关于该有机物的说法不正确的是( )
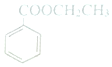

| A. | 分子式为C9H10O2 | |
| B. | 能发生取代、加成反应 | |
| C. | 苯环上的一氯代物有3种 | |
| D. | 在酸性条件下水解产物均能与NaOH溶液反应 |
4.如图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子是Ar
(2)地壳中含量最多的金属元素是Al;非金属性最强的元素F
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.①的最高价氧化物对应的水化物的化学式为HNO3,其稀溶液与铜反应的化学方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.当有0.4mol该物质被还原,则转移的电子为0.3mol.
(5)①、②、③所形成的气体氢化物的稳定性由强到弱的顺序HF>H2O>NH3
(6)完成下列反应的化学方程式:⑦的氧化物与氢氧化钠溶液反应SiO2+2NaOH=Na2SiO3+H2O,④、⑥的最高价氧化物对应的水化物两两反应:Al(OH)3+NaOH=NaAlO2+2H2O.
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | |||||
| 三 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ||
| 四 | ⑩ |
(2)地壳中含量最多的金属元素是Al;非金属性最强的元素F
(3)这些元素中的最高价氧化物对应的水化物中,酸性最强的是HClO4,碱性最强的是KOH,呈两性的氢氧化物是Al(OH)3.
(4)在这些元素中,原子半径最小的是F,原子半径最大的是K.①的最高价氧化物对应的水化物的化学式为HNO3,其稀溶液与铜反应的化学方程式为3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O.当有0.4mol该物质被还原,则转移的电子为0.3mol.
(5)①、②、③所形成的气体氢化物的稳定性由强到弱的顺序HF>H2O>NH3
(6)完成下列反应的化学方程式:⑦的氧化物与氢氧化钠溶液反应SiO2+2NaOH=Na2SiO3+H2O,④、⑥的最高价氧化物对应的水化物两两反应:Al(OH)3+NaOH=NaAlO2+2H2O.
3.设NA为阿伏加德罗常数的值.下列说法正确的是( )
0 161614 161622 161628 161632 161638 161640 161644 161650 161652 161658 161664 161668 161670 161674 161680 161682 161688 161692 161694 161698 161700 161704 161706 161708 161709 161710 161712 161713 161714 161716 161718 161722 161724 161728 161730 161734 161740 161742 161748 161752 161754 161758 161764 161770 161772 161778 161782 161784 161790 161794 161800 161808 203614
| A. | 标准状况下,11.2L CHCl3含有的原子总数为2.5NA | |
| B. | 25g质量分数为68%的H2O2溶液中含有氧原子数目为NA | |
| C. | 高温下,16.8gFe与足量水蒸气完全反应失去0.8NA个电子 | |
| D. | 1molCH5+中含有的电子数目为11NA |