4.下列有关性质的比较,不能用元素周期律解释的是( )
| A. | 碱性:KOH>NaOH | B. | 金属性:Na>Al | C. | 稳定性:HF>CH4 | D. | 酸性:HClO<HClO4 |
3.化学与生活密切相关,下列说法不正确的是( )
| A. | 次氯酸钠溶液可用作环境的杀菌消毒 | |
| B. | 硅胶可用作商品包装袋的干燥剂 | |
| C. | 爆竹燃放后,硫燃烧生成SO3 | |
| D. | 施肥时,草木灰不能与胺态氮肥混合使用 |
2.某学习小组探究Mg与NaHCO3溶液反应的机理,做了如下探究.
实验一:
(1)实验B的目的是与实验A做对照,排除水的干扰
(2)用化学用语表示NaHCO3溶于水所发生的所有变化NaHCO3=Na++HCO3-、HCO3-?H++CO32-,HCO3-+H2O?H2CO3+OH-.
(3)写出Mg与H2O反应方程式Mg+2H2O=Mg(OH)2+H2↑
实验二:

(4)根据氧化还原规律,实验A和B产生的气体中必然有H2(填分子式)
实验三:
分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象.
(5)实验三说明Mg与NaHCO3溶液反应产生了CO32-(填离子符号).用平衡移动原理解释产生该离子的原因:溶液中存在平衡HCO3-?H++CO32-,加入镁与H+反应,使c(H+)减少,平衡正移,产生CO32-.
实验四:
对A中白色沉淀的成分,同学们提出了如下假设:
Ⅰ.Mg(OH)2 Ⅱ.MgCO3Ⅲ.碱式碳酸镁
将A中白色沉淀过滤、洗涤后,取0.1mol加入1mol/L盐酸800mL恰好完全反应,产生标况下的CO2气体6.72L.
(6)填写上述假设.Mg(OH)2、MgCO3(填两个既得分)
(7)白色沉淀的主要成分为Mg(OH)2 •3MgCO3.
(8)综上所述,Mg与NaHCO3溶液反应的产物有Na2CO3、H2、CO2、Mg(OH)2•3MgCO3.(填写化学式)
实验一:
| 实验A | 实验B | |
| 操作 | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL饱和NaHCO3溶液. | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL蒸馏水. |
| 现象 | 有气体产生,20min后注射器内壁和底部产生大量白色沉淀 | 缓慢产生气体 |
(2)用化学用语表示NaHCO3溶于水所发生的所有变化NaHCO3=Na++HCO3-、HCO3-?H++CO32-,HCO3-+H2O?H2CO3+OH-.
(3)写出Mg与H2O反应方程式Mg+2H2O=Mg(OH)2+H2↑
实验二:

(4)根据氧化还原规律,实验A和B产生的气体中必然有H2(填分子式)
实验三:
分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象.
(5)实验三说明Mg与NaHCO3溶液反应产生了CO32-(填离子符号).用平衡移动原理解释产生该离子的原因:溶液中存在平衡HCO3-?H++CO32-,加入镁与H+反应,使c(H+)减少,平衡正移,产生CO32-.
实验四:
对A中白色沉淀的成分,同学们提出了如下假设:
Ⅰ.Mg(OH)2 Ⅱ.MgCO3Ⅲ.碱式碳酸镁
将A中白色沉淀过滤、洗涤后,取0.1mol加入1mol/L盐酸800mL恰好完全反应,产生标况下的CO2气体6.72L.
(6)填写上述假设.Mg(OH)2、MgCO3(填两个既得分)
(7)白色沉淀的主要成分为Mg(OH)2 •3MgCO3.
(8)综上所述,Mg与NaHCO3溶液反应的产物有Na2CO3、H2、CO2、Mg(OH)2•3MgCO3.(填写化学式)
20.下列设计的实验方案能达到相应实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 证明“84”消毒液的氧化能力随溶液pH的减小而增强 | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 |
| B | 证明反应速率会随反应物浓度的增大而加快 | 用3 mL稀硫酸与足量纯锌反应,产生气泡速率较慢,然后加入1mL 1mol•L-1CuSO4溶液,迅速产生较多气泡 |
| C | 检验Na2SO3晶体是否已氧化变质 | 将Na2SO3样品溶于稀硝酸后,滴加BaCl2溶液,观察是否有沉淀生成 |
| D | 证明同温度下氯化银的溶解度大于硫化银的溶解度 | 向2 mL0.1 mol•L-1硝酸银溶液中加入1mL0.1mol•L-1 NaC1溶液,出现白色沉淀,再加入几滴0.1 mol•L-1的Na2S溶液,有黑色沉淀生成 |
| A. | A | B. | B | C. | C | D. | D |
19.关于有机物的下列说法,正确的是( )
| A. | 分子式为C5H12的有机物有三种,它们互为同系物 | |
| B. | 淀粉和纤维素的化学式相同,化学性质相似 | |
| C. | 乙酸乙酯在过量氢氧化钠溶液中加热,生成乙酸和乙醇 | |
| D. | 溶解度:甘油>1-丁醇>甲酸甲酯 |
18.一定条件下,某含碳钢腐蚀情况与溶液pH的关系如表
下列说法正确的是( )
| pH | 2 | 4 | 6 | 6.5 | 8 | 13.5 | 14 | |
| 腐蚀快慢 | 较快 | 慢 | 较快 | |||||
| 主要产物 | Fe2+ | Fe3O4 | Fe2O3 | FeO2- | ||||
| A. | 随pH的升高,碳钢腐蚀速率逐渐加快 | |
| B. | pH<4,发生析氢腐蚀 | |
| C. | pH为14,其负极反应为2H2O+Fe_3e-═FeO2-+4H+ | |
| D. | pH为7时,负极反应为Fe_3e-═Fe3+,生成的Fe3+被空气中的氧气氧化为Fe2O3 |
17.下列离子或分子能够在指定的分散系中大量共存的是( )
0 161512 161520 161526 161530 161536 161538 161542 161548 161550 161556 161562 161566 161568 161572 161578 161580 161586 161590 161592 161596 161598 161602 161604 161606 161607 161608 161610 161611 161612 161614 161616 161620 161622 161626 161628 161632 161638 161640 161646 161650 161652 161656 161662 161668 161670 161676 161680 161682 161688 161692 161698 161706 203614
| A. | 空气中:CO2、NO、N2、NH3 | |
| B. | 明矾溶液中:H+、Mg2+、Na+、Cl- | |
| C. | 过量铁与稀硝酸反应后的溶液中:H+、Cl-、I-、Na+ | |
| D. | 常温下,水电离出的c(H+)=1×10-12mol/L的溶液中:NH4+、Na+、Cl-、CO32- |

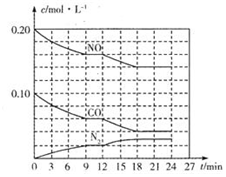 为有效控制雾霾,各地积极采取措施改善大气质量,有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.
为有效控制雾霾,各地积极采取措施改善大气质量,有效控制空气中氮氧化物、碳氧化物和硫氧化物显得尤为重要.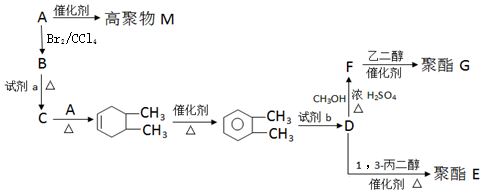
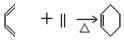
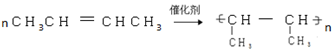 ②B→C
②B→C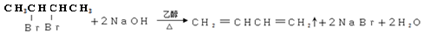
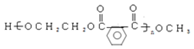 .
. 以CH3CHO为初始原料,选择必要试剂,经过三步反应合成化合物C,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)
以CH3CHO为初始原料,选择必要试剂,经过三步反应合成化合物C,写出合成路线(用结构简式表示有机物,用箭头表示转化关系,箭头上注明试剂和反应条件)