题目内容
17.下列离子或分子能够在指定的分散系中大量共存的是( )| A. | 空气中:CO2、NO、N2、NH3 | |
| B. | 明矾溶液中:H+、Mg2+、Na+、Cl- | |
| C. | 过量铁与稀硝酸反应后的溶液中:H+、Cl-、I-、Na+ | |
| D. | 常温下,水电离出的c(H+)=1×10-12mol/L的溶液中:NH4+、Na+、Cl-、CO32- |
分析 A.NO与氧气反应;
B.离子之间不发生反应;
C.酸性条件下硝酸根离子具有强氧化性;
D.常温下,水电离出的c(H+)=1×10-12mol/L的溶液可能呈酸性或碱性.
解答 解:A.NO与氧气反应,不能在空气中大量共存,故A错误;
B.明矾溶液中离子之间不发生反应,可大量共存,故B正确;
C.酸性条件下硝酸根离子具有强氧化性,可氧化亚铁离子,故C错误;
D.常温下,水电离出的c(H+)=1×10-12mol/L的溶液可能呈酸性或碱性,碱性条件下NH4+不能大量共存,酸性条件下CO32-不能大量共存,故D错误.
故选B.
点评 本题考查离子共存问题,为高考常见题型,侧重于元素化合物知识的综合考查和学生的分析能力、审题的能力的考查,注意把握常见离子的性质以及反应类型的判断,题目难度不大.

练习册系列答案
相关题目
7.将下列离子:Al3+、Na+、K+、NO3-、OH-、S2-、MnO4-、Fe3+、NH4+、H+、AlO2-、CO32-按可能大量共存的情况,把它们全部分成A、B两组,而且每组中都含有不少于两种阳离子和两种阴离子.下列离子不会同在一组的是( )
| A. | Na+、NO3- | B. | S2-、AlO2- | C. | Al3+、Fe3+ | D. | MnO4-、NH4+ |
12.下列物质:①甲醇;②邻甲基苯酚;③甲醛;④甲酸;⑤甲酸钠;⑥甲酸甲酯,在一定条件下能与新制氢氧化铜悬浊液反应生成红色沉淀的是( )
| A. | ①②③④ | B. | ③④⑤⑥ | C. | ②③④⑤ | D. | 全部都可以 |
2.某学习小组探究Mg与NaHCO3溶液反应的机理,做了如下探究.
实验一:
(1)实验B的目的是与实验A做对照,排除水的干扰
(2)用化学用语表示NaHCO3溶于水所发生的所有变化NaHCO3=Na++HCO3-、HCO3-?H++CO32-,HCO3-+H2O?H2CO3+OH-.
(3)写出Mg与H2O反应方程式Mg+2H2O=Mg(OH)2+H2↑
实验二:

(4)根据氧化还原规律,实验A和B产生的气体中必然有H2(填分子式)
实验三:
分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象.
(5)实验三说明Mg与NaHCO3溶液反应产生了CO32-(填离子符号).用平衡移动原理解释产生该离子的原因:溶液中存在平衡HCO3-?H++CO32-,加入镁与H+反应,使c(H+)减少,平衡正移,产生CO32-.
实验四:
对A中白色沉淀的成分,同学们提出了如下假设:
Ⅰ.Mg(OH)2 Ⅱ.MgCO3Ⅲ.碱式碳酸镁
将A中白色沉淀过滤、洗涤后,取0.1mol加入1mol/L盐酸800mL恰好完全反应,产生标况下的CO2气体6.72L.
(6)填写上述假设.Mg(OH)2、MgCO3(填两个既得分)
(7)白色沉淀的主要成分为Mg(OH)2 •3MgCO3.
(8)综上所述,Mg与NaHCO3溶液反应的产物有Na2CO3、H2、CO2、Mg(OH)2•3MgCO3.(填写化学式)
实验一:
| 实验A | 实验B | |
| 操作 | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL饱和NaHCO3溶液. | 在注射器中加入过量镁片(擦去表面氧化膜),吸入15mL蒸馏水. |
| 现象 | 有气体产生,20min后注射器内壁和底部产生大量白色沉淀 | 缓慢产生气体 |
(2)用化学用语表示NaHCO3溶于水所发生的所有变化NaHCO3=Na++HCO3-、HCO3-?H++CO32-,HCO3-+H2O?H2CO3+OH-.
(3)写出Mg与H2O反应方程式Mg+2H2O=Mg(OH)2+H2↑
实验二:

(4)根据氧化还原规律,实验A和B产生的气体中必然有H2(填分子式)
实验三:
分别取少量实验A和B的上层清液于两支试管中,各加入2滴BaCl2溶液,A中立即产生白色沉淀,B中无明显现象.
(5)实验三说明Mg与NaHCO3溶液反应产生了CO32-(填离子符号).用平衡移动原理解释产生该离子的原因:溶液中存在平衡HCO3-?H++CO32-,加入镁与H+反应,使c(H+)减少,平衡正移,产生CO32-.
实验四:
对A中白色沉淀的成分,同学们提出了如下假设:
Ⅰ.Mg(OH)2 Ⅱ.MgCO3Ⅲ.碱式碳酸镁
将A中白色沉淀过滤、洗涤后,取0.1mol加入1mol/L盐酸800mL恰好完全反应,产生标况下的CO2气体6.72L.
(6)填写上述假设.Mg(OH)2、MgCO3(填两个既得分)
(7)白色沉淀的主要成分为Mg(OH)2 •3MgCO3.
(8)综上所述,Mg与NaHCO3溶液反应的产物有Na2CO3、H2、CO2、Mg(OH)2•3MgCO3.(填写化学式)
9.已知苯乙烯的结构为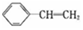 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )
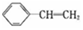 .有关该物质的下列说法正确的是( )
.有关该物质的下列说法正确的是( )| A. | 该物质在一定条件下和氢气完全加成,加成产物的一溴取代物有6种 | |
| B. | 该物质能使溴水和酸性高锰酸钾溶液褪色,褪色原理完全相同 | |
| C. | 苯乙烯分子的所有原子不可能在同一平面上 | |
| D. | 除去 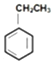 中的苯乙烯可以通入等量氢气反应 中的苯乙烯可以通入等量氢气反应 |
6.向盛有不同试剂的试管b中分别滴加适量0.1mol/L FeCl3 溶液,下列对b中现象的解释正确的是( )
| 实验 | b中物质 | b中现象 | 结论或解释 | |
 | A | Mg(OH)2悬浊液 | 有红棕色胶体产生 | 发生反应:Fe3++3OH-═Fe(OH)3(胶体) |
| B | Cu粉 | 溶液变蓝,试管底部有固体 | 溶液变蓝的原因是:3Cu+2Fe3+═2Fe+3Cu2+ | |
| C | 5%H2O2溶液 | 有气泡生成 | 该气体为氯气,双氧水强氧化性氧化Cl-产生 | |
| D | 饱和NaHCO3溶液 | 有气泡生成,且试管底部有固体 | 发生反应:Fe3++3HCO3-═Fe(OH)3+3CO2 |
| A. | A | B. | B | C. | C | D. | D |
7.根据表中信息判断,下列选项不正确的是( )
| 序号 | 反应物 | 产物 |
| ① | KMnO4、H2O2、H2SO4 | K2SO4、MnSO4 |
| ② | Cl2、FeBr2 | FeCl3、FeBr3 |
| ③ | MnO4-、Cl- | Cl2、Mn2+ |
| A. | 第①组反应的其余产物为H2O和O2 | |
| B. | 第②组反应中参加反应的Cl2与FeBr2的物质的量之比为1:2 | |
| C. | 第③组反应中生成1molCl2,转移电子2mol | |
| D. | 氧化性由强到弱顺序为MnO4->Cl2>Fe3+>Br2 |