5.氮气是一种不活泼的气体,其根本原因是( )
| A. | 氮元素的非金属性较弱 | B. | 氮原子半径较小 | ||
| C. | 氮气是双原子分子 | D. | 使N≡N键断裂需要很高的能量 |
4.下列措施不会影响水的电离平衡的是( )
| A. | 恒温条件下向水中加入少量Na2SO4固体 | |
| B. | 将水加热煮沸 | |
| C. | 恒温条件下向水中通入SO2气体 | |
| D. | 恒温条件下向水中通入氨气 |
3.下列化学反应的速率,前者一定大于后者的是( )
| A. | 相同温度下,颗粒大小相同的锌粒分别与pH值相同的硫酸和盐酸反应 | |
| B. | A+B$\stackrel{500℃}{→}$C;D+E$\stackrel{100℃}{→}$F | |
| C. | 相同温度下,与同浓度盐酸反应的锌粒和铁粉 | |
| D. | G+H→W+Q(Q>0),其他条件相同时分别在200℃和100℃时反应 |
2.判断溶液为中性的依据是( )
| A. | c(OH-)=1×10-7mol/L | B. | c(H+)=1×10-7mol/L | ||
| C. | c(OH-)=c(H+) | D. | pH=7 |
1.实验室可用如图装置(启普发生器)制取氢气.欲使得到氢气的速率加快,下列措施可行的是( )


| A. | 将稀硫酸改用浓硫酸 | B. | 向稀硫酸中加入少量硫酸铜溶液 | ||
| C. | 向稀硫酸中加入硫酸钠固体 | D. | 给装置中发生反应的部分加热 |
20.下列所述的操作中没有涉及到化学变化的是( )
| A. | 豆科作物的根瘤菌对空气中氮的固定 | |
| B. | 将NO2气体冷却后颜色会变浅 | |
| C. | 熟石膏转化为生石膏 | |
| D. | 工业制液态氧 |
18.下列关于电解质的有关叙述中正确的是( )
| A. | 电解质溶液的浓度越大,其导电性一定越强 | |
| B. | 熔融态能导电的物质一定是离子化合物 | |
| C. | 强极性键的共价化合物不一定都是强电解质 | |
| D. | 多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强 |
17.下列物质属于电解质的是( )
| A. | 氯水 | B. | Cu | C. | NH3 | D. | CaO |
16. 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
(1)将浓度为0.1mol/LHF溶液加水稀释一倍(假设温度不变),下列各量减小的是A.
A.c(H+) B.c(H+)•c(OH-) C.c(H+)/c(HF) D.c(OH-)/c(H+)
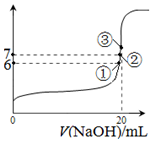
(2)25℃时,在20mL0.1mol•L-1氢氟酸中加入VmL0.1mol•L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是BC.
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时pH=7,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol•L-1
(3)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液,pH由大到小的顺序是①>④>②>③(用序号表示).
(4)Na2CO3水解的化学方程式Na2CO3+H2O?NaHCO3+NaOH
(5)简要说明NaHCO3溶液显碱性的原因HCO3-的水解程度大于HCO3-的电离程度.
0 161481 161489 161495 161499 161505 161507 161511 161517 161519 161525 161531 161535 161537 161541 161547 161549 161555 161559 161561 161565 161567 161571 161573 161575 161576 161577 161579 161580 161581 161583 161585 161589 161591 161595 161597 161601 161607 161609 161615 161619 161621 161625 161631 161637 161639 161645 161649 161651 161657 161661 161667 161675 203614
 电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:
电离平衡常数(用Ka表示)的大小可以判断电解质的相对强弱.25℃时,有关物质的电离平衡常数如下表所示:| 化学式 | HF | H2CO3 | HClO |
| 电离平衡常数 (Ka) | 7.2×10-4 | K1=4.4×10-7 K2=4.7×10-11 | 3.0×10-8 |
A.c(H+) B.c(H+)•c(OH-) C.c(H+)/c(HF) D.c(OH-)/c(H+)
(2)25℃时,在20mL0.1mol•L-1氢氟酸中加入VmL0.1mol•L-1NaOH溶液,测得混合溶液的pH变化曲线如图所示,下列说法正确的是BC.
A.pH=3的HF溶液和pH=11的NaF溶液中,由水电离出的c(H+)相等
B.①点时pH=6,此时溶液中,c(F-)-c(Na+)=9.9×10-7mol/L
C.②点时pH=7,溶液中的c(F-)=c(Na+)
D.③点时V=20mL,此时溶液中c(F-)<c(Na+)=0.1mol•L-1
(3)物质的量浓度均为0.1mol/L的下列四种溶液:①Na2CO3溶液②NaHCO3溶液③NaF溶液④NaClO溶液,pH由大到小的顺序是①>④>②>③(用序号表示).
(4)Na2CO3水解的化学方程式Na2CO3+H2O?NaHCO3+NaOH
(5)简要说明NaHCO3溶液显碱性的原因HCO3-的水解程度大于HCO3-的电离程度.
 固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的热化学方程式是:CO2+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ
固定和利用CO2,能有效地利用资源,并减少空气中的温室气体.工业上正在研究利用CO2来生产甲醇燃料的方法,该方法的热化学方程式是:CO2+3H2(g)?CH3OH(g)+H2O(g)+49.0kJ