题目内容
18.下列关于电解质的有关叙述中正确的是( )| A. | 电解质溶液的浓度越大,其导电性一定越强 | |
| B. | 熔融态能导电的物质一定是离子化合物 | |
| C. | 强极性键的共价化合物不一定都是强电解质 | |
| D. | 多元酸、多元碱的导电性一定比一元酸、一元碱的导电性强 |
分析 A.溶液导电能力与自由移动的离子浓度、离子带电荷数有关;
B.离子化合物是含有离子键的化合物;
C.电解质强弱取决于电离程度;
D.溶液导电能力与自由移动的离子浓度、离子带电荷数有关;
解答 解:A.电解质溶液的浓度越大,导电能力不一定越强,如浓硫酸不导电,故A错误;
B.铜熔融状态下能导电,属于单质,不是离子化合物,故B错误;
C.强极性键的共价化合物不一定都是强电解质,如H-F,故C正确;
D.溶液的导电能力与离子浓度与离子的电荷有关,浓度越大、所带电荷越多,导电能力越强,与几元酸碱无关,如磷酸是三元酸,但其为弱酸,同浓度电离出的离子浓度不及二元酸硫酸,故D错误;
故选:C.
点评 本题综合性较大,涉及强电解质、导电能力、极性等,难度不大,掌握物质的性质是解题的关键,平时注意基础知识的积累.

练习册系列答案
相关题目
8.化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
| A. | 原子核内有10个中子的氧原子:${\;}_{\;}^{18}$O | |
| B. | 乙烯的结构简式:CH2CH2 | |
| C. | CH4分子的比例模型: | |
| D. | 乙炔分子的电子式: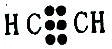 |
9.用如图所示装置进行下列实验,所选的药品、现象和结论正确的一组是( )
| 选项 | a | b | c | 现象 | 结论 | 装置 |
| A | 稀盐酸 | 大理石 | Na2SiO3溶液 | c中有白色胶状沉淀生成 | H2CO3酸性大于H2SiO3 | 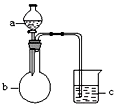 |
| B | 浓盐酸 | MnO2 | 石蕊 试液 | 石蕊试液先 变红后褪色 | 氯气具有漂白性 | |
| C | 稀硫酸 | 锌粒 | 水 | 一段时间有气泡 | 反应生成了H2 | |
| D | NaOH溶液 | Al | 水 | 产生大量气泡 | Al能与NaOH 溶液反应 |
| A. | A | B. | B | C. | C | D. | D |
6.下列各组物质中,前者为电解质,后者为非电解质的是( )
| A. | 硫酸,硫酸钡 | B. | NH3,氢氧化钠 | C. | 盐酸,醋酸 | D. | 食盐,酒精 |
13.在压强为2.20×104KPa、温度达到374℃时,水成为“超临界状态”,此时水可与CO2等含碳化合物反应生成有机物,这就是“水热反应”,生物质在地下高温高压条件下通过水热反应可生成石油、煤等矿物能源.下列说法不正确的是( )
| A. | “水热反应”是一种复杂的化学变化 | |
| B. | 二氧化碳与超临界水作用生成汽油的反应,属于放热反应 | |
| C. | 火力发电厂可望利用废热,将二氧化碳转变为能源物质 | |
| D. | 随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环 |
3.下列化学反应的速率,前者一定大于后者的是( )
| A. | 相同温度下,颗粒大小相同的锌粒分别与pH值相同的硫酸和盐酸反应 | |
| B. | A+B$\stackrel{500℃}{→}$C;D+E$\stackrel{100℃}{→}$F | |
| C. | 相同温度下,与同浓度盐酸反应的锌粒和铁粉 | |
| D. | G+H→W+Q(Q>0),其他条件相同时分别在200℃和100℃时反应 |
10.在一定温度下的密闭容器中,当下列物理量不再变化时,表明A(s)+2B(g)?C(g)+D(g)已达平衡的是( )
| A. | 混合气体的压强 | B. | C和D物质的量浓度相等 | ||
| C. | 混合气体的密度 | D. | 混合气体的总物质的量 |
6.下列气体可用向上排空气法收集的是( )
| A. | NH3 | B. | H2 | C. | Cl2 | D. | CH4 |
7.通常情况下,不能用铁制容器盛放的是( )
| A. | 浓硫酸 | B. | 盐酸 | C. | 汽油 | D. | 酒精 |