15. 乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:
乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:
①25℃时有关弱酸的电离常数如表:
②Ksp(CaCO3)=2.8×10-9.
请回答下列问题:
(1)用pH试纸检测NaCN溶液的酸碱性时,pH试纸变为蓝色.用离子方程式解释出现这种现象的原因:CN-+H2O?HCN+OH-.
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液的pH=6,则$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$=$\frac{1}{18}$.
(3)在任一浓度的NaHCO3溶液中.c(OH-)-c(H+)=(填“>”、“=”或“<”)c(H2CO3)-c(CO32-).
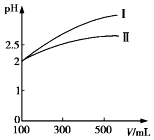
(4)体积均为100mL pH=2的CH3COOH溶液与HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶液的pH变化趋势的曲线是I(填“I”或“Ⅱ”).
(5)在容器中使氯化钙溶液与碳酸钠溶液等体积混合,己知碳酸钠溶液的浓度为2×l0-4mol/L,则生成沉淀所需氯化钙溶液的最小浓度为5.6×l0-5mol/L.
 乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:
乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:①25℃时有关弱酸的电离常数如表:
| 弱酸的化学式 | CH3COOH | HCN | H2CO3 |
| 电离常数 | Ka=l.8×l0-5 | Ka=4.9×10-10 | Kal=4.3×10-7 Ka2=5.6×10-11 |
请回答下列问题:
(1)用pH试纸检测NaCN溶液的酸碱性时,pH试纸变为蓝色.用离子方程式解释出现这种现象的原因:CN-+H2O?HCN+OH-.
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液的pH=6,则$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$=$\frac{1}{18}$.
(3)在任一浓度的NaHCO3溶液中.c(OH-)-c(H+)=(填“>”、“=”或“<”)c(H2CO3)-c(CO32-).
(4)体积均为100mL pH=2的CH3COOH溶液与HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶液的pH变化趋势的曲线是I(填“I”或“Ⅱ”).
(5)在容器中使氯化钙溶液与碳酸钠溶液等体积混合,己知碳酸钠溶液的浓度为2×l0-4mol/L,则生成沉淀所需氯化钙溶液的最小浓度为5.6×l0-5mol/L.
14.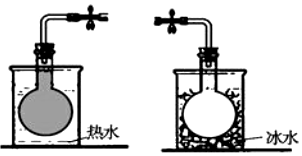 在密封的烧瓶中充入一定量的NO2,发生可逆反应:2NO2?N2O4.不同温度下烧瓶中气体的颜色深浅如图所示.下列有关说法正确的是( )
在密封的烧瓶中充入一定量的NO2,发生可逆反应:2NO2?N2O4.不同温度下烧瓶中气体的颜色深浅如图所示.下列有关说法正确的是( )
 在密封的烧瓶中充入一定量的NO2,发生可逆反应:2NO2?N2O4.不同温度下烧瓶中气体的颜色深浅如图所示.下列有关说法正确的是( )
在密封的烧瓶中充入一定量的NO2,发生可逆反应:2NO2?N2O4.不同温度下烧瓶中气体的颜色深浅如图所示.下列有关说法正确的是( )| A. | 该反应的正反应为吸热反应 | |
| B. | 反应达到平衡时,再充入少量NO2,平衡后NO2的转化率增大 | |
| C. | 反应达到平衡时,再充入少量N2O4,气体颜色变浅 | |
| D. | 反应达到平衡时,增大压强,平衡向正反应方向移动,逆反应速率减小 |
13.己知2NO+2H2=N2+2H2O分两步进行:(l)2NO+H2=N2+H2O2(很慢);(2)H2O2+H2=2H2O(很快).下列说法不正确的是( )
| A. | H2O2是中间产物,不是催化剂 | |
| B. | 总反应速率由反应(1)决定 | |
| C. | 用不同物质表示的反应速率,数值和含义都相同 | |
| D. | 加入高效催化剂,能降低反应的活化能 |
12.下列除去杂质(括号中的物质为杂质)的方法中,不正确的是( )
| A. | NH3气体(H2O):通过浓H2SO4干燥 | |
| B. | FeCl2溶液(FeCl3):加入铁粉,过滤 | |
| C. | CO气体(CO2):通过NaOH溶液洗气后干燥 | |
| D. | Cl2气体(HCl):通过饱和NaCl溶液洗气后干燥 |
11.不能正确表示下列反应的离子方程式是( )
| A. | Na与稀硫酸反应的离子方程式为2Na+2H+═2 Na++H2↑ | |
| B. | Na2O2溶于水产生O2:2Na2O2+2H2O=4Na++4OH-+O2↑ | |
| C. | 碳酸氢钙溶液中滴加氢氧化钠溶液至Ca2+恰好完全沉淀 Ca2++HCO3-+OH-=CaCO3↓+H2O | |
| D. | 饱和碳酸钠溶液中通入过量二氧化碳气体,溶液变浑浊CO32-+CO2+H2O=HCO3- |
10.下列说法不正确的是( )
| A. | 用胆矾炼铜、烧结粘土制陶瓷都涉及化学变化 | |
| B. | 中国古代利用明矾溶液的酸性清除铜镜表面的铜锈 | |
| C. | 食盐、醋酸、氨水和硫酸钡都是电解质 | |
| D. | 胶体区别其它分散系的本质特征是分散质微粒直径在lnm〜l00nm之间 |
9.相同温度下,相同物质的量浓度的下列溶质:①NaOH、②NH4Cl、③Na2SO4、④NaHSO4、⑤NH3•H2O,按 c(OH-)由大到小顺序排列正确的是( )
| A. | ⑤①③②④ | B. | ④②③①⑤ | C. | ①⑤③②④ | D. | ①⑤③④② |
8.下列关于 FeCl3水解的说法不正确的是( )
| A. | 水解达到平衡时(不饱和),加氯化铁溶液达饱和,溶液的酸性会增强 | |
| B. | 浓度为5 mol•L-1和0.5 mol•L-1的两种 FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者小 | |
| C. | 有50℃和20℃的同浓度的两种FeCl3稀溶液,其他条件相同时,Fe3+的水解程度前者比后者小 | |
| D. | 为抑制 Fe3+的水解,较好地保存 FeCl3溶液,应加少量盐酸 |
7.现有25℃的下列四种溶液,其中碱性最强的是( )
| A. | pH=11的溶液 | B. | 4 g NaOH溶于水形成1L的水溶液 | ||
| C. | c(OH-)=0.12 mol•L-1 | D. | c(H+)=1×10-10 mol•L-1的溶液 |
6.造成西安雾霾的重要原因之一是汽车尾气,已知汽车尾气无害化处理的反应之一为 2NO(g)+2CO(g)?N2(g)+2CO2(g)△H<0,下列说法正确的是( )
0 161476 161484 161490 161494 161500 161502 161506 161512 161514 161520 161526 161530 161532 161536 161542 161544 161550 161554 161556 161560 161562 161566 161568 161570 161571 161572 161574 161575 161576 161578 161580 161584 161586 161590 161592 161596 161602 161604 161610 161614 161616 161620 161626 161632 161634 161640 161644 161646 161652 161656 161662 161670 203614
| A. | 升高温度可以提高NO和CO的转化率 | |
| B. | 使用高效催化剂可以提高NO和CO的转化率 | |
| C. | 反应达到平衡后,NO 的生成速率和消耗速率相等 | |
| D. | 若该反应已达到平衡状态,增大压强(通过减小体积实现)对平衡无影响 |