10.在一定条件下,既能与CO2反应,又能跟SiO2 反应的物质( )
①NaHCO3溶液 ②浓硫酸 ③NaOH溶液 ④碳.
①NaHCO3溶液 ②浓硫酸 ③NaOH溶液 ④碳.
| A. | ①② | B. | ①③ | C. | ②④ | D. | ③④ |
9.短周期主族元素X、Y、Z、W的原子序数依次增大,X元素原子最外层电子数是内层的2倍,Z是地壳中含量最高的元素,W是同周期原子半径最大的金属元素.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(W)>r(Z)>r(Y) | |
| B. | X的最高价氧化物对应水化物的酸性比Y的强 | |
| C. | Z的简单气态氢化物的热稳定性比Y的强 | |
| D. | Z分别与X、W形成的化合物的化学键类型相同 |
8.分子式为C5H12O的醇有多种结构,其中能发生催化氧化生成醛的结构有(不考虑立体异构)( )
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
7.某校化学实验小组对电化学问题进行了如图所示实验探究.
探究一:探究弱酸性条件下铁发生电化学腐蚀类型的影响因素.将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
(1)请完成以下实验设计表(表中不要留空格):
(2)编号①实验测得容器中的压强随时间的变化如图(2)所示.t2时,容器中压强明显小于起始压强,其原因是铁发生了吸氧 腐蚀,请在图(3)中用箭头标出发生该腐蚀时电子的流动方向;此时,炭粉表面发生的电极反应式是O2+2H2O+4e-═4OH-.
(3)该小组对图(2)中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:反应放热使锥形瓶内温度升高;
探究二:探究电解现象
利用图2装置做电解50mL 0.5mol•L-1CuCl2溶液的实验.
实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的淀粉碘化钾试纸先变蓝后褪色(提示:Cl2氧化性大于IO3-);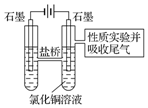
B.电解一段时间以后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体.
(4))分析实验记录A中试纸颜色变化,用离子方程式解释:
①2I-+Cl2=I2+2Cl-;
②5Cl2+I2+6H2O=10Cl-+2IO3-+12H+.
(5)分析实验记录B中浅蓝色固体可能是Cu(OH)2(写化学式),试分析生成该物质的原因(用必要的文字和化学用语解释)电解较长时间后,铜离子浓度下降,氢离子开始放电,溶液的PH增大,铜离子转化为氢氧化铜沉淀.
探究一:探究弱酸性条件下铁发生电化学腐蚀类型的影响因素.将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.

(1)请完成以下实验设计表(表中不要留空格):
| 编号 | 实验目的 | 碳粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.5 | 90.0 |
| ② | ? | 0.5 | 2.5 | 36.0 |
| ③ | 碳粉质量的影响 | 0.2 | ? | 90.0 |
(3)该小组对图(2)中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
假设一:发生析氢腐蚀产生了气体;
假设二:反应放热使锥形瓶内温度升高;
探究二:探究电解现象
利用图2装置做电解50mL 0.5mol•L-1CuCl2溶液的实验.
实验记录:
A.阳极上有黄绿色气体产生,该气体使湿润的淀粉碘化钾试纸先变蓝后褪色(提示:Cl2氧化性大于IO3-);

B.电解一段时间以后,阴极表面除有铜吸附外,还出现了少量气泡和浅蓝色固体.
(4))分析实验记录A中试纸颜色变化,用离子方程式解释:
①2I-+Cl2=I2+2Cl-;
②5Cl2+I2+6H2O=10Cl-+2IO3-+12H+.
(5)分析实验记录B中浅蓝色固体可能是Cu(OH)2(写化学式),试分析生成该物质的原因(用必要的文字和化学用语解释)电解较长时间后,铜离子浓度下降,氢离子开始放电,溶液的PH增大,铜离子转化为氢氧化铜沉淀.
5.已知同温同压下,下列反应的焓变和平衡常数分别表示为
(1)2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ•mol-1 K1=a
(2)2NO(g)+O2(g)?2NO2(g)△H2=-144kJ•mol-1 K2=b
(3)NO2(g)+SO2(g)?SO3(g)+NO(g)△H3=-m kJ•mol-1 K3=c
下列说法正确的是( )
(1)2SO2(g)+O2(g)?2SO3(g)△H1=-197kJ•mol-1 K1=a
(2)2NO(g)+O2(g)?2NO2(g)△H2=-144kJ•mol-1 K2=b
(3)NO2(g)+SO2(g)?SO3(g)+NO(g)△H3=-m kJ•mol-1 K3=c
下列说法正确的是( )
| A. | m=53 c2=a/b | B. | m=-26.5 2c=a-b | C. | m=-170.5 2c=a-b | D. | m=26.5 c2=$\frac{a}{b}$ |
4.下列有关电化学装置的说法正确的是( )
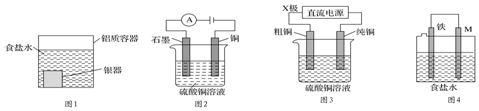

| A. | 用图1装置处理银器表面的黑斑(Ag2S),银器表面发生的反应为Ag2S+2e-═2Ag+S2-,该过程中总反应为2Al+3Ag2S═6Ag+Al2S3 | |
| B. | 用图2装置电解一段时间后,铜电极部分溶解,溶液中铜离子的浓度基本不变 | |
| C. | 图3装置中若直流电源的X极为正极,则该装置可实现粗铜的电解精炼 | |
| D. | 图4装置中若M是铜,则该装置能防止铁被腐蚀 |
3. 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )
 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )| A. | 从曲线变化可以看出,反应进行到10min至20min时可能采取的措施是使用了催化剂 | |
| B. | 25min时平衡正向移动但达到新平衡后 NH3的体积分数比原平衡大 | |
| C. | 反应开始到第一次平衡时,N2的平均反应速率为0.0625mol•(L•min)-1,H2的转化率为75% | |
| D. | 从曲线变化可以看出,反应进行至25min时,采取的措施是分离出0.1mol的氨气,平衡正向移动 |
2.下列说法正确的是( )
0 161419 161427 161433 161437 161443 161445 161449 161455 161457 161463 161469 161473 161475 161479 161485 161487 161493 161497 161499 161503 161505 161509 161511 161513 161514 161515 161517 161518 161519 161521 161523 161527 161529 161533 161535 161539 161545 161547 161553 161557 161559 161563 161569 161575 161577 161583 161587 161589 161595 161599 161605 161613 203614
| A. | 已知CH3OH(l)的燃烧热为238.6 kJ•mol-1,则CH3OH(l)+$\frac{3}{2}$O2(g)═CO2(g)+2H2O(g)△H=-238.6 kJ•mol-1 | |
| B. | 钢铁水闸可用牺牲阳极或外加电流的阴极保护法防止其腐蚀 | |
| C. | 反应H2+Cl2═2HCl(△H<0)的机理包含①Cl2-→2Cl(慢),②H2+Cl-→HCl+H(快),③Cl2+H-→HCl+Cl(快),则反应①的活化能小于反应②的活化能 | |
| D. | 一定条件下反应N2+3H2?2NH3达到平衡时,3v正(H2)=2v逆(NH3) |
 (1)下列事实不能说明醋酸是弱酸的是①③
(1)下列事实不能说明醋酸是弱酸的是①③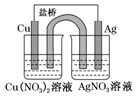 (3)某同学用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)设计成一个原电池,如图所示,下列判断中正确的是d.
(3)某同学用铜片、银片、Cu(NO3)2溶液、AgNO3溶液、导线和盐桥(装有琼脂-KNO3的U形管)设计成一个原电池,如图所示,下列判断中正确的是d.