6.镁-次氯酸盐燃料电池的工作原理如图所示,该电池反应为:Mg+ClO-+H2O=Mg(OH)2+Cl-,下列有关说法正确的是( )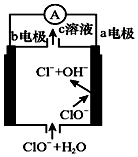

| A. | 电池工作时,c溶液中的溶质一定是MgCl2 | |
| B. | 负极反应式:ClO--2e-+H2O=Cl-+2OH- | |
| C. | 电池工作时,OH-向b电极移动 | |
| D. | b电极发生还原反应,每转移0.1 mol电子,理论上生成0.1 mol Cl- |
4.化学与生产、生活、社会密切相关,下列说法正确的是( )
| A. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒 | |
| B. | 小苏打是制作面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂 | |
| C. | 浓硫酸可刻蚀石英制艺术品 | |
| D. | 煤经过气化和液化等物理变化可以转化为清洁燃料 |
3.25℃时,下列溶液中各离子的浓度关系不正确的是( )
| A. | 等体积、等浓度的K2CO3溶液与盐酸混合,则混合液中:c(K+)>c(Cl-)>c(HCO3-)>c(OH-)>c(H+) | |
| B. | 向氨水中滴加盐酸至中性,则溶液中:c(NH4+)=c(Cl-)>c(OH-)=c(H+) | |
| C. | 等体积、等浓度的CH3COOH溶液与NaOH溶液混合后,溶液的pH=8,则c(OH-)-c(CH3COOH)=1×10-8mol•L-1 | |
| D. | 等体积、等浓度①NaCl、②CH3COONa、③NaClO溶液中离子总数大小顺序:③>②>① |
2.下列有关电化学装置的说法正确的是( )
| A. |  用如图装置处理银器表面的黑斑(Ag2S),银器表面发生的反应为Ag2S+2e-═2Ag+S2- | |
| B. |  如图装置电解一段时间后,铜电极部分溶解,溶液中通离子的浓度基本不变 | |
| C. |  如图装置中若直流电源的X极为负极,则该装置可实现粗铜的电解精炼 | |
| D. |  如图,图中若M是铜,则该装置能防止铁被腐蚀 |
1.鉴别苯酚溶液、已烯和甲苯,可选用的最佳试剂( )
| A. | 溴水 | B. | FeCl3溶液 | C. | 新制Cu(OH)2悬浊液 | D. | 酸性KMnO4溶液 |
20.某温度下,在固定容积的容器中,可逆反应A(g)+3B(g)?2C(g)达到平衡,此时测得n(A):n(B):n(C)=2:2:1.若保持温度不变,以n(A):n(B):n(C)=2:2:1的比例向该容器中再充入A、B和C,下列叙述正确的是( )
| A. | 刚充入时反应速率υ正减少,υ逆增大 | |
| B. | 平衡向正反应方向移动 | |
| C. | 平衡向逆反应方向移动 | |
| D. | 物质C的质量分数增大 |
19.下列离子方程式,书写正确的是( )
| A. | 用惰性电极电解熔融氯化钠:2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$Cl2↑+H2↑+2OH- | |
| B. | 铁粉溶于稀硫酸:2Fe+6H+═2Fe3++3H2↑ | |
| C. | 用 CuSO4溶液吸收 H2S:Cu2++H2S═CuS↓+2H+ | |
| D. | 向 NH4HSO4 溶液中滴加少量的 Ba(OH)2溶液:Ba2++2OH-+NH+H2O+H++SO2-═BaSO4↓+NH3•H2O |
18.25℃时,下列溶液中有关微粒的物质的量浓度关系错误的是( )
| A. | pH=4的0.1mol/L NaHA溶液:c(HA-)>c(H+)>c(A2-)>c(OH-)>c(H2A) | |
| B. | 10mL 0.1mol/L CH3COOH溶液与20mL 0.1mol/L NaOH溶液混合后,溶液中离子浓度关系:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH) | |
| C. | 两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1<10c2 | |
| D. | 已知:HA为弱酸,则两种溶液①0.1mol/LHA溶液;②0.3mol/LHA溶液与0.1mol/LNaOH溶液等体积的混合液,c(H+)①>② |
17.在盛放浓硫酸的试剂瓶标签上应该印有下列警示标记中的( )
0 161227 161235 161241 161245 161251 161253 161257 161263 161265 161271 161277 161281 161283 161287 161293 161295 161301 161305 161307 161311 161313 161317 161319 161321 161322 161323 161325 161326 161327 161329 161331 161335 161337 161341 161343 161347 161353 161355 161361 161365 161367 161371 161377 161383 161385 161391 161395 161397 161403 161407 161413 161421 203614
| A. |  爆炸品 | B. |  易燃液体 | C. |  剧毒品 | D. |  腐蚀品 |