12.某有机物的红外光谱表明有O-H键和C-H键,核磁共振氢谱有两组吸收峰,峰面积之比为2:1,该有机物可能是( )
| A. | CH2=CH-CH=CH2 | B. | HOCH2-CH2OH | C. | 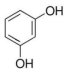 | D. | HCOOH |
11.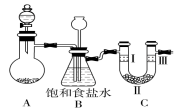 某学习小组围绕氯气设计了一系列实验.
某学习小组围绕氯气设计了一系列实验.
(1)用如图装置A制备氯气.选用的药品为漂粉精固体和浓盐酸,相关的化学方程式为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除氯气中的氯化氢;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗下端导管中液面会上升,形成水柱.
(3)为检验氯气是否具有漂白性,使氯气依次通过Ⅰ、Ⅱ、Ⅲ三种物质,物质的顺序正确的是D.
(4)为了进一步比较氧化性强弱,将一定量氯气通入溴化亚铁溶液后,再加入四氯化碳,振荡,静置,整个过程中肯定能观察到的现象是A.
A.水层显棕黄色 B.水层无色C.四氯化碳层显红棕色 D.四氯化碳层无色
(5)查阅资料后小组发现,氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中的I-选择了价格并不便宜的亚硝酸钠,排除环境方面的因素,可能的原因是:氯气、浓硝酸、酸性高锰酸钾等氧化性太强,还能继续氧化碘单质.
(6)有人提出,工业上为防止污染空气,可用足量的Na2SO3溶液吸收余氯,试写出相应的离子方程式:Cl2+SO32-+H2O=SO42-+2H++Cl-.判断改用NaHSO3溶液是否可行:否(填“是”或“否”).
 某学习小组围绕氯气设计了一系列实验.
某学习小组围绕氯气设计了一系列实验.(1)用如图装置A制备氯气.选用的药品为漂粉精固体和浓盐酸,相关的化学方程式为Ca(ClO)2+4HCl(浓)═CaCl2+2Cl2↑+2H2O.
(2)装置B中饱和食盐水的作用是除氯气中的氯化氢;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:B中长颈漏斗下端导管中液面会上升,形成水柱.
(3)为检验氯气是否具有漂白性,使氯气依次通过Ⅰ、Ⅱ、Ⅲ三种物质,物质的顺序正确的是D.
| A | B | C | D | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
A.水层显棕黄色 B.水层无色C.四氯化碳层显红棕色 D.四氯化碳层无色
(5)查阅资料后小组发现,氯气、浓硝酸、酸性高锰酸钾等都是常用的强氧化剂,但工业上氧化卤水中的I-选择了价格并不便宜的亚硝酸钠,排除环境方面的因素,可能的原因是:氯气、浓硝酸、酸性高锰酸钾等氧化性太强,还能继续氧化碘单质.
(6)有人提出,工业上为防止污染空气,可用足量的Na2SO3溶液吸收余氯,试写出相应的离子方程式:Cl2+SO32-+H2O=SO42-+2H++Cl-.判断改用NaHSO3溶液是否可行:否(填“是”或“否”).
7.近日,科学研究发现液态水或存在第二形态,当水被加热到40℃~60℃之间时,它的导热性、折射率、导电性等属性也会发生改变.下列说法正确的是( )
| A. | 氢氧两种元素只能组成H2O | |
| B. | 导热性等属于水的化学性质 | |
| C. | 0℃时冰的密度比液态水的密度小 | |
| D. | 液态水两种形态间转化需断裂O-H键 |
5.25℃时,浓度均为 0.1mol•L-1 的 HA 溶液和 BOH 溶液,pH 分别是 1 和 11.下列说法正确的是( )
| A. | BOH 溶于水,其电离方程式是 BOH═B++OH- | |
| B. | 在 0.1 mol•L-1 BA 溶液中,c(B+)>c(A-)>c(OH-)>c(H+) | |
| C. | 若一定量的上述两溶液混合后 pH=7,则 c(A- )=c(B+ ) | |
| D. | 若将 0.1 mol•L-1 BOH 溶液稀释至 0.001 mol•L-1,则溶液的 pH=9 |
4.某酸性工厂废水中含有浓度约为0.01mol•L-1的Ag+、Pb2+等重金属离子,已知:Ksp(AgOH)=5.6×10-8;Ksp[Pb(OH)2]=1.2×10-15;某工程师用CaO处理上述废水,最终溶液的pH=8,处理后废水中c(Pb2+)是( )
| A. | 1.2×10-3mol•L-1 | B. | 1.2×10-9mol•L-1 | C. | 2.4×10-5mol•L-1 | D. | 3.2×10-6mol•L-1 |
3.用指定材料做阳极和阴极来电解一定浓度的溶液甲,然后加入物质乙能使溶液物质为甲溶液原来的浓度,则合适的组合是( )
0 161128 161136 161142 161146 161152 161154 161158 161164 161166 161172 161178 161182 161184 161188 161194 161196 161202 161206 161208 161212 161214 161218 161220 161222 161223 161224 161226 161227 161228 161230 161232 161236 161238 161242 161244 161248 161254 161256 161262 161266 161268 161272 161278 161284 161286 161292 161296 161298 161304 161308 161314 161322 203614
| 阳极 | 阴极 | 溶液甲 | 物质乙 | |
| A | Pt | Pt | NaOH | NaOH固体 |
| B | Pt | Pt | H2SO4 | H2O |
| C | Pt | Pt | NaCl | NaOH |
| D | 粗铜 | 精铜 | CuSO4 | Cu(OH)2 |
| A. | A | B. | B | C. | C | D. | D |
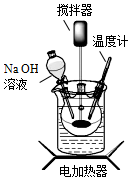 超细Fe3O4粉体可制成磁流体,一种制备超细Fe3O4粉体的实验步骤如下:
超细Fe3O4粉体可制成磁流体,一种制备超细Fe3O4粉体的实验步骤如下:
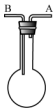 利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr
利用如图装置收集以下气体:①H2、②Cl2、③CH4、④HCl、⑤HBr