11.通常人们把拆开1mol某化学键所吸收的能量或形成1mol某化学键所释放的能量看成该化学键的键能.已知热化学方程式:N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol,请根据热化学方程式和表中数据计算:H-N键的键能x约为( )
| 化学键 | H-H | N≡N | H-N |
| 键能 | 436kJ/mol | 946kJ/mol | x |
| A. | 391kJ/mol | B. | 431kJ/mol | C. | 349kJ/mol | D. | 469kJ/mol |
9.下列各组物质相互混合反应,既有气体生成,最终又一定有沉淀生成是( )
①金属钠投入FeCl3溶液中 ②少量电石投入过量碳酸氢钠溶液中
③过氧化钠投入AlCl3溶液中 ④碳酸钠投入明矾溶液中.
①金属钠投入FeCl3溶液中 ②少量电石投入过量碳酸氢钠溶液中
③过氧化钠投入AlCl3溶液中 ④碳酸钠投入明矾溶液中.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
8.化学与材料、生活和环境密切相关,下列有关分类中正确的是( )
| A. | 新型材料聚酯纤维、光导纤维都属于有机高分子 | |
| B. | 火柴头的主要成分是氯酸钾和硫单质,分别属于电解质和非电解质 | |
| C. | 蛋白质、淀粉、纤维素都属于有机高分子化合物 | |
| D. | 天然纤维和合成纤维的主要成分是纤维素 |
7.下列有关甲烷、乙烯、苯的说法正确的是( )
| A. | 1mol甲烷和1mol氯气在光照条件下充分反应,生成1mol CH3Cl | |
| B. | 等物质的量的乙烯与碳酸二甲酯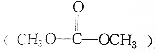 完全燃烧耗氧量相同 完全燃烧耗氧量相同 | |
| C. | 苯和液溴在FeCl3的催化作用下发生加成反应 | |
| D. | 苯在工业上可通过石油分馏得到 |
6.有一真空瓶充入空气后质量为m1,在相同状况下,若改为充入某气体A时,总质量为m2,且m2>m1,则气体A可能是( )
| A. | H2 | B. | N2 | C. | O2 | D. | CO |
5.下列说法中,正确的是( )
| A. | 苯不与溴水反应,但苯能从溴水中提取溴单质 | |
| B. | 苯在一定条件下能发生加成反应和取代反应,但不能发生氧化反应 | |
| C. | 苯和乙烯都能使酸性KMnO4溶液褪色 | |
| D. | 苯在一定条件下与氢气、硝酸等发生加成反应 |
4.下列说法或表示方法正确的是( )
| A. | HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(s);△H=-26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | 由C(石墨)═C(金刚石)△H=1.90 kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 在100 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
2.用酸性氢氧燃料电池为电源进行电解的实验装置示意图如图所示.下列说法正确的是( )

0 161102 161110 161116 161120 161126 161128 161132 161138 161140 161146 161152 161156 161158 161162 161168 161170 161176 161180 161182 161186 161188 161192 161194 161196 161197 161198 161200 161201 161202 161204 161206 161210 161212 161216 161218 161222 161228 161230 161236 161240 161242 161246 161252 161258 161260 161266 161270 161272 161278 161282 161288 161296 203614

| A. | 燃料电池工作时,正极反应为O2+2H2O+4e-═4OH- | |
| B. | 此装置用于铁表面镀铜时,a为铁b为Cu,工作一段时间要使右池溶液复原可加入适量的CuO | |
| C. | a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 | |
| D. | 若a、b两极均为石墨时,在相同条件下,a极产生的气体与电池中消耗的H2体积相同 |