题目内容
4.下列说法或表示方法正确的是( )| A. | HI(g)?$\frac{1}{2}$H2(g)+$\frac{1}{2}$I2(s);△H=-26.5kJ/mol,由此可知1mol HI在密闭容器中分解后可以放出26.5kJ的能量 | |
| B. | 在稀溶液中,H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | 由C(石墨)═C(金刚石)△H=1.90 kJ•mol-1可知,金刚石比石墨稳定 | |
| D. | 在100 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ•mol-1 |
分析 A.为可逆反应,1molHI不能完全分解;
B.生成1molH2O(l)放出热量为57.3kJ,浓硫酸稀释放热;
C.由C(石墨)═C(金刚石)△H=1.90 kJ•mol-1可知,石墨能量低;
D.在100 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,可知1molH2完全燃烧生成液态水,放出285.8 kJ热量.
解答 解:A.为可逆反应,1molHI不能完全分解,放出热量小于26.5kJ,故A错误;
B.生成1molH2O(l)放出热量为57.3kJ,浓硫酸稀释放热,则含0.5 mol H2SO4的浓硫酸与含1mol NaOH的溶液混合,放出的热量大于57.3 kJ,故B正确;
C.由C(石墨)═C(金刚石)△H=1.90 kJ•mol-1可知,石墨能量低,可知石墨比金刚石稳定,故C错误;
D.在100 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,可知1molH2完全燃烧生成液态水,放出285.8 kJ热量,则H2燃烧的热化学方程式为H2(g)+$\frac{1}{2}$O2(g)═H2O(l)△H=-285.8 kJ•mol-1,故D错误;
故选B.
点评 本题考查反应热与焓变,为高频考点,把握反应中能量变化、中和热、燃烧热为解答的关键,侧重分析与应用能力的考查,注意选项D为易错点,题目难度不大.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
14.含有两个碳原子的部分有机物如下,有关判断错误的是( )
①CH3CH3②CH2═CH2③CH2═CHCl④CH3CH2OH⑤CH3COOH⑥HCOOCH3.
①CH3CH3②CH2═CH2③CH2═CHCl④CH3CH2OH⑤CH3COOH⑥HCOOCH3.
| A. | 能发生取代反应的只有①、④和⑤ | |
| B. | 能与H2发生加成反应的只有②和③ | |
| C. | 所有原子位于同一平面的只有②和③ | |
| D. | 能发生水解反应生成两种有机物的只有⑥ |
15.下列各组的两种物质在溶液中的反应,可用同一离子方程式表示的是( )
| A. | 石灰石与硝酸反应;石灰石与盐酸 | |
| B. | BaCl2溶液与Na2SO4溶液;Ba(OH)2溶液与H2SO4溶液 | |
| C. | Na2CO3溶液与硝酸溶液;CaCO3溶液与硝酸溶液 | |
| D. | 氢氧化钠与盐酸,;氢氧化钠与碳酸 |
12.已知,常温常压下,过氧化钠(N2O2)是一种固体.标准状况下,等物质的量的N2O2和O2中相同的是( )
| A. | 两种物质中所含的氧原子数 | B. | 两种物质中所含的氧分子数 | ||
| C. | 两种物质的体积 | D. | 两种物质的质量 |
9.下列各组物质相互混合反应,既有气体生成,最终又一定有沉淀生成是( )
①金属钠投入FeCl3溶液中 ②少量电石投入过量碳酸氢钠溶液中
③过氧化钠投入AlCl3溶液中 ④碳酸钠投入明矾溶液中.
①金属钠投入FeCl3溶液中 ②少量电石投入过量碳酸氢钠溶液中
③过氧化钠投入AlCl3溶液中 ④碳酸钠投入明矾溶液中.
| A. | ①②③ | B. | ②③④ | C. | ①②④ | D. | ①③④ |
16.化学在生活中有着广泛的应用,下列对应关系错误的是( )
| 化学性质 | 实际应用 | |
| A. | 三价铁比二价铜氧化性强 | FeCl3腐蚀Cu刻制印刷电路板 |
| B. | 次氯酸盐具有氧化性 | 次氯酸钙可做漂白剂 |
| C. | 稀硝酸可与银反应 | 稀硝酸可除去试管内壁的银镜 |
| D. | HF能与Si反应 | 氢氟酸在玻璃器皿上刻蚀标记 |
| A. | A | B. | B | C. | C | D. | D |
14.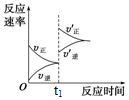 如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )
如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )
 如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )
如图为化学反应3A(g)?B(g)+C(g),△H<0在一密闭容器中反应的速率-时间图,下列叙述符合此图所给信息的是( )| A. | t1 时,向容器中通入一定量的A气体 | |
| B. | t1 时,缩小容器的体积 | |
| C. | t1 时,升高体系温度 | |
| D. | 从t1 开始到新的平衡的过程中,平衡向逆反应方向移动 |
 .
.