8.${\;}_{235}^{92}$U是重要的工业原料,铀浓缩一直为国际社会关注.下列说法正确的是( )
| A. | ${\;}_{235}^{92}$U原子核中含有 92 个中子 | |
| B. | ${\;}_{235}^{92}$U原子核外有 143 个电子 | |
| C. | ${\;}_{235}^{92}$U 与 ${\;}_{92}^{238}$U 互为同位素 | |
| D. | ${\;}_{235}^{92}$U与${\;}_{92}^{238}$U 同一核素 |
7.具备基本的化学实验技能是进行科学探究的基础和保证.下列有关实验操作正确的 是( )
| A. |  点燃酒精灯 | B. | 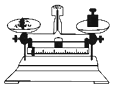 称量固体 | C. |  液体加热 | D. |  量取9.0mL液体 |
6.下列叙述Ⅰ和Ⅱ均正确并且有因果关系的是( )
| 选项 | 叙述Ⅰ | 叙述Ⅱ |
| A | 浓硝酸和稀硝酸都具有强氧化性 | 浓硝酸和稀硝酸均可使紫色石蕊试液先变红后褪色 |
| B | 浓硫酸具有强氧化性和吸水性 | 浓硫酸可干燥H2和CO,不可干燥 SO2和NH3 |
| C | SO2是酸性氧化物 | SO2可使含有酚酞的NaOH溶液褪色 |
| D | 铵盐受热易分解 | NH4Cl和NH4HCO3均可用作氮肥和制取氨气 |
| A. | A | B. | B | C. | C | D. | D |
5.设NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 0.5 mol Al与足量盐酸反应转移电子数为NA | |
| B. | 标准状况下,22.4 L氨气与22.4 L氮气所含原子数均为2 NA | |
| C. | 7.8gNa2O2所含的离子数为0.3NA | |
| D. | 11.2LCl2完全溶于NaOH溶液,电子转移数为0.5 NA |
2.醋酸的下列性质中,可以证明它是弱电解质的是( )
①白醋中滴入石蕊试液呈红色
②室温时,0.1mol/L醋酸溶液的pH约为3
③10mL 1mol/L醋酸恰好与10mL 1mol/L NaOH溶液完全反应
④常温下,测得醋酸钠溶液的pH>7
⑤醋酸溶液的导电性比强酸溶液的弱
⑥常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4.
①白醋中滴入石蕊试液呈红色
②室温时,0.1mol/L醋酸溶液的pH约为3
③10mL 1mol/L醋酸恰好与10mL 1mol/L NaOH溶液完全反应
④常温下,测得醋酸钠溶液的pH>7
⑤醋酸溶液的导电性比强酸溶液的弱
⑥常温下,将pH=1的醋酸溶液稀释1000倍,测得pH<4.
| A. | ②④⑤⑥ | B. | ①②④ | C. | ②④⑥ | D. | ②⑥ |
1.由水电离产生的[H+]=10-13mol/L的溶液中,一定可以大量共存的离子组是( )
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、Mg2+、HCO3- | ||
| C. | NO3-、Na+、K+、Cl- | D. | NO3-、K+、[Al(OH)4]-、OH- |
20.下列有关说法正确的是( )
| A. | CaCO3(s)=CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△S<0 | |
| B. | 镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 | |
| C. | N2(g)+3H2(g)?2NH3(g)△H<0,其他条件不变时升高温度,氢气的反应速率和转化率均增大 | |
| D. | 水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
19.已知充分燃烧a g乙炔(C2H2)气体时生成2mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧热的热化学方程式正确的是( )
0 161051 161059 161065 161069 161075 161077 161081 161087 161089 161095 161101 161105 161107 161111 161117 161119 161125 161129 161131 161135 161137 161141 161143 161145 161146 161147 161149 161150 161151 161153 161155 161159 161161 161165 161167 161171 161177 161179 161185 161189 161191 161195 161201 161207 161209 161215 161219 161221 161227 161231 161237 161245 203614
| A. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-2b kJ/mol | |
| B. | C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-b kJ/mol | |
| C. | 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l)△H=-4b kJ/mol | |
| D. | C2H2(g)+$\frac{5}{2}$O2(g)=2CO2(g)+H2O(l)△H=-2b kJ/mol |
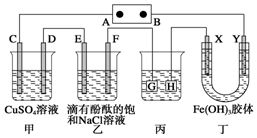 如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.
如图装置所示,C、D、E、F、X、Y都是惰性电极,甲、乙中溶液的体积和浓度都相同(假设通电前后溶液体积不变),A、B为外接直流电源的两极.将直流电源接通后,F极附近呈红色.