8.设NA为阿伏伽德罗常数的数值,下列说法正确的是( )
| A. | 标准状况下,11.2L SO3中含有的分子数为0.5NA | |
| B. | 常温下,46gNO2和N2O4的混合气体中含有原子总数为3NA | |
| C. | 1mol C10H22含共价键数目32NA | |
| D. | 1L 2mol/L的MgCl2溶液中含Mg2+数为2NA |
7.氢化铝钠由于具有储氢性能而备受关注,它可用氢化物、铝、高压氢在烃或醚溶剂中反应制得:2NaH+2Al+3H2=2NaAlH4.下列说法正确的是( )
| A. | NaAH4中氢元素的化合价为+1价 | |
| B. | 若有1 mol NaAl4生成,则转移4 mol电子 | |
| C. | 反应中氧化剂与还原剂的物质的量之比为3:2 | |
| D. | 氢化铝钠溶于水时除有气泡产生外,还有大量的白色沉淀生成 |
6.亚氨基锂(Li2NH)时一种储氢容量大,安全性好的固体储氢材料,其储氢原理可表示为:Li2NH+H2=LiNH2+LiH.下列有关说法正确的是( )
| A. | Li+和H+的离子半径相等 | B. | 此法储氢和钢瓶储氢的原理相同 | ||
| C. | 金属锂在空气中燃烧生成Li2O2 | D. | 该反应中H2既是氧化剂又是还原剂 |
5.某化学兴趣趣小组为探究Cl2、Br2、Fe3+的氧化性强弱,设计了如下实验:
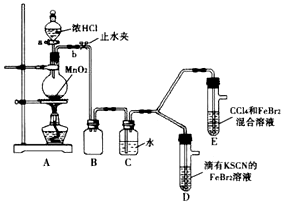
(1)①A装置中圆底烧瓶中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↓+2H2O;
②检查气体发生装置 A的气密性的操作是:关闭止水夹b,打开活塞a,向分液漏斗中注水,若水不能顺利流下,则气密性良好.
③装置B的作用是安全瓶,防止液体倒吸
(2)整套实验装置存在一处明显不足,请指出缺少尾气处理装置.
用改正后的装置进行实验.实验过程如表:
(3)因忙于观察和记录,没有及时停止反应,D、E中均发生了新的变化:
D装置中:红色慢慢褪去
E装置中:CCl4层先由无色变为橙色,后颜色逐渐变成红色.
为探究上述实验现象的本质,小组同学查得资料如表:
①请用平衡移动原理(结合化学用语) 解释Cl2过量时D中溶液红色褪去的原因过量氯气和SCN-反应2SCN-+Cl2=2Cl-+(SCN)2,使SCN-浓度减小,则使Fe3++3SCN-?Fe(SCN)3平衡向逆反应方向移动而褪色.
②欲探究E中颜色变化的原因,设计实验如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生,请结合化学用语解释仅产生白色沉淀的原因BrCl+H2O=HBrO+HCl反应产生Cl-,没有Br-生成,由于AgBrO易溶于水,加入AgNO3溶液,只能生成AgCl沉淀.

(1)①A装置中圆底烧瓶中发生反应的离子方程式为MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↓+2H2O;
②检查气体发生装置 A的气密性的操作是:关闭止水夹b,打开活塞a,向分液漏斗中注水,若水不能顺利流下,则气密性良好.
③装置B的作用是安全瓶,防止液体倒吸
(2)整套实验装置存在一处明显不足,请指出缺少尾气处理装置.
用改正后的装置进行实验.实验过程如表:
| 实验操作 | 实验现象 | 结论 |
| 打开活塞a,向圆底烧瓶中滴入适置浓盐酸,然后关闭活塞a,点燃酒精灯 | D装罝中:溶液变红,E装置中:水层溶液变黄,振荡后CCl4层无明显变化 | Cl2、Br2、Fe2+的氧化性由强到弱的顺序为Cl2>Br2>Fe3+ |
D装置中:红色慢慢褪去
E装置中:CCl4层先由无色变为橙色,后颜色逐渐变成红色.
为探究上述实验现象的本质,小组同学查得资料如表:
| i.(SCN)2性质与卤素单质类似.氧化性:Cl2>(SCN)2 ii.Cl2和Br2反应生成BrCl,它呈红色(略带黄色)沸点约为5℃,与水发生水解反应 iii.AgClO、AgBrO均可溶于水 |
②欲探究E中颜色变化的原因,设计实验如下:
用分液漏斗分离出E的下层溶液,蒸馏、收集红色物质,取少量,加入AgNO3溶液,结果观察到仅有白色沉淀产生,请结合化学用语解释仅产生白色沉淀的原因BrCl+H2O=HBrO+HCl反应产生Cl-,没有Br-生成,由于AgBrO易溶于水,加入AgNO3溶液,只能生成AgCl沉淀.
4.能正确表示下列反应的离子方程式是( )
| A. | 钾与CuSO4溶液反应:2K++Cu2+═Cu+2K+ | |
| B. | 向Mg(HCO3)2溶液中加入过量的NaOH溶液:Mg2++2HCO3-+4OH-═Mg (OH)2↓+2CO32-↑+2H2O | |
| C. | 向NaHSO4溶液中滴入少量Ba (OH)2溶液:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 浓盐酸与铁屑反应:2Fe+6H+═2Fe3++3H2↑ |
3.关于下列词句或谚语,说法不正确的是( )
| A. | “水乳交融,火上浇油”前者包含物理变化,而后者包含化学变化 | |
| B. | “曾青得铁化为铜”发生了置换反应 | |
| C. | “春蚕到死丝方尽”中的“丝”的和“慈母手中线,游子身上衣”中的棉“线”主要成分都是纤维素 | |
| D. | “卤水点豆腐,一物降一物”的前半句话与胶体知识有关 |
2.用NA表示阿伏加德罗常数的数值.下列叙述正确的是( )
| A. | 6.4 g SO2与足量氧气反应生成SO3时,转移的电子数为0.2NA | |
| B. | 1 mol氯气与足量FeI2溶液反应时,转移的电子数为2NA | |
| C. | 标准状况下,5.6 L NO和5.6 LO2混合后的气体中含有的分子数为0.5NA | |
| D. | 50 mL 18.4mol/L浓硫酸与足量铜微热反应,生成SO2的分子数为0.46NA |
1.化学在生产生活中有着广泛的应用,下列对应关系错误的是( )
| 选项 | 化学性质 | 实际应用 |
| A | 浓硫酸有脱水性 | 浓硫酸作干燥剂 |
| B | Cu能与FeCl3溶液反应 | FeCl3溶液蚀刻铜线路板 |
| C | K2FeO4与水反应生成O2和Fe(OH)3 | K2FeO4可作水的消毒剂和净化剂 |
| D | 常温下干燥的氯气与铁不反应 | 用钢瓶储存液氯 |
| A. | A | B. | B | C. | C | D. | D |
20.下列化学用语书写正确的是( )
| A. | 镁离子的结构示意图: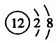 | B. | 苯甲酸乙酯的结构简式: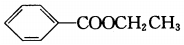 | ||
| C. | CO2的电子式: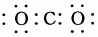 | D. | 中子数为18的氯原子:${\;}_{17}^{18}$Cl |
19.在下列给定条件的溶液中,可能大量共存的离子组是( )
0 160880 160888 160894 160898 160904 160906 160910 160916 160918 160924 160930 160934 160936 160940 160946 160948 160954 160958 160960 160964 160966 160970 160972 160974 160975 160976 160978 160979 160980 160982 160984 160988 160990 160994 160996 161000 161006 161008 161014 161018 161020 161024 161030 161036 161038 161044 161048 161050 161056 161060 161066 161074 203614
| A. | 含有大量Fe3+的溶液中:Na+、SCN-、Cl-、Br- | |
| B. | 与铝粉反应放出氢气的无色溶液中:NO3-、Al3+、Na+、SO42- | |
| C. | AlO2-、Cl-、Al3+、K+ | |
| D. | 在由水电离出的c(H+)=1.0×10-12mol/L的溶液中:CO32-、Na+、K+、Cl- |