1.关于化学式为[TiCl(H2O)5]Cl2•H2O的配合物的下列说法中正确的是( )
| A. | 配位体是Cl-和H2O,配位数是9 | |
| B. | 中心离子是Ti3+,形成配位键时提供电子对 | |
| C. | 配离子是[TiCl(H2O)5]2+,内界和外界中的Cl-的数目比是1:2 | |
| D. | 向含1 mol该配合物的水溶液中加入足量AgNO3溶液,生成AgCl沉淀3 mol |
20.下列分子或离子中,中心原子不是sp3杂化的是( )
| A. | SO42- | B. | NO3- | C. | CH4 | D. | H2S |
19.下列说法正确的是( )
| A. | π键是由两个p轨道“头碰头”重叠形成的 | |
| B. | σ键就是单键,π键就是双键 | |
| C. | 乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键 | |
| D. | H2分子中含σ键,而Cl2分子中含π键 |
18.下列说法不正确的是( )
| A. | 俄国化学家门捷列夫于1869年发表了第一张元素周期表 | |
| B. | 现代化学常利用原子光谱的特征谱线来测定分子的结构 | |
| C. | DNA双螺旋的两个螺旋链是用氢键相结合的 | |
| D. | 区分晶体和非晶体最可靠的科学方法是X-射线衍射实验 |
16.(1)请将下列变化过程中破坏的微粒间作用力名称的编号填在横线上:
A.共价键 B.离子键 C.金属键 D.分子间作用力
①氢氧化钠熔化B;②干冰升华D;
③二氧化硅熔化A; ④钠熔化C.
(2)单质硼有无定形和晶体两种,参考表数据.
①根据表中数据判断晶体硼的晶体类型属于原子晶体;
②请解释金刚石的熔沸点高于晶体硅的原因是C-C键长比Si-Si键长短,所以C-C键能比Si-Si键能大,熔化或汽化所需要的能量多,所以金刚石的熔、沸点比晶体硅高.
A.共价键 B.离子键 C.金属键 D.分子间作用力
①氢氧化钠熔化B;②干冰升华D;
③二氧化硅熔化A; ④钠熔化C.
(2)单质硼有无定形和晶体两种,参考表数据.
| 金刚石 | 晶体硅 | 晶体硼 | |
| 熔点(K) | >3823 | 1683 | 2573 |
| 沸点(K) | 5100 | 2628 | 2823 |
| 硬度(Moh) | 10 | 7.0 | 9.5 |
②请解释金刚石的熔沸点高于晶体硅的原因是C-C键长比Si-Si键长短,所以C-C键能比Si-Si键能大,熔化或汽化所需要的能量多,所以金刚石的熔、沸点比晶体硅高.
15.在恒温、恒容条件下,能使A(g)+B(g)?C(g)+D(s) 正反应速率增大的措施是( )
| A. | 减小C或D的浓度 | B. | 再加入一定量D | C. | 减小B的浓度 | D. | 增大A或B的浓度 |
14.实验室用如图所示装置制备氯气并进行性质实验(必要时可加热,省略夹持装置).
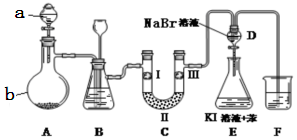
(1)仪器a的名称是:分液漏斗;装置B中长颈漏斗的作用是:平衡装置中压强,防止玻璃仪器破裂.蒸馏烧瓶b中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)洗气装置B试剂是饱和食盐水,其作用是除去氯气中的氯化氢气体,分液漏斗D中发生反应的化学方程式为Cl2+2NaBr=Br2+2NaCl.
(3)装置C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,设计C装置的目的是验证氯气还是次氯酸具有漂白性.
(4)F处为尾气吸收装置,写出实验室利用烧碱溶液吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(5)实验结束后将产生的氯气通入含紫色石蕊溶液的试管里,请填写表中的空白:

(1)仪器a的名称是:分液漏斗;装置B中长颈漏斗的作用是:平衡装置中压强,防止玻璃仪器破裂.蒸馏烧瓶b中发生反应的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(2)洗气装置B试剂是饱和食盐水,其作用是除去氯气中的氯化氢气体,分液漏斗D中发生反应的化学方程式为Cl2+2NaBr=Br2+2NaCl.
(3)装置C中I、II、III依次放入湿润的有色布条、无水氯化钙、干燥的有色布条,设计C装置的目的是验证氯气还是次氯酸具有漂白性.
(4)F处为尾气吸收装置,写出实验室利用烧碱溶液吸收Cl2的离子方程式Cl2+2OH-=Cl-+ClO-+H2O.
(5)实验结束后将产生的氯气通入含紫色石蕊溶液的试管里,请填写表中的空白:
| 实验现象 | 原因 |
| 溶液最初从紫色逐渐变为红色 | 氯气与水反应生成的H+使石蕊变色 |
| 随后溶液逐渐变为无色 | 氯气与水反应生成HClO具有漂白性 |
| 然后溶液从无色逐渐变为浅黄绿色 | 过量氯气溶解于水中 |
13.设NA 表示阿伏加德罗常数值.下列说法正确的是( )
0 160740 160748 160754 160758 160764 160766 160770 160776 160778 160784 160790 160794 160796 160800 160806 160808 160814 160818 160820 160824 160826 160830 160832 160834 160835 160836 160838 160839 160840 160842 160844 160848 160850 160854 160856 160860 160866 160868 160874 160878 160880 160884 160890 160896 160898 160904 160908 160910 160916 160920 160926 160934 203614
| A. | 标准状况下,11.2 L的甲醇所含的氢原子数等于2NA | |
| B. | 常温下,Na2O2与H2O反应生成1mol O2时,转移电子数是2NA | |
| C. | 标准状况下,2.24 LCl2溶于水中达到饱和,可得到HClO分子的数目是0.1NA | |
| D. | 1L 1 mol/L CuCl2溶液中含有的铜离子数为NA |
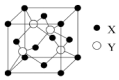 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层电子数的3倍;元素W基态原子的核外电子共有16种运动状态.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为1;元素Y基态原子的3p轨道上有5个电子;元素Z的原子最外层电子数是其内层电子数的3倍;元素W基态原子的核外电子共有16种运动状态. .
.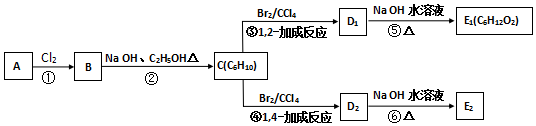
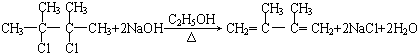 ,C的化学名称为2,3-二甲基-1,3-丁二烯,E2的结构简式是
,C的化学名称为2,3-二甲基-1,3-丁二烯,E2的结构简式是 ,②的反应类型是消去反应.
,②的反应类型是消去反应. +2NaOH$→_{△}^{H_{2}O}$
+2NaOH$→_{△}^{H_{2}O}$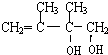 +2NaBr.
+2NaBr.