3.下列各组物质混合、加热蒸干、并经充分灼烧,得到混合物的是( )
| A. | 0.1 mol•L-1 CH3COOH溶液与0.1 mol•L-1NaOH溶液等体积混合 | |
| B. | 向40mL0.2 mol•L-1的NaOH溶液中通入67.2mLCO2(标况) | |
| C. | 在100mL1 mol•L-1NH4Cl溶液中,投入3.9gNa2O2 | |
| D. | 在20mL0.01 mol•L-1Ma(HCO3)2溶液中,投入0.2g Ma(OH)2 |
2.下列说法不正确的是( )
| A. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 | |
| B. | 用热的纯碱溶液去油污效果更好 | |
| C. | 制备无水的AlCl3、FeCl3均不能采用将溶液在空气中直接蒸干的方法 | |
| D. | 室温下,向0.1mol/L的HF溶液中加入少量水溶液显碱性的物质,HF的电离程度一定增大 |
1.下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 某弱酸的酸式盐NaHA溶液中一定有:c(OH-)+2c(A2-)=c(H+)+c(H2A) | |
| B. | 0.2 mol•L-1 CH3COONa溶液与0.1 mol•L-1盐酸等体积混合后的酸性溶液中:>c(CH3COO-)>c(CH3COOH)>c(Cl-)>c(H+) | |
| C. | 室温下,向100ml0.5mol/L的Na2CO3溶液中加入0.05molCaO,溶液中增大$\frac{c(O{H}^{-})}{c(H{{C}_{3}}^{-})}$ | |
| D. | 0.1 mol•L-1(NH4)2Fe(SO4)2溶液中:c(NH4+)+c(NH3•H2O)+c(Fe2+)=0.3 mol•L-1 |
20.在一定条件下,将C(s)和H2O(g)分别加入甲、乙两个密闭容器,发生反应:C(s)+2H2O(g)?CO2(g)+2H2(g),其相关数据如表所示:
(1)T1>T2(填“>”、“<”或“=”)
(2)达到平衡后,保持温度和体积不变,向甲容器内再充入0.8molH2O和3.2molH2,则此时V正=V逆
(填“>”、“<”或“=”)
(3)在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是BD.
A.V逆(CO2)═2V正(H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均相对分子质量保持不变
(4)某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:
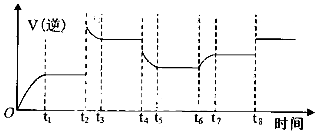
可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是通入H2O,则从t1到t8哪个时间段H2O (g)的平衡转化率最低t7-t8,(填“t1~t2,以此类推”).
| 容器 | 容积/L | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所需时间/min | |
| C(s) | H2O(g) | H2(g) | ||||
| 甲 | 2 | T1 | 2 | 4 | 3.2 | 2.8 |
| 乙 | 1 | T2 | 1 | 2 | 1.2 | 3.0 |
(2)达到平衡后,保持温度和体积不变,向甲容器内再充入0.8molH2O和3.2molH2,则此时V正=V逆
(填“>”、“<”或“=”)
(3)在密闭恒容的容器中,能表示上述反应达到化学平衡状态的是BD.
A.V逆(CO2)═2V正(H2)
B.混合气体的密度保持不变
C.c(H2O):c(CO2):c(H2)=2:1:2
D.混合气体的平均相对分子质量保持不变
(4)某同学为了研究反应条件对化学平衡的影响,测得逆反应速率与时间的关系如图所示:

可见在t1、t3、t5、t7时反应都达了到平衡状态,如果t2、t4、t6、t8时都只改变了一个反应条件,则t6时刻改变的条件是通入H2O,则从t1到t8哪个时间段H2O (g)的平衡转化率最低t7-t8,(填“t1~t2,以此类推”).
19.短周期元素X、Y、Z、M 的原子序数依次增大,元素X 的一种单质是高硬度的宝石,Y2+的电子层结构与氖相同,Z的质子数为偶数.室温下M 的单质为淡黄色固体.下列说法正确的是( )
| A. | 原子半径:M>Z>Y>X | |
| B. | 气态氢化物:X<Z | |
| C. | X的氧化物一定是非极性分子 | |
| D. | Y单质可用于航空航天合金材料的制备 |
18.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | lmolNacl 固体中含有NA个Na+ | |
| B. | 18gD2O和18gH2 O中含有的质子数均为10NA | |
| C. | 标准状况下2.24LH2O 含有的共价键数为0.2NA | |
| D. | 密闭容答中2molNO 与lmolO2充分反应,产物的分子数为2NA |
17.化学与生活、生产密切相关.下列食品添加剂中,其使用目的与反应速率有关的是( )
0 159415 159423 159429 159433 159439 159441 159445 159451 159453 159459 159465 159469 159471 159475 159481 159483 159489 159493 159495 159499 159501 159505 159507 159509 159510 159511 159513 159514 159515 159517 159519 159523 159525 159529 159531 159535 159541 159543 159549 159553 159555 159559 159565 159571 159573 159579 159583 159585 159591 159595 159601 159609 203614
| A. | 调味剂 | B. | 防腐剂 | C. | 增稠剂 | D. | 着色剂 |
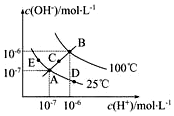 已知水的电离平衡曲线如图示,试回答下列问题:
已知水的电离平衡曲线如图示,试回答下列问题:

 ;
;