12.合金是一类用途广泛的金属材料.下列物质中,不属于合金的是( )
| A. | 水银 | B. | 青铜 | C. | 碳素钢 | D. | 不锈钢 |
11.反应Br+H2═HBr+H的能量与反应历程的关系曲线如图所示,下列叙述中正确的是( )


| A. | 反应热:过程Ⅰ>过程Ⅱ | |
| B. | 两个过程的反应热是相同的,△H=-80 kJ•mol-1 | |
| C. | 过程I中使用了催化剂 | |
| D. | 该反应为吸热反应 |
10.已知四价铅有强氧化性,能跟盐酸反应生成氯气,将SO2通入悬浮着黑色PbO2的热水中,过一会儿,将发生的情形是( )
| A. | 悬浮物由黑色变为白色,因SO2是一种漂白剂 | |
| B. | 悬浮物由黑色变为白色,因为形成了PbSO4 | |
| C. | 有黄色沉淀生成 | |
| D. | 有臭鸡蛋味的气体放出 |
9.现将标准状况下的2.24L HCl气体溶解在含有0.2mol醋酸钠溶液的烧杯中,测得溶液体积为1L.若此溶液中c(CH3COO-)>c(Cl-),则下列判断中不正确的是( )
| A. | c(CH3COO-)+c(OH-)=0.10 mol•L-1 | B. | c(CH3COOH)+c(CH3COO-)=0.20 mol•L-1 | ||
| C. | c(CH3COOH)<c(CH3COO-) | D. | 温度为298 K时,pH<7 |
8.有机物分子中的原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )
| A. | 苯酚与浓硝酸、浓硫酸反应生成 ,苯与浓硝酸、浓硫酸反应生成硝基苯 ,苯与浓硝酸、浓硫酸反应生成硝基苯 | |
| B. | 乙烯能发生加成反应,乙醇不能发生加成反应 | |
| C. | 苯酚能和氢氧化钠溶液反应,而乙醇不能和氢氧化钠溶液反应 | |
| D. | 苯酚苯环上的氢比苯分子中的氢更容易被卤素原子取代 |
7.两种气态烃组成的混合气体0.1mol,完全燃烧得0.16mol CO2和3.6g H2O,则下列关于混合气体组成的推断正确的是( )
| A. | 一定有甲烷 | B. | 一定是甲烷和乙烯 | ||
| C. | 一定没有丙炔 | D. | 一定有乙炔 |
6.短周期元素X、Y、Z、W、Q在元素周期表中的相对位置如图所示.下列说法正确的是( ) 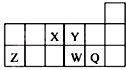

| A. | 原子半径的大小顺序为:rX>rY>rZ>rW>rQ | |
| B. | 离子Y2-和Z3+的核外电子数和电子层数都不相同 | |
| C. | 元素W的最高价氧化物对应的水化物的酸性比Q的强 | |
| D. | 元素Y的单质比元素X的单质更容易与氢气反应 |
5.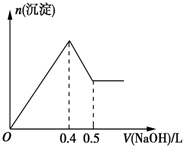 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
 现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入0.1mol/L的NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 6:1 | B. | 2:3 | C. | 1:3 | D. | 3:1 |
4.某研究性学习小组进行如下探究活动:
实验目的:探究Cl2、Br2、I2的氧化性强弱.
查阅资料:①常温下,高锰酸钾与浓盐酸反应产生氯气;
②溴单质易挥发,碘单质易升华;
③淀粉溶液遇到碘单质变蓝色;
④溴、碘在不同溶剂中所形成溶液(从稀到浓)的颜色变化如图所示.
实验方案:该小组设计如图所示装置实验(夹持仪器已略去,装置气密性完好)

实验过程:
Ⅰ先打开弹簧夹,再打开活塞a,滴加浓盐酸
Ⅱ当B和C中的溶液都变黄时,加紧弹簧夹
Ⅲ当B中的溶液由黄色变为棕色时,关闭活塞a
Ⅳ…
回答以下问题:
(1)验证氯气的氧化性强于碘的实验现象是A中湿润的淀粉碘化钾试纸变蓝,写出该反应的化学方程式Cl2+2KI═I2+2KCl;
(2)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是打开活塞b,将分液漏斗中的黄色溶液滴入D中,关闭活塞b,取下试管D振荡,静置,观察到D中CCl4层溶液变为紫红色,说明溴的氧化性强于碘,写出该反应的离子方程式2I-+Br 2=2Br-+I2;
(3)由实验得到的氯、溴、碘单质的氧化性由强到弱的顺序为Cl2>Br2>I2;
(4)你认为实验中为什么要加过程Ⅲ这一步操作,请简述个人观点B、C中的NaBr溶液的浓度和体积均相同,棕色溶液B含有的溴单质比黄色溶液C中的多,说明C中还存有溴离子,不存在氯气,确保了氯气不干扰溴与碘化钾的反应.
实验目的:探究Cl2、Br2、I2的氧化性强弱.
查阅资料:①常温下,高锰酸钾与浓盐酸反应产生氯气;
②溴单质易挥发,碘单质易升华;
③淀粉溶液遇到碘单质变蓝色;
④溴、碘在不同溶剂中所形成溶液(从稀到浓)的颜色变化如图所示.
| 水 | 四氯化碳 | |
| 溴 | 黄→棕 | 橙→橙红 |
| 碘 | 深黄→褐 | 紫→深紫 |

实验过程:
Ⅰ先打开弹簧夹,再打开活塞a,滴加浓盐酸
Ⅱ当B和C中的溶液都变黄时,加紧弹簧夹
Ⅲ当B中的溶液由黄色变为棕色时,关闭活塞a
Ⅳ…
回答以下问题:
(1)验证氯气的氧化性强于碘的实验现象是A中湿润的淀粉碘化钾试纸变蓝,写出该反应的化学方程式Cl2+2KI═I2+2KCl;
(2)为验证溴的氧化性强于碘,过程Ⅳ的操作和现象是打开活塞b,将分液漏斗中的黄色溶液滴入D中,关闭活塞b,取下试管D振荡,静置,观察到D中CCl4层溶液变为紫红色,说明溴的氧化性强于碘,写出该反应的离子方程式2I-+Br 2=2Br-+I2;
(3)由实验得到的氯、溴、碘单质的氧化性由强到弱的顺序为Cl2>Br2>I2;
(4)你认为实验中为什么要加过程Ⅲ这一步操作,请简述个人观点B、C中的NaBr溶液的浓度和体积均相同,棕色溶液B含有的溴单质比黄色溶液C中的多,说明C中还存有溴离子,不存在氯气,确保了氯气不干扰溴与碘化钾的反应.
3.下列叙述不正确的是( )
0 156597 156605 156611 156615 156621 156623 156627 156633 156635 156641 156647 156651 156653 156657 156663 156665 156671 156675 156677 156681 156683 156687 156689 156691 156692 156693 156695 156696 156697 156699 156701 156705 156707 156711 156713 156717 156723 156725 156731 156735 156737 156741 156747 156753 156755 156761 156765 156767 156773 156777 156783 156791 203614
| A. | NH4H的电子式为 | |
| B. | NH4Cl的电子式为 | |
| C. | NH4H含有极性共价键和离子键 | |
| D. | NH4H固体投入少量热水中,有两种气体生成 |