题目内容
3.下列叙述不正确的是( )| A. | NH4H的电子式为 | |
| B. | NH4Cl的电子式为 | |
| C. | NH4H含有极性共价键和离子键 | |
| D. | NH4H固体投入少量热水中,有两种气体生成 |
分析 A.氢化铵(NH4H)与氯化铵的结构相似是离子化合物,铵根离子和氢阴离子形成离子键;
B.氯化铵是氯离子和铵根离子形成的离子化合物,氯离子最外层电子为标出;
C.NH4H是离子化合物,铵根中含有极性共价键,铵根离子和氢离子形成离子键;
D.氢化铵与水反应生成氨气和氢气.
解答 解:A.氢化铵(NH4H)与氯化铵的结构相似是离子化合物,铵根离子和氢阴离子形成离子键,电子式为: ,故A正确;
,故A正确;
B.氯化铵是氯离子和铵根离子形成的离子化合物,氯离子最外层电子为标出,正确的电子式为: ,故B错误;
,故B错误;
C.NH4H是离子化合物,铵根中含有极性共价键N-H键,铵根离子和氢离子形成离子键,故C正确;
D.NH4H固体投入少量热水中反应生成氢气和氨气,方程式:NH4H+H2O=NH3↑+H2↑+H2O,故D正确;
故选:B.
点评 本题考查了电子式书写及物质所含化学键类型的判断,明确氢化铵的结构特点及所含化学键类型是解题关键,题目难度中等.

练习册系列答案
相关题目
13.下列物质的分子中,共用电子对数目最多的是( )
| A. | N2 | B. | NH3 | C. | H2O | D. | CH4 |
14.将X气体通入Y溶液中,实验结果与预测的现象一致的组合是( )
| 选项 | X气体 | Y溶液 | 预测的现象 |
| ① | CO2 | BaCl2溶液 | 白色沉淀析出 |
| ② | SO2 | Ba(N03)2溶液 | 白色沉淀析出 |
| ③ | Cl2 | AgNO3溶液 | 白色沉淀析出 |
| ④ | NH3 | FeCl2溶液 | 白色沉淀产生 |
| A. | ①②③ | B. | ①②④ | C. | ①③④ | D. | ②③④ |
11.下列各组顺序的排列不正确的是( )
| A. | 原子半径:Na>Mg>Al | B. | 热稳定性:HCl<H2S<PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H3PO4 | D. | 熔点:Na>K>Rb |
18.下列说法正确的是( )
| A. | 每一周期元素都是从碱金属开始,以稀有气体结束 | |
| B. | f区都是副族元素,s区和p区的都是主族元素 | |
| C. | 铝的第一电离能小于K的第一电离能 | |
| D. | B电负性和Si相近 |
8.有机物分子中的原子间(或原子与原子团间)的相互影响会导致物质化学性质的不同.下列各项的事实不能说明上述观点的是( )
| A. | 苯酚与浓硝酸、浓硫酸反应生成 ,苯与浓硝酸、浓硫酸反应生成硝基苯 ,苯与浓硝酸、浓硫酸反应生成硝基苯 | |
| B. | 乙烯能发生加成反应,乙醇不能发生加成反应 | |
| C. | 苯酚能和氢氧化钠溶液反应,而乙醇不能和氢氧化钠溶液反应 | |
| D. | 苯酚苯环上的氢比苯分子中的氢更容易被卤素原子取代 |
15.下列每个选项的甲乙两个反应中,属于同一种反应类型的是( )
| 选项 | 甲 | 乙 |
| A | 溴乙烷水解制备乙醇 | 乙烯水化制备乙醇 |
| B | 甲烷与氯气反应制备四氯化碳 | 乙烯通入KMnO4溶液中 |
| C | 甲苯与KMnO4溶液反应生成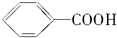 | 苯与液溴反应制备溴苯 |
| D | 蛋白质水解得到氨基酸 | 乙醇与冰醋酸反应生成乙酸乙酯 |
| A. | A | B. | B | C. | C | D. | D |
12.将盛有12mL NO2和O2的混合气体的量筒倒立于水槽中,充分反应后,还剩余2mL无色气体,则原混合气体中O2的体积和剩余的2mL气体分别是( )
| A. | 1.2 mL,NO | B. | 2.4 mL,O2 | C. | 3.5 mL,O2 | D. | 4 mL,NO |
13.根据元素周期律及元素周期表的知识分析,下列关系中不正确的是( )
| A. | 酸性强弱:H3PO4>H2SO4>HClO4 | B. | 离子半径大小:F->Na+>Mg2+>Al3+ | ||
| C. | 稳定性大小:SiH4<PH3<H2S<HCl | D. | 碱性强弱:NaOH>Mg(OH)2>Al(OH)3 |