
(1)该硫酸的物质的量浓度是________mol/L。
(2)某化学兴趣小组进行硫酸性质的实验探究时,需要490 mL 4.6 mol/L的稀硫酸,则需要取________mL的该硫酸。
(3)配制时,所需的玻璃仪器除量筒、烧杯、玻璃棒和胶头滴管之外,还需要 (填仪器名称);
(4)配制溶液有如下(未按顺序排列):a.溶解,b.摇匀,c.洗涤,d.冷却,e.称量,f.将溶液移至容量瓶,g.定容等操作。 其中摇匀的前一步操作是 ;(填写字母)
(5)在下列配制过程示意图中,有错误的是(填写序号) 。

(6)在配制4.6 mol/L的稀硫酸的过程中,下列情况会引起硫酸溶液物质的量浓度偏高的是_________
A.未经冷却趁热将溶液注入容量瓶中 | B.容量瓶洗涤后,未经干燥处理 |
C.定容时仰视观察液面 | D.未洗涤烧杯和玻璃棒 |
4.某羧酸酯的分子式为C10H18O4,在NaOH溶液中1mol该酯完全水解可得到2mol乙醇和1mol羧酸钠,将羧酸钠酸化后得羧酸X,则X可能的结构共有(不考虑立体异构)( )
| A. | 7种 | B. | 8种 | C. | 9种 | D. | 10种 |
3.明代宋应星在《天工开物》对“膏夜”的描述:“草木之实,其中蕴藏膏液而不能自流.假媒水火,凭借木石,而后倾注而出焉.”、“榨出水油清亮无比,贮小盏之中,独根心草燃至天明,盖诸清油所不及者.”,下列有关说法中正确的是( )
| A. | “膏液”的主要成分是石油 | B. | “膏液”是天然高分子化合物 | ||
| C. | “膏液”是烃的混合物 | D. | “膏液”能发生取代反应 |
1.25℃时氯水含Cl2、HClO和ClO-组份φ%(以物质的量计算)分布图如下,下列结论正确的是( )

| A. | n(Cl2)、n(HClO)和n(ClO-)之和不随pH变化而变化 | |
| B. | 当pH逐渐增大时,HClO先增大后减小 | |
| C. | 当pH>8.5时,c(H+)=c(OH-)+c(ClO-)+c(Cl-) | |
| D. | K1、K2均是通过曲线交点计算得出的酸的电离平衡常数 |
20.高铁酸钾(K2FeO4)作为多功能水处理剂具有广泛的用途,下面是利用次氯酸盐在碱性条件下氧化硝酸铁制备的生产K2FeO4工艺流程图:

下列判断正确的是( )
0 154598 154606 154612 154616 154622 154624 154628 154634 154636 154642 154648 154652 154654 154658 154664 154666 154672 154676 154678 154682 154684 154688 154690 154692 154693 154694 154696 154697 154698 154700 154702 154706 154708 154712 154714 154718 154724 154726 154732 154736 154738 154742 154748 154754 154756 154762 154766 154768 154774 154778 154784 154792 203614

下列判断正确的是( )
| A. | 反应中氯气只起氧化剂的作用 | |
| B. | 溶液Ⅰ的溶质是KClO | |
| C. | 生成反应液II中的反应氧化剂与还原剂的物质的量之比为1:1 | |
| D. | 溶液Ⅱ的溶液成分中含有K2FeO4 |
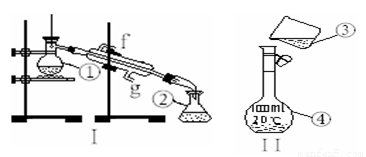
 出下列仪器的名称:① ②
出下列仪器的名称:① ②