2.下列有关Al(OH)3的图象不正确的是( )
| A. | 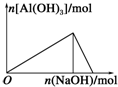 向AlCl3溶液中滴加NaOH溶液 | B. | 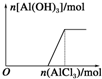 向NaOH溶液中滴加AlCl3溶液 | ||
| C. | 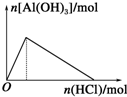 向Na[Al(OH)4]溶液中通入CO2 | D. |  向AlCl3溶液中滴氨水 |
1.下列固体物质属于晶体的是( )
| A. | 橡胶 | B. | 食盐 | C. | 石蜡 | D. | 玻璃 |
19.在盛有足量A的体积可变的密闭容器中通入B,发生反应:A(s)+2B(g)?4C(g)+D(g)△H>0,在一定温度、压强下达到平衡.平衡时C的物质的量与通入B的物质的量的变化关系如图所示.下列说法正确的是:( )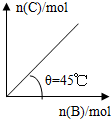
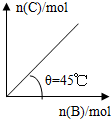
| A. | 平衡时B的转化率为40% | |
| B. | 若再通入B,则再次达平衡时C的体积分数增大 | |
| C. | 在容器中加入催化剂,则B的转化率增大 | |
| D. | 若保持压强一定,当温度升高时,图中θ>45° |
18.用已知浓度的NaOH滴定未知浓度的盐酸,下列操作(其他操作正确)会造成测定结果偏高的是( )
| A. | 滴定终点读数时俯视度数 | |
| B. | 酸式滴定管使用前,水洗后未用待测盐酸润洗 | |
| C. | 锥形瓶洗净后未干燥 | |
| D. | 碱式滴定管滴定前尖嘴部分有气泡,滴定后气泡消失 |
16.饱和醇X的分子式为C5H12O,与足量乙酸反应生成酯Y,且X可由烯烃与水在一定条件下反应制得,Y的结构共有( )
| A. | 6种 | B. | 7种 | C. | 8种 | D. | 9种 |
15.设NA代表阿伏加德罗常数的数值,下列有关说法正确的是( )
| A. | 1mol乙烷含C-H键的数目为7NA | |
| B. | 1L0.5mol/LNa2S溶液中HS-的数目为0.5NA | |
| C. | 标准状况下,Na与水反应产生22.4 LH2时转移电子数目为2 NA | |
| D. | 含1mol HCOOH的水溶液中含氧原子的总数目为2NA |
14.将金属钠投入AlCl3溶液中,下列有关叙述一定正确的是( )
0 154513 154521 154527 154531 154537 154539 154543 154549 154551 154557 154563 154567 154569 154573 154579 154581 154587 154591 154593 154597 154599 154603 154605 154607 154608 154609 154611 154612 154613 154615 154617 154621 154623 154627 154629 154633 154639 154641 154647 154651 154653 154657 154663 154669 154671 154677 154681 154683 154689 154693 154699 154707 203614
| A. | 最后一定有沉淀生成,且有气体放出 | |
| B. | 溶液最后一定澄清,且有气体放出 | |
| C. | 一定有气体放出 | |
| D. | 一定无气体放出 |
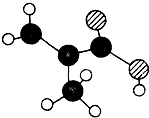 某物质只含C,H,O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表化学键:单键、双键等):
某物质只含C,H,O三种元素,其分子模型如图所示,分子中共有12个原子(图中球与球之间的连线代表化学键:单键、双键等):
