8.用如图所示的装置进行实验,反应一段时间后断开K,向烧杯中加入0.1mol CuO后CuSO4溶液恰好恢复到反应前的浓度和pH.下列说法中不正确的是( )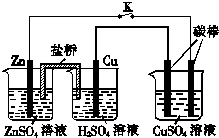

| A. | 铜棒为正极,其电极反应式为2H++2e-=H2↑ | |
| B. | 烧杯右侧碳棒为阴极,其电极表面有红色物质析出 | |
| C. | 反应中消耗锌的质量为6.5 g | |
| D. | 导线中通过电子的物质的量为0.1 mol |
6.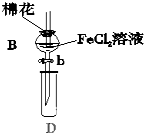 某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气.
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子.
Ⅲ.接着再向B中通入一定量的SO2气体.
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子.
(1)棉花中浸润的溶液为NaOH溶液,目的是防止污染环境.
(2)实验室制备氯气的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)过程Ⅲ中一定发生反应的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是取溶液少许于试管中,先加入足量稀盐酸酸化,再滴加少量BaCl2溶液,若有白色沉淀生成,证明有SO42-,反之无SO42-.
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是SO2>Fe2+>Cl-
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是乙、丙.
 某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:
某探究学习小组用如图所示装置进行SO2、Fe2+和Cl-还原性强弱比较实验,实验过程如下:Ⅰ.先向B中的FeCl2溶液(约10mL)中通入Cl2,当B中溶液变黄时,停止通气.
Ⅱ.打开活塞b,使约2mL的溶液流入D试管中,检验取出溶液中的离子.
Ⅲ.接着再向B中通入一定量的SO2气体.
Ⅳ.更新试管D,重复过程Ⅱ,检验取出溶液中的离子.
(1)棉花中浸润的溶液为NaOH溶液,目的是防止污染环境.
(2)实验室制备氯气的化学方程式为MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O.
(3)过程Ⅲ中一定发生反应的离子方程式为2Fe3++SO2+2H2O═2Fe2++SO42-+4H+,过程Ⅳ中检验取出溶液中是否含有硫酸根的操作是取溶液少许于试管中,先加入足量稀盐酸酸化,再滴加少量BaCl2溶液,若有白色沉淀生成,证明有SO42-,反之无SO42-.
(4)该小组对SO2、Fe2+和Cl-还原性强弱比较期望达到的结论是SO2>Fe2+>Cl-
(5)甲、乙、丙三同学分别完成了上述实验,下表是他们的检测结果,他们的检测结果一定能够证明SO2、Fe2+和Cl-还原性强弱关系的是乙、丙.
| 过程Ⅱ中检出离子 | 过程Ⅳ中检出离子 | |
| 甲 | 有Fe3+无Fe2+ | 有SO42- |
| 乙 | 既有Fe3+又有Fe2+ | 有SO42- |
| 丙 | 有Fe3+无Fe2+ | 有Fe2+ |
5.气体摩尔体积的单位是( )
| A. | g/L | B. | L/mol | C. | mol/L | D. | L/g |
3.下列说法正确的是( )
| A. | 硫粉在过量的纯氧中燃烧可以生成三氧化硫 | |
| B. | 用饱和碳酸钠溶液除去二氧化碳中的二氧化硫 | |
| C. | 等质量的NaHCO3和Na2CO3与足量稀盐酸反应产生CO2的量:Na2CO3<NaHCO3 | |
| D. | 过量的铁在氯气中燃烧生成FeCl2 |
2.短周期元素A、B、C、D、E、R、T原子序数依次增大,原子结构及性质如表所示:
(1)R元素在周期表的位置是第三周期IVA族,化合物DT中存在的化学键是离子键.
(2)写出E单质与NaOH溶液反应的离子方程式2Al+2H2O+2OH-═2AlO2-+3H2↑.
(3)1g B2A4完全燃烧,恢复到常温时放出a kJ的热量,写出B2A4完全燃烧的热化学方程式C2H4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-28a kJ/mol;B2A4形成高分子的化学方程式n C2H4$\stackrel{一定条件}{→}$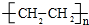 .
.
(4)RT4极易水解生成两种酸,写出该反应的化学方程式SiCl4+4H2O=H4SiO4↓+4HCl.
(5)工业上用A元素的单质、C元素的单质合成化合物,此反应的平衡常数表达式为$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}(N{H}_{3})}$;为了提高合成效率,常采用的方法有采取高温高压、使用催化剂.
(6)D的过氧化物的电子式为 ;它可用于潜艇或呼吸面具的供氧剂,它与H2O反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
;它可用于潜艇或呼吸面具的供氧剂,它与H2O反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
(7)工业上电解饱和DT水溶液的离子方程式为2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑.
| 元素 | 结构及性质 |
| A | A的原子半径最小 |
| B | B原子最外层电子数是次外层的两倍 |
| C | C元素在空气中含量最多 |
| D | D是短周期中金属性最强的元素 |
| E | E的最高价氧化物对应水化物是一种常见的两性氢氧化物 |
| R | R与B同主族 |
| T | T的负一价阴离子的核外电子排布与Ar原子相同 |
(2)写出E单质与NaOH溶液反应的离子方程式2Al+2H2O+2OH-═2AlO2-+3H2↑.
(3)1g B2A4完全燃烧,恢复到常温时放出a kJ的热量,写出B2A4完全燃烧的热化学方程式C2H4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-28a kJ/mol;B2A4形成高分子的化学方程式n C2H4$\stackrel{一定条件}{→}$
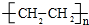 .
.(4)RT4极易水解生成两种酸,写出该反应的化学方程式SiCl4+4H2O=H4SiO4↓+4HCl.
(5)工业上用A元素的单质、C元素的单质合成化合物,此反应的平衡常数表达式为$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}(N{H}_{3})}$;为了提高合成效率,常采用的方法有采取高温高压、使用催化剂.
(6)D的过氧化物的电子式为
 ;它可用于潜艇或呼吸面具的供氧剂,它与H2O反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.
;它可用于潜艇或呼吸面具的供氧剂,它与H2O反应的化学方程式为2Na2O2+2H2O=4NaOH+O2↑.(7)工业上电解饱和DT水溶液的离子方程式为2Cl-+2H2O $\frac{\underline{\;电解\;}}{\;}$2OH-+Cl2↑+H2↑.
20.下列反应中硝酸既能表现出酸性又表现出氧化性的是( )
0 154494 154502 154508 154512 154518 154520 154524 154530 154532 154538 154544 154548 154550 154554 154560 154562 154568 154572 154574 154578 154580 154584 154586 154588 154589 154590 154592 154593 154594 154596 154598 154602 154604 154608 154610 154614 154620 154622 154628 154632 154634 154638 154644 154650 154652 154658 154662 154664 154670 154674 154680 154688 203614
| A. | 使石蕊试液变红 | |
| B. | 与铜反应生成Cu(NO3)2和NO气体 | |
| C. | 与Na2CO3反应放出CO2气体生成NaNO3 | |
| D. | 与C单质混合共热时生成CO2和NO2 |