题目内容
20.下列反应中硝酸既能表现出酸性又表现出氧化性的是( )| A. | 使石蕊试液变红 | |
| B. | 与铜反应生成Cu(NO3)2和NO气体 | |
| C. | 与Na2CO3反应放出CO2气体生成NaNO3 | |
| D. | 与C单质混合共热时生成CO2和NO2 |
分析 硝酸既能表现出酸性又表现出氧化性,在反应中应生成硝酸盐,且硝酸钡还原生成NO或NO2等物质,以此解答.
解答 解:A.使石蕊变红,只能说明硝酸具有酸性,不能说明氧化性,故A错误;
B.与铜反应生成Cu(NO3)2和NO气体,生成硝酸铜表现酸性,生成NO表现硝酸的氧化性,故B正确;
C.与Na2CO3反应放出CO2气体生成NaNO3,说明硝酸的酸性比碳酸强,不发生氧化还原反应,故C错误;
D.与C单质混合共热时生成H2SO4和CO2,只表现硝酸的氧化性,不表现酸性,故D错误.
故选B.
点评 本题考查硝酸的性质,侧重于学生的分析能力和元素化合物知识的综合运用,有利于培养学生学习的积极性和良好的科学素养,难度不大.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案 开心蛙状元作业系列答案
开心蛙状元作业系列答案
相关题目
11.下列关于物质性质的叙述中,正确的是( )
| A. | 硫是一种淡黄色的能溶于水的晶体,既有氧化性又有还原性 | |
| B. | N2是大气中的主要成分之一,雷雨时,可直接转化为NO2 | |
| C. | Cl2能与金属活动顺序表中大多数金属反应 | |
| D. | 硅是应用广泛的半导体材料,常温下化学性质活泼 |
5.气体摩尔体积的单位是( )
| A. | g/L | B. | L/mol | C. | mol/L | D. | L/g |
12.常温下,将0.1mol•L-1氢氧化钠溶液与0.06mol•L-1硫酸溶液等体积混合,该混合溶液的pH等于( )lg2=0.3.
| A. | 1.7 | B. | 2.0 | C. | 12.0 | D. | 11.7 |
9.在蒸发发皿中加热蒸干并灼烧(低于400℃)下列的溶液,可以得到该物质的固体是( )
| A. | 氯化铝溶液 | B. | 硫酸亚铁溶液 | C. | 碳酸氢钠溶液 | D. | 硫酸铝溶液 |
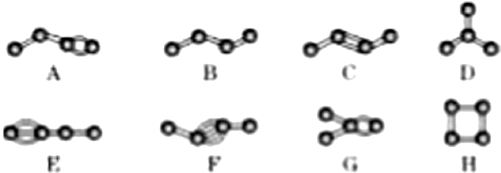

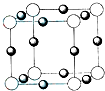 X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.
X、Y、Z、W、U五种元素,均位于周期表的前四周期,它们的核电荷数依次增加,且核电荷数之和为57.Y原子的L层p轨道中有2个电子,Z的原子核外有三个未成对电子,W与Y原子的价电子数相同,U原子的K层电子数与最外层电子数之比为2:1,其d轨道处于全充满状态.