14.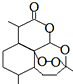 1971年,中国科学家发现、分离、提纯了用于治疗疟疾的“青蒿素”,拯救了数千万人的生命.屠呦呦起了重要的作用,因而与另两位外国科学家获得2015年诺贝尔医学奖.青蒿素分子结构如图.下列说法错误的是( )
1971年,中国科学家发现、分离、提纯了用于治疗疟疾的“青蒿素”,拯救了数千万人的生命.屠呦呦起了重要的作用,因而与另两位外国科学家获得2015年诺贝尔医学奖.青蒿素分子结构如图.下列说法错误的是( )
 1971年,中国科学家发现、分离、提纯了用于治疗疟疾的“青蒿素”,拯救了数千万人的生命.屠呦呦起了重要的作用,因而与另两位外国科学家获得2015年诺贝尔医学奖.青蒿素分子结构如图.下列说法错误的是( )
1971年,中国科学家发现、分离、提纯了用于治疗疟疾的“青蒿素”,拯救了数千万人的生命.屠呦呦起了重要的作用,因而与另两位外国科学家获得2015年诺贝尔医学奖.青蒿素分子结构如图.下列说法错误的是( )| A. | 青蒿素可以起取代反应 | B. | 青蒿素中的氧均为-2价 | ||
| C. | 青蒿素可以和NaOH溶液反应 | D. | 青蒿素的分子式为C15H22O5 |
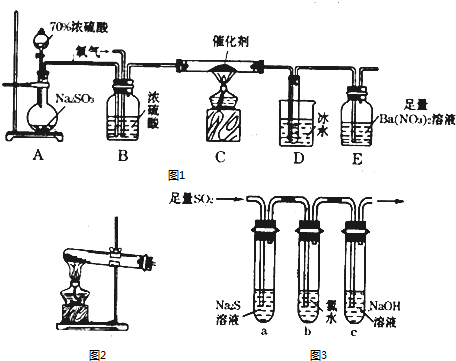
12.设NA为阿伏加德罗常数的值,下列叙述正确的是( )
| A. | 标准状况下,22.4L SO3中含有的分子数为NA个 | |
| B. | 标准状况下,2.24 L NH3和CH4的混合气体,所含电子总数为2NA | |
| C. | 7.1 g Cl2与足量的铁反应转移的电子数目是0.3NA | |
| D. | 1 mol C5H12分子中共价键总数为16NA |
11.下列关于含Mg、C元素的物质性质、存在和制备的叙述中,不正确的是( )
| A. | 自然界中,不存在镁单质,碳元素多种单质 | |
| B. | CO可以还原氧化铜,Mg能还原CO2,反应类型均为置换反应 | |
| C. | 电解熔融氯化镁可制备Mg单质和氯气,海水提取海盐后的卤水可用于提取氯化镁 | |
| D. | 煤与水蒸气高温反应生成水煤气,其主要成分是CO和H2 |
10.纳米碳是“纳米材料”中的一种,若将纳米碳均匀地分散到蒸馏水中,所形成的分散系①是浊液 ②是胶体 ③静置后析出黑色碳粒 ④能产生丁达尔效应.判断正确的是( )
| A. | ①②④ | B. | ②③④ | C. | ②④ | D. | ①③④ |
9.化学与生产、生活密切相关.下列叙述不正确的是( )
| A. | “地沟油”禁止食用,但可以用来制肥皂 | |
| B. | 氢氧化铝、碳酸氢钠都可用于治疗胃酸过多 | |
| C. | 为改善食物的色、香、味并防止变质,可在其中加入适量食品添加剂 | |
| D. | 用化纤面料替代棉质面料,以减少二氧化碳的排放 |
8.有机物的结构简式可以用键线式表示,如: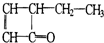 ,可表示为
,可表示为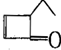 ,某有机物
,某有机物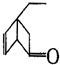 的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )
的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )
0 154119 154127 154133 154137 154143 154145 154149 154155 154157 154163 154169 154173 154175 154179 154185 154187 154193 154197 154199 154203 154205 154209 154211 154213 154214 154215 154217 154218 154219 154221 154223 154227 154229 154233 154235 154239 154245 154247 154253 154257 154259 154263 154269 154275 154277 154283 154287 154289 154295 154299 154305 154313 203614
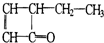 ,可表示为
,可表示为 ,某有机物
,某有机物 的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )
的多种同分异构体中,属于芳香醇的一共有(不考虑立体异构)( )| A. | 3种 | B. | 4种 | C. | 5种 | D. | 9种 |