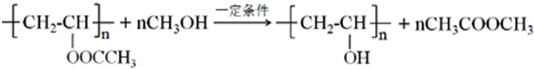
17. 我国本土科学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理和医学奖.已知二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )
我国本土科学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理和医学奖.已知二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )
 我国本土科学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理和医学奖.已知二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )
我国本土科学家屠呦呦因为发现青蒿素而获得2015年的诺贝尔生理和医学奖.已知二羟甲戊酸是生物合成青蒿素的原料之一,下列关于二羟甲戊酸的说法正确的是( )| A. | 与乙醇发生酯化反应生成产物的分子式为C8H18O4 | |
| B. | 能发生加成反应,不能发生取代反应 | |
| C. | 在铜的催化下与氧气反应的产物可以发生银镜反应 | |
| D. | 标准状况下1mol该有机物可以与足量金属钠反应产生22.4L H2 |
16.下列说法正确的是( )
| A. | 由反应SiO2+4HF═SiF4+2H2O,可知SiO2是碱性氧化物 | |
| B. | 由酸性溶液中MnO4-可以氧化Cl-,可知酸性溶液中MnO4-也能氧化Br- | |
| C. | 由反应CuSO4+H2S═CuS+H2SO4,可知酸性H2S>H2S04 | |
| D. | 由常温下金属钠、铝可溶于NaOH溶液,可知金属镁也能溶于NaOH溶液 |
15.X、Y、Z、W是原子序数依次增大的短周期元素,X的一种原子没有中子,Y、Z易形成质量比为3:4和3:8的两种常见化合物,W所在的周期数和族序数相同.下列说法正确的是( )
| A. | W的最高价氧化物对应水化物是强碱 | |
| B. | 原子半径:Y<Z<W | |
| C. | X、Y可以形成既有极性键也有非极性键的化合物 | |
| D. | 原子最外层电子数:W>Z>Y |
14.化学在工农业生产和日常生活中都有重要应用.下列叙述正确的是( )
| A. | 葡萄糖和蛋白质等高分子化合物是人体必需的营养物质 | |
| B. | 酸雨是指pH<7.0的雨水 | |
| C. | 居室中放置一盆石灰水可以吸收CO,预防中毒 | |
| D. | 用二氧化碳生产聚碳酸酯可以减少碳排放,以减缓温室效应 |
9.CuCl 是难溶于水的白色固体,是一种重要的催化剂.工业上,由孔雀石(主要成分Cu(OH)2•CuCO3,含FeS、FeO 和SiO2杂质)制备CuCl 的某流程如下

下列说法不正确的是( )

下列说法不正确的是( )
| A. | H2O2 将溶液1 中Fe2+氧化为Fe3+,再通过控制pH 转化为Fe(OH)3除去 | |
| B. | CO32-作用是控制溶液pH,促使CuCl 沉淀的生成 | |
| C. | SO32-将溶液3 中的Cu2+还原,反应得到CuCl | |
| D. | 若改变试剂加入顺序,将溶液3缓慢加入到含大量$\frac{S{O}_{3}^{2-}}{C{O}_{3}^{2-}}$的溶液中,同样可制取CuCl |
8. 25℃时,已知:
25℃时,已知:
H2CO3?H++HCO3- K1=4.3×10-7
HCO3-?H++CO32- K2=5.6×10-11
H2O?H++OH- KW=1.0×10-14
现取10.6g Na2CO3 与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH 的关系如图所示.在25℃时,下列有关溶液中离子浓度关系叙述正确的是( )
0 153980 153988 153994 153998 154004 154006 154010 154016 154018 154024 154030 154034 154036 154040 154046 154048 154054 154058 154060 154064 154066 154070 154072 154074 154075 154076 154078 154079 154080 154082 154084 154088 154090 154094 154096 154100 154106 154108 154114 154118 154120 154124 154130 154136 154138 154144 154148 154150 154156 154160 154166 154174 203614
 25℃时,已知:
25℃时,已知:H2CO3?H++HCO3- K1=4.3×10-7
HCO3-?H++CO32- K2=5.6×10-11
H2O?H++OH- KW=1.0×10-14
现取10.6g Na2CO3 与盐酸混合所得的一组体积为1L 的溶液,溶液中部分微粒与pH 的关系如图所示.在25℃时,下列有关溶液中离子浓度关系叙述正确的是( )
| A. | W 点所示的溶液中:c(Na+)+c(H+)=2c(CO32-)+c(OH-)+c(HCO3-) | |
| B. | pH=4 的溶液中:c(H2CO3)+c(HCO3-)+c(CO32-)=0.1 mol•L-1 | |
| C. | pH=8 的溶液中:c(H+)+c(H2CO3)+c(HCO3-)=c(OH-)+c(Cl-) | |
| D. | pH=11 的溶液中:CO32-+H2O HCO3-+OH- K≈1.8×l0-4 |