6.下列实验方案中,可以达到实验目的是
( )
| 选项 | 实验目的 | 实验方案 |
| A | 检验亚硫酸钠是否变质 | 先将亚酸钠样品溶于水配成溶液,然后加入足量稀盐酸酸化,再加入Ba(NO3)2溶液观察是否生成白色沉淀观察是否产生白色沉淀 |
| B | 除去苯中混有的苯酚 | 加入适量的溴水充分反应后过滤弃去沉淀 |
| C | 除去NaCl晶体中少量的KNO3杂质 | 先将晶体溶于水配成溶液,然后蒸发结晶并趁热过滤弃去滤液 |
| D | 检验CH3CH2Br中存在的溴元素 | 将CH3CH2Br与NaOH溶液共热,冷却后,取出上层水溶液,加入AgNO3溶液,观察是否产生淡黄色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
5.下列说法中正确的是( )
| A. | 分别与滴有酚酞的NaOH溶液共热可区别煤油与植物油 | |
| B. | 煤含有苯、甲苯等,先干馏后分馏获可得苯、甲苯等芳香烃 | |
| C. | 在水电离出H+浓度为1×10-12mol/L溶液中一定大量存在Fe2+、Na+、NO3-、Cl- | |
| D. | 在NH4HSO3溶液中加入少量NaOH溶液反应的离子方程式为NH4++OH-=NH3•H2O |
4.立方烷的结构简式如图所示.下列有关立方烷的说法中正确的是( )


| A. | 立方烷属于烷烃 | |
| B. | 立方烷的二氯代物有三种同分异构体 | |
| C. | 立方烷在通常情况下是气体 | |
| D. | 常温下立方烷能使酸性KMnO4溶液褪色 |
3.设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A. | 在过氧化钠与水的反应中,每生成0.1mol氧气,转移的电子数目为0.4NA | |
| B. | 氢氧燃料电池正极消耗22.4L气体时,电路中通过的电子数目为4NA | |
| C. | 在30g二氧化硅晶体中含有的共价键数目为2NA | |
| D. | 将常温下含NA个NO2、N2O4分子的混合气体冷却至标准状况,其体积约为22.4L |
2.化学与生产、生活密切相关.下列叙述错误的是( )
| A. | 大气中PM2.5比表面积大,吸附力强,能吸附许多有毒有害物质 | |
| B. | 在厨房里可用米汤检验加碘食盐中的碘 | |
| C. | 14C可用于文物年代的鉴定,14C与12C互为同位素 | |
| D. | 喝补铁剂时,加服维生素C效果更好,原因是维生素C具有还原性 |
19.工业上接触法生产硫酸的主要反应之一是:在一定的温度、压强和钒催化剂存在的条件下,S02被空气中的02氧化为S03.

(1)V205是钒催化剂的活性成分,郭汗贤等提出:V205在对反应I的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如图1:
①关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
由此计算反应I的△H=-98kJ•mol-1.
②反应Ⅱ、Ⅲ的化学方程式为S02+V205?V204•S03、2V204•S03+02?2V205+S03.
(2)某实验从废钒催化剂(主要成分为V2O5和V2O4)中回收V2O5,其简要过程如下:

(DVO2+和V02+可看成是钒相应价态的简单阳离子完全水解的产物).①写出水解生成V02+的离子方程式:V5++2H2O=V02++4H+.
②在沉钒时,为使钒元素的沉淀率达到98%,至少应调节溶液中的c(NH4+)为0.8mol/L[25℃,Ksp(NH4VO3)=1.6×10 -3,溶液体积变化忽略不计].
(3)在保持体系总压为0.1MPa的条件下进行反应:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g),原料气中SO2和02的物质的量之比(k)不同时,S02的平衡转化率与温度(t)的关系如2图所示:
①图中k1、k2、k3的大小顺序为k1>k2>k3,理由是相同温度和压强下,K值减小,氧气浓度越大,平衡正向移动,二氧化硫转化率提高.
②该反应的化学平衡常数Kp表达式为Kp=$\frac{P(S{O}_{3})}{P(S{O}_{2}){P}^{\frac{1}{2}}({O}_{2})}$(用平衡分压代替平衡浓度表示).图中A点原料气的成分是:n(SO2):n(O2):n(N2)=7:11:82,达平衡时SO2的分压p( SO2)的计算式为_$\frac{0.1×12%×7}{12%×7+11-0.5×88%×7+88%×7+82}$(分压=总压×物质的量分数).
③近年,有人研发出用氧气代替空气的新工艺,使SO2趋于完全转化.此工艺的优点除了能充分利用含硫的原料外,主要还有无尾气排放,不污染环境.

(1)V205是钒催化剂的活性成分,郭汗贤等提出:V205在对反应I的催化循环过程中,经历了Ⅱ、Ⅲ两个反应阶段,图示如图1:
①关气体分子中1mol化学键断裂时需要吸收的能量数据如下:
| 化学键 | S=O(SO2) | O=O(O2) | S=O(SO3) |
| 能量/KJ | 535 | 496 | 472 |
②反应Ⅱ、Ⅲ的化学方程式为S02+V205?V204•S03、2V204•S03+02?2V205+S03.
(2)某实验从废钒催化剂(主要成分为V2O5和V2O4)中回收V2O5,其简要过程如下:

(DVO2+和V02+可看成是钒相应价态的简单阳离子完全水解的产物).①写出水解生成V02+的离子方程式:V5++2H2O=V02++4H+.
②在沉钒时,为使钒元素的沉淀率达到98%,至少应调节溶液中的c(NH4+)为0.8mol/L[25℃,Ksp(NH4VO3)=1.6×10 -3,溶液体积变化忽略不计].
(3)在保持体系总压为0.1MPa的条件下进行反应:SO2(g)+$\frac{1}{2}$O2(g)?SO3(g),原料气中SO2和02的物质的量之比(k)不同时,S02的平衡转化率与温度(t)的关系如2图所示:
①图中k1、k2、k3的大小顺序为k1>k2>k3,理由是相同温度和压强下,K值减小,氧气浓度越大,平衡正向移动,二氧化硫转化率提高.
②该反应的化学平衡常数Kp表达式为Kp=$\frac{P(S{O}_{3})}{P(S{O}_{2}){P}^{\frac{1}{2}}({O}_{2})}$(用平衡分压代替平衡浓度表示).图中A点原料气的成分是:n(SO2):n(O2):n(N2)=7:11:82,达平衡时SO2的分压p( SO2)的计算式为_$\frac{0.1×12%×7}{12%×7+11-0.5×88%×7+88%×7+82}$(分压=总压×物质的量分数).
③近年,有人研发出用氧气代替空气的新工艺,使SO2趋于完全转化.此工艺的优点除了能充分利用含硫的原料外,主要还有无尾气排放,不污染环境.
18.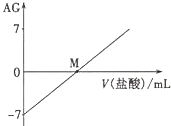 溶液的酸碱性可用酸度(AG)表示,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.室温下,将0.01mol•L-l盐酸逐滴滴人20.00mL 0.01 mol•L-l氨水中,溶液的AG变化如图所示.下列说法正确的是( )
溶液的酸碱性可用酸度(AG)表示,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.室温下,将0.01mol•L-l盐酸逐滴滴人20.00mL 0.01 mol•L-l氨水中,溶液的AG变化如图所示.下列说法正确的是( )
0 153975 153983 153989 153993 153999 154001 154005 154011 154013 154019 154025 154029 154031 154035 154041 154043 154049 154053 154055 154059 154061 154065 154067 154069 154070 154071 154073 154074 154075 154077 154079 154083 154085 154089 154091 154095 154101 154103 154109 154113 154115 154119 154125 154131 154133 154139 154143 154145 154151 154155 154161 154169 203614
 溶液的酸碱性可用酸度(AG)表示,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.室温下,将0.01mol•L-l盐酸逐滴滴人20.00mL 0.01 mol•L-l氨水中,溶液的AG变化如图所示.下列说法正确的是( )
溶液的酸碱性可用酸度(AG)表示,AG=lg$\frac{c({H}^{+})}{c(O{H}^{-})}$.室温下,将0.01mol•L-l盐酸逐滴滴人20.00mL 0.01 mol•L-l氨水中,溶液的AG变化如图所示.下列说法正确的是( )| A. | 室温下,0.01 mol•L-l盐酸的AG=12 | B. | M点时溶液中:c(NH4+)=c(Cl-) | ||
| C. | M点加入盐酸的体积大于20.00 mL | D. | M点以后NH4+的水解程度逐渐增大 |
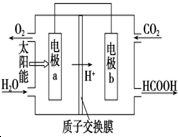 燃料的使用和防污染是社会发展中一个无法回避的矛盾话题.
燃料的使用和防污染是社会发展中一个无法回避的矛盾话题. 是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如所示:
是合成高聚酚酯的原料,其合成路线(部分反应条件略去)如所示:
 $→_{△}^{H_{2}O/H+}$
$→_{△}^{H_{2}O/H+}$
 .
. $→_{△}^{催化剂}$
$→_{△}^{催化剂}$ +H2O.
+H2O. ,与D互为同分异构体且含有碳碳双键的苯的二取代物有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是
,与D互为同分异构体且含有碳碳双键的苯的二取代物有6种,其中核磁共振氢谱为5组峰,且峰面积比为2:1:2:2:1的结构简式是 (任写一种).
(任写一种). )的
)的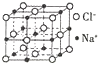 由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症.
由C、N、O、Na、Fe五种元素组成的配合物Na2[Fe(CN)5(NO)]可用于治疗高血压急症.