16.对于反应:3BrF3+5H2O=Br2+HBrO3+O2+9HF,下列说法正确的是( )
| A. | 该反应中,有三种元素化合价发生改变 | |
| B. | 该反应的氧化剂为BrF3,氧化产物为O2 | |
| C. | 1.5molBrF3参加反应,有4mole一转移 | |
| D. | 1.5molH2O参加反应,被H2O还原的BrF3为0.4mol |
15.K、Ka、KW分别表示化学平衡常数、电离平衡常数和水的离子积,下列判断正确的是( )
| A. | 温度升高,三者都增大 | |
| B. | 室温下Ka(HCN)<Ka(CH3COOH),说明CH3COOH的电离度一定比HCN大 | |
| C. | 2SO2(g)+O2(g)?2SO3(g)平衡后,仅增大压强,平衡向右移动,但K值不变 | |
| D. | 化学平衡常数的大小与温度、浓度、催化剂等有关 |
14.已知下面三个数据:7.2×10-4、4.6×10-4、4.9×10-10分别是下列三种酸的电离常数,若已知下列反应可以发生:NaCl+HNO2═HCN+NaNO2,NaNO2+HF═HNO2+NaF.据此判断,下列叙述不正确的是( )
| A. | K(HF)=7.2×10-4 | B. | K(HNO2)=4.9×10-10 | ||
| C. | 反应NaCN+HF═HCN+NaF可以发生 | D. | K(HCN)<K(HNO2)<K(HF) |
12.W、X、Y、Z、Q是五种常见的短周期主族元素,原子序数依次增大,在周期表中W原子半径最小;X元素原子核外电子总数是其次外层电子数的3倍;W和Y、X和Z均位于同一主族;Q的非金属性在同周期元素中最强.下列说法正确的是( )
| A. | 简单离子半径:Y>Q | |
| B. | Q分别与X、Z形成的最简单化合物中化学键类型相同 | |
| C. | YW能与WQ发生复分解反应 | |
| D. | 最简单气态氢化物的稳定性:X<Z |
11.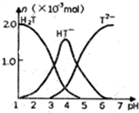 常温下,向10ml0.2mol•L-1草酸(用H2T表示)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的PH有如图关系,下列说法正确的是( )
常温下,向10ml0.2mol•L-1草酸(用H2T表示)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的PH有如图关系,下列说法正确的是( )
 常温下,向10ml0.2mol•L-1草酸(用H2T表示)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的PH有如图关系,下列说法正确的是( )
常温下,向10ml0.2mol•L-1草酸(用H2T表示)溶液中逐滴加入等浓度的NaOH溶液.有关微粒的物质的量与混合溶液的PH有如图关系,下列说法正确的是( )| A. | HT-在溶液中水解程度大于电离程度 | |
| B. | 当V(NaOH)=10mL时,溶液中水的电离程度比纯水大 | |
| C. | 当V(NaOH)=15mL时,溶液中存在:c(Na+)>c(HT-)>c(T2-)>c(OH-)>c(H+) | |
| D. | 当V(NaOH)=20mL时,溶液中存在:c(OH-)=c(HT-)+2c(H2T)+c(H+) |
10.下列各项中的两个量,其比值一定为2:1的是( )
| A. | 在相同温度下,等浓度的H2SO4和CH3COOH溶液中的c(H+) | |
| B. | 相同温度下,等浓度的Ba(OH)2和NaOH溶液,前者与后者的c(OH-) | |
| C. | 相同温度下,0.2 mol•L-1醋酸溶液和0.1 mol•L-1醋酸溶液中的c(H+) | |
| D. | 液面在“0”刻度时,50 mL碱式滴定管和25 mL碱式滴定管所盛液体的体积 |
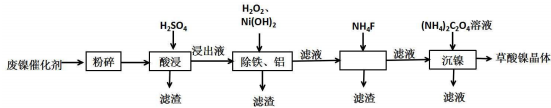
9.草酸镍晶体(NiC2O4•2H2O)可用于制镍催化剂,某小组用废镍催化剂(成分为Al2O3、Ni、Fe、SiO2、CaO等)制备草酸镍晶体的部分实验流程如图:
已知:①Ksp(CaF2)=1.46×10-10,Ksp(CaCO3)=2.34×10-9.
②相关金属离子生成氢氧化物沉淀的pH如表(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
(1)“粉碎”的目的是增大接触面积,加快反应速率,提高镍的浸出率.
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图.“酸浸”的适宜温度与时间分别为c(填字母).
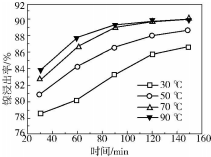
a.30℃、30min b.90℃、150min
c.70℃、120min d.90℃、120min
(3)将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110℃下烘干,得草酸镍晶体.用75%乙醇溶液洗涤的目的是洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失.
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为5.0≤pH<6.7.第2步中加入适量NH4F溶液的作用是除去杂质Ca2+.
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O.

已知:①Ksp(CaF2)=1.46×10-10,Ksp(CaCO3)=2.34×10-9.
②相关金属离子生成氢氧化物沉淀的pH如表(开始沉淀的pH按金属离子浓度为1.0mol•L-1计算).
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Al3+ | 3.0 | 5.0 |
| Ni3+ | 6.7 | 9.5 |
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图.“酸浸”的适宜温度与时间分别为c(填字母).

a.30℃、30min b.90℃、150min
c.70℃、120min d.90℃、120min
(3)将“沉镍”工序得到的混合物过滤,所得固体用75%乙醇溶液洗涤、110℃下烘干,得草酸镍晶体.用75%乙醇溶液洗涤的目的是洗去(NH4)2SO4杂质、便于烘干、减少草酸镍晶体损失.
(4)在除铁和铝工序中,应先加入H2O2氧化,再加氢氧化镍调节pH值的范围为5.0≤pH<6.7.第2步中加入适量NH4F溶液的作用是除去杂质Ca2+.
(5)将得到的草酸镍晶体在真空中加热至320℃分解可重新制得单质镍催化剂,写出该制备过程的化学方程式NiC2O4•2H2O$\frac{\underline{\;320℃\;}}{\;}$Ni+2CO2↑+2H2O.
8.为了减少CO对大气的污染,某学习小组拟研究CO和H2O反应转化为绿色能源H2
(1)已知:2CO(g)+O2(g)═2CO2(g);△H=-566kJ•moL-1
2H2(g)+O2(g)═2H2O(g);△H=-483.6KJ•moL-1
H2O (g)═H2O(l);△H=-44.0KJ•moL-1
写出CO和H2O(g)作用生成CO2和H2的热化学方程式CO(g)+H2O(g)=H2(g)+CO2(g)△H=-41.2KJ•moL-1
(2)在850℃时,反应:CO(g)+H2O(g)?CO2(g)+H2(g)的K=1.
①:若升高温度到950℃时,达到平衡时K<1(填“>”、“<”或“=”).
②:850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和x mol H2,若要使上述反应开始时向正反应方向进行,则x应满足的条件是x<3.
③:在②的条件下,按下列加料方式加料,达到平衡时H2的体积分数如下:
则:a=b(填“>”、“<”或“=”).
(3)H2是一种理想的绿色能源,可作燃料电池.
①若该氢氧燃料电池以KOH为电解质溶液,其正极的电极反应式是O2+4e-+2H2O═4OH-
②在25℃时,以氢氧燃料电池为电源,用石墨电极电解1000mL一定浓度的CuSO4溶液.5min后电解完全,在一个石墨电极上只有1.28g Cu生成.试回答下列问题:
电解的总反应式为2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4.
电解过程中转移的电子数为0.08mol,同时生成标准状况下气体的体积为0.896L.
0 153865 153873 153879 153883 153889 153891 153895 153901 153903 153909 153915 153919 153921 153925 153931 153933 153939 153943 153945 153949 153951 153955 153957 153959 153960 153961 153963 153964 153965 153967 153969 153973 153975 153979 153981 153985 153991 153993 153999 154003 154005 154009 154015 154021 154023 154029 154033 154035 154041 154045 154051 154059 203614
(1)已知:2CO(g)+O2(g)═2CO2(g);△H=-566kJ•moL-1
2H2(g)+O2(g)═2H2O(g);△H=-483.6KJ•moL-1
H2O (g)═H2O(l);△H=-44.0KJ•moL-1
写出CO和H2O(g)作用生成CO2和H2的热化学方程式CO(g)+H2O(g)=H2(g)+CO2(g)△H=-41.2KJ•moL-1
(2)在850℃时,反应:CO(g)+H2O(g)?CO2(g)+H2(g)的K=1.
①:若升高温度到950℃时,达到平衡时K<1(填“>”、“<”或“=”).
②:850℃时,若向一容积可变的密闭容器中同时充入1.0mol CO,3.0mol H2O,1.0mol CO2和x mol H2,若要使上述反应开始时向正反应方向进行,则x应满足的条件是x<3.
③:在②的条件下,按下列加料方式加料,达到平衡时H2的体积分数如下:
| 加料方式(mol) | H2的体积分数 | ||||
| 物质 | CO(g) | H2O(g) | CO2(g) | H2(g) | |
| 加料一 | 1 | 3 | 0 | 0 | a% |
| 加料二 | 0 | 1.2 | 0.6 | 0.6 | b% |
(3)H2是一种理想的绿色能源,可作燃料电池.
①若该氢氧燃料电池以KOH为电解质溶液,其正极的电极反应式是O2+4e-+2H2O═4OH-
②在25℃时,以氢氧燃料电池为电源,用石墨电极电解1000mL一定浓度的CuSO4溶液.5min后电解完全,在一个石墨电极上只有1.28g Cu生成.试回答下列问题:
电解的总反应式为2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4.
电解过程中转移的电子数为0.08mol,同时生成标准状况下气体的体积为0.896L.
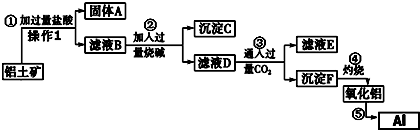
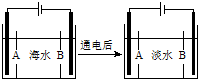 海南某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验.
海南某小岛上,可利用的淡水资源相当匮乏,解放军战士为了寻找合适的饮用水源,对岛上山泉水进行分析化验.